| 高二化学练习-烃 | ||||||||||||||||||||||||||||||||||||||||||||
|
一、选择(每小题不止一个答案) 1. 下列有机分子中,所有的原子不可能处于同一平面的是 2.用于制造隐形飞机物质具有吸收微波的功能,其主要成分的结构如图,它属于
B.烃 C.高分子化合物 D.有机物 3.m摩C2H2跟n摩H2在密闭容器中反应,当其达到平衡时,生成p摩C2H4.将平衡混合气体完全燃烧生成CO2和H2O,所需氧气的物质的量是( ).
4.下列物质有固定元素组成的是( ). (A)空气 (B)石蜡 (C)氨水 (D)二氧化氮气体 5、1,2,3-三苯基环丙烷的三个苯基可以分布在环丙烷环平面的上下,因此有如下两个异构体: 6.根据以下叙述,回答1~2小题. 1995年诺贝尔化学奖授予致力于研究臭氧层被破坏问题的三位环境化学家.大气中的臭氧层可滤除大量的紫外光,保护地球上的生物.氟利昂(如CCl2F2可在光的作用下分解,产生Cl原子,Cl原子会对臭氧层产生长久的破坏作用(臭氧的分子式为O3).有 关反应为:
(1).在上述臭氧变成氧气的反应过程中,Cl是( ). (A)反应物 (B)生成物 (C)中间产物 (D)催化剂 (2).O3和O2是( ). (A)同分异构体 (B)同系物 (C)氧的同素异形体 (D)氧的同位素 7.某烃的一种同分异构体只能生成一种一氯代物,该烃的分子式可以是( ). (A)C3H8 (B)C4H10 (C)C5H12 (D)C6H14 8.下列说法正确的是(N0表示阿伏伽德罗常数的值)( ). (A)标准状况下,以任意比例混和的甲烷和丙烷混和物22.4升,所含有的分子数为N0 (B) 标准状况下,1升辛烷完全燃烧后,所生成气态产物的分子数为
(C)常温常压下,活泼金属从盐酸中置换出1摩H2,发生转移的电子数为2N0 (D)常温常压下,1摩氦气含有的核外电子数为4N0 9.120℃时,1体积某烃和4体积O2混和,完全燃烧后恢复到原来的温 (A)1 (B)2 (C)3 (D)4 10.描述CH3—CH=CH—C≡C—CF3分子结构的下列叙述中,正确的是( ). (A)6个碳原子有可能都在一条直线上 (B)6个碳原子不可能都在一条直线上 (C)6个碳原子有可能都在同一平面上 (D)6个碳原子不可能都在同一平面上 11.CaC2和MgC2都是离子化合物.下列叙述中正确的是 12.两种气态烃以任意比例混合,在105℃时1 L该混合烃与9 L氧气混合,充分燃烧后恢复到原状态,所得气体体积仍是10 L.下列各组混合烃中不符合此条件的是 (A)CH4 C2H4 (B)CH4 C3H6 (C)C2H4 C3H4 (D)C2H2 C3H6 13.实验测得乙烯与氧气混和气体的密度是氢气14.5倍,可知其中乙烯的质量百分比为 (A)25.0% (B)27.6% (C)72.4% (D)75.0% 14.少量下列化学药品应保存水里的是 [ ]. (A)金属钾 (B)白磷 (C)硫磺 (D)苯 15.设计了四种制备气体的方案:①加热稀硫酸和乙醇制备乙烯;②加热稀盐酸和二氧化锰制备氯气;③用稀硫酸和大理石制备二氧化碳;④用稀硝酸和硫化亚铁制备硫化氢.不宜采用的方案有哪些? (A)只有①和② (B)只有②和③
根据以下叙述,回答第16和17题
16.跟(Ⅰ)、(Ⅱ)式等同的结构式是 [ ]. 17.跟(Ⅰ)、(Ⅱ)式是同分异构体的是 [ ].
二、填空
18.工程塑料ABS树脂(结构简式如下),合成时用了三种单体 这三种单体的结构简式分别是: 、 、 . 19.以苯、硫酸、氢氧化钠、亚硫酸钠为原料、经典的合成苯酚的方法可简单表示为:
20.羧酸酯RCOOR′在催化剂存在时可跟醇R″OH发生如下反应
此反应称为酯交换反应,常用于有机合成中.
在合成维纶的过程中,有一个步骤是把聚乙酸乙烯酯 交换反应来实现的. (1)反应中甲醇为什么要过量? . (2)写出聚乙烯醇的结构简式: . (3)写出聚乙酸乙烯酯与甲醇进行酯交换反应的化学方程式: . 21.下图是一套实验室制气装置,用于发生、干燥和收集气体.下列各组物质中能利用这套装置进行实验的是 (填正确选项的标号). (A)铜屑和浓硝酸 (B)二氧化锰和浓盐酸 (C)电石和水
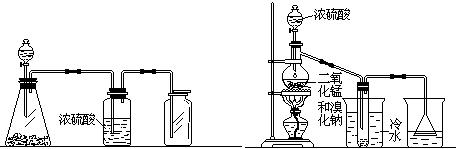
(D)碳酸钙和稀盐酸 22.根据右上图实验,填空和回答问题: (1)烧瓶中所发生的主要反应的化学方程式是 ,装置(Ⅱ)的烧杯中冷水所起的作用是 ,装置(Ⅲ)的烧杯中液体的作用是 . (2)进行此实验时,烧瓶内的橡皮塞最好用锡箔包住,用橡皮管连接的两玻璃管口要相互紧靠,这是因为 . (3)装置(Ⅲ)烧杯中使用倒置漏斗可防止液体倒吸,试简述其原因.
23. 1,2 - 二溴乙烷可作汽油抗爆剂的添加剂,常温下它是无色液体,密度2.18 g·cm-3,沸点131.4℃,熔点9.79℃,不溶于水,易溶于醇、醚、丙酮等有机溶剂.在实验室中可以用下图所示装置制备1,2- 二溴乙烷.其中分液漏斗和烧瓶a中装有乙醇和浓硫酸的混合液,试管d中装有液溴(表面覆盖少量水). 填写下列空白: (1)写出本题中制备1,2-二溴乙烷的两个化学反应方程式. ___________________________________________________________ ___________________________________________________________ (2)安全瓶b可以防止倒吸,并可以检查实验进行时试管d是否发生堵塞.请 (3)容器c中NaOH溶液的作用是:__________________________________. (4)某学生在做此实验时,使用一定量的液溴,当溴全部褪色时,所消耗乙醇和浓硫酸混合液的量,比正常情况下超过许多.如果装置的气密性没有问题,试分析其可能的原因. ___________________________________________________________ ___________________________________________________________
24. 合成分子量在2000-50000范围内具有确定结构的有机化合物是一个新的研究领域.1993年报道合成了两种烃A和B,其分子式分别为C1134H1146C1398H1278. B分子比A分子多了 个这样的结构单元(填写数字). 25.实验室制备硝基苯的主要步骤如下: ①配制一定比例的浓硫酸与浓硝酸的混和酸,加入反应器中. ②向室温下的混和酸中逐滴加入一定量的苯,充分振荡,混和均匀. ③在50-60℃下发生反应,直至反应结束. ④除去混和酸后,粗产品依次用蒸馏水和5%NaOH溶液洗涤,最后再用蒸馏水洗涤. ⑤将用无水CaCl2干燥后的粗硝基苯进行蒸馏,得到纯硝基苯. 填写下列空白: (1)配制一定比例浓硫酸与浓硝酸混和酸时,操作注意事项是: . (2)步骤③中,为了使反应在50-60℃下进行,常用的方法是 . (3)步骤④中洗涤、分离粗硝基苯应使用的仪器是 . (4)步骤④中粗产品用5%NaOH溶液洗涤的目的是 . (5)纯硝基苯是无色,密度比水 (填"小"或"大"),具有 气味的油状液体. 26.常温下,一种烷烃A和一种单烯烃B组成混和气体,A或B分子最多只含有4个碳原子,且B分子的碳原子数比A分子的多. (1) 将1升该混和气体充分燃烧,在同温同压下得到2.5升CO2气体.试推断原混和气体中A和B所有可能的组合及其体积比,并将结果填入下表: (2) 120℃时取1升该混和气体与9升氧气混和,充分燃烧后,当恢复到120℃和燃烧前的压强时,体积增大6.25%.试通过计算确定A和B的分子式.
27. (1)已知某混和气体的体积百分组成为80.0%CH4、15.0%C2H4和 5.00%C2H6.请计算0.500摩该混和气体的质量和标准状况下的密度(克/升). (2)CH4在一定条件下催化氧化可以生成C2H4、C2H6(水和其它反应产物忽略不计).取一定量CH4经催化氧化后得到一种混和气体,它在标准状况下的密度为0.780克/升.已知反应中CH4消耗了20.0%,计算混和气体中 C2H4的体积百分含量.(本题计算过程中请保持3位有效数字) 28. 1996年诺贝化学奖授予对发现C60有重大贡献的三位科学家.C60分子是形如球状的多面体(如图),该结构的建立基于以下考虑:
②C60分子只含有五边形和六边形;
③多面体的顶点数、面数和棱边数的关系,遵循欧拉定理: 据上所述,可推知C60分子有12个五边形和20个六边形,C60分子所含的双键数为30. 请回答下列问题: (1)固体C60与金刚石相比较,熔点较高者应是____________,理由是: _________________________________________________________. (2)试估计C60跟F2在一定条件下,能否发生反应生成C60F60(填“可能”或“不可能”)_________________________,并简述其理由:________________________________________________________. (3)通过计算,确定C60分子所含单键数. C60分子所含单键数为_______________. (3) C70分子也已制得,它的分子结构模型可以与C60同样考虑而推知.通过计算确 (4)C70分子中五边形和六边形的数目. C70分子中所含五边形数为__,六边形数为_______. |
教育最重要的是使人变得更聪明。教育就是要开启人的心智,使人身体好,更主动、积极,行动能力强,更能干。
中文域名: 古今中外.com
英文域名: www.1-123.com
丰富实用的教育教学资料

 A.无机物
A.无机物 








 ①C60分子中每个碳原子只跟相邻的3个碳原子形成
①C60分子中每个碳原子只跟相邻的3个碳原子形成