
A.54.7% B.45.3% C.11.8% D.4.53%
2.下列计算式正确的是: [ ]

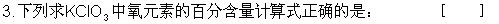
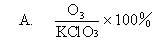
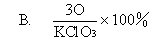
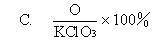
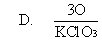

A.21.4千克 B.10.7千克
C.2.14千克 D.32.1千克
5.测知硝酸铵样品其含氮量为34.3%,则这种硝酸铵样品的纯度是:[ ]
A.65.7% B.82%
C.96% D.98%
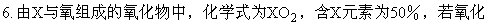
物中含X元素为40%,其化学式应为: [ ]
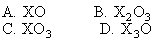
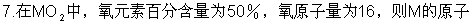
量是: [ ]
A.8 B.16
C.32 D.64
8.还原某金属氧化物,得到金属M,质量减少36.8%,如果金属M的
原子量为55,则该金属氧化物是: [ ]

A.含氧原子个数比为2∶3
B.含氧元素质量比为6∶5
C.含硫原子个数比为1∶1
D.含硫元素质量比为5∶4
10.某无水盐M的式量是106。经测定2.65克此无水盐能跟4.5克水结
合成结晶水合物。这种结晶水合物的化学式是: [ ]

镁原子的质量是: [ ]

12.20℃时,18克食盐溶于50克水中形成饱和溶液,则: [ ]
A.食盐的溶解度为18克
B.食盐的溶解度为36克
C.20℃时,食盐溶解度为36
D.20℃时,食盐的溶解度为36克
13.在一定温度下,某物质的溶解度为n克,其饱和溶液的百分比浓度为
m%,则n、m在数值上的关系为: [ ]
A.n>m B.n<m
C.n=m D.没有一定关系
14.t℃时,甲物质的饱和溶液的质量百分比浓度为15%,乙物质的
溶解度为15克,丙物质的10克饱和溶液蒸干后可得1.5克丙,当这
三种物质的饱和溶液质量相等时,所含溶质量的大小顺序是:[ ]
A.甲=丙>乙 B.丙>甲=乙
C.甲>乙>丙 D.乙>甲>丙
15.M克m%的食盐溶液与N克n%的食盐溶液相混合,所得的混合溶
液的百分比浓度是: [ ]
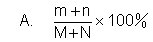
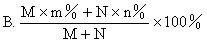
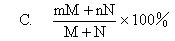
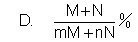

的质量百分比浓度最接近的值是: [ ]
A.78.2% B.43.9%
C.56.10% D.12.20%
17.t℃时,将W克某物质溶于V毫升水中制成饱和溶液,若继续加入B
克该物质,则溶液的百分比浓度为: [ ]
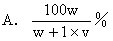
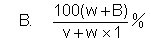
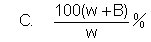
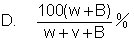
18.x物质的不饱和溶液100克,其浓度为20%,向该溶液再加入20克
x物质(全部溶解),此时该溶液的百分比浓度为: [ ]
A.40% B.20%
C.16.7% D.33.3%
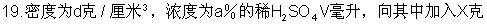
铁粉,恰好完全反应,则X值: [ ]
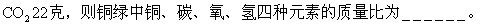
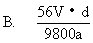
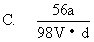
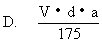
20.20℃时,甲物质溶液的浓度为60%,乙物质溶液的浓度为40%,温
度不变,减少等质量的溶剂,析出晶体的质量
①甲>乙②甲<乙③甲=乙④无法确定其中正确的是: [ ]
A.只有① B.①和③ C.②③和④ D.只有④
21.把红磷放在氧气中燃烧制取15克五氧化二磷,如果氧气由氯酸钾与
二氧化锰共热制得,所需氯酸钾的质量是: [ ]
A.21.6克 B.43.2克 C.21克 D.6.9克
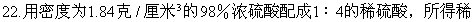

A.20% B.80% C.30.88% D.19.7%
23.用12.25克氯酸钾和3克二氧化锰混合加热制取氧气,反应完全后还
残留固体物10.45克,此反应氯酸钾的分解百分率是: [ ]
A.100% B.80% C.50% D.60%
24.浓度为4%的氢氧化钠溶液250克,吸收了5.5克二氧化碳,所得碳
酸钠溶液的百分比浓度是: [ ]
A.5.40% B.2.2% C.5.30% D.5.19%



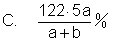

26. 9.5克不纯的氯化镁与足量的硝酸银溶液反应生成氯化银沉淀30.5
克,则氯化镁中可能含有的物质是: [ ]

27.加热14.7克氯酸钾和二氧化锰的混合物,充分反应后,得到固体物
质9.9克,根据质量守恒定律,加入催化剂的质量是: [ ]
A.2.45克 B.9.6克
C.1.25克 D.4.8克
28.在氯化铁和硫酸铁混合溶液中.已知铁离子和氯离子个数比为
5∶3,若溶液中铁离子为5n个,则硫酸根离子的个数为:[ ]
A.10n B.6n
C.5n D.3n
二、填空题(共44分)
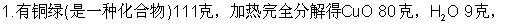
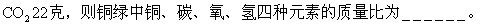

的质量比Cu∶S∶O∶H为_______________。
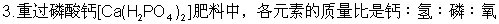
=_____________;所含磷的百分率是_______________。
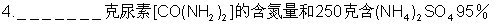
的硫铵的含氮量相等。
5.标准碳原子的质量A千克,硫原子质量是B千克,则硫的原子量是
_______________,如果已知镁的原子量为M,则镁原子的质量为
_______________。
6.在A+B=C+D的反应中,生成物C和D的质量比为1∶3,若
反应物A与B在反应中共消耗4.8克,则生成C的质量是
_______________克,生成D的质量是_______________克。
7. 21克碳酸镁在高温下完全分解,生成氧化镁10克。测得氧化镁里镁
元素的质量占60%,二氧化碳里含的碳元素和氧元素的质量比为
3∶8,根据上述数据计算碳酸镁里各元素的质量之比是_______。
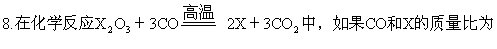

9.10℃时,蒸干50克饱和食盐溶液,得到晶体13.18克,则食盐在
10℃时的溶解度为_______________克。
10.20℃时,将m克KCl完全溶于n克水中,恰好配成100克饱和溶
液,则20℃时,KCl的溶解度为_______________克,该饱和溶液
的百分比浓度为_______________。
11.t℃时用A克X物质溶于水,配成B克饱和溶液,则该物质在t℃
时的溶解度为_______________,若温度不变,蒸发掉C克水,可析
出_______________克X物质。
12.20℃时,某物质的不饱和溶液的浓度为10%,若再加入5克该物质
或蒸发掉32.26克水,都可以成为饱和溶液。那么,该物质在20℃时
的溶解度是_______________。
13.配制10%的硫酸铜溶液200克,要用胆矾_______________克,水
_______________克。
14.从20%的某溶液中取出3/4,在剩余液体中加水至原质量,再倒回
1/2,则剩余溶液的质量百分比浓度为_______________。
15.50℃的氯化铵饱和溶液250克,计算:
(1)蒸发掉80克水后,温度仍降到50℃,析出_______________克氯
化铵晶体。(50℃时,氯化铵的溶解度是50克)
(2)析出晶体后氯化铵溶液的百分比浓度是_______________。
16.已知t℃A物质的溶解度是25克。试回答:
t℃时,200克A溶液中含A30克,溶液是否饱和____________
(填饱和、不饱和)。需加入_______________克A或蒸发掉__________
克水,溶液才达到饱和状态。
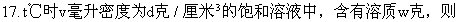
t℃时,该物质的溶解度是_______________克;该溶液的质量百分
比浓度为_______________。
18.在2升30%氢氧化钠溶液中(密度为1.33克/毫升),含有_________克
NaOH,_______________克水。
19.一块质量为7克的锌,可能含有Fe、Mg、Ca、Cu中的一种杂
质,让这块锌与足量盐酸反应,生成氢气0.2克,则锌块中所含杂质
是_______________。
20._______________克锌与_______________克浓度为20%的盐酸恰好
完全反应,所得氢气能把16克氧化铜全部还原成铜。
21.用28%的氢氧化钾溶液中和250克36.5%的盐酸溶液。
试求:完全中和这种盐酸需28%的氢氧化钾溶液_______________
克;生成的溶液百分比浓度为_______________。

