化学试卷
本试卷分选择题和非选择题两部分,满分120分。考试时间100分钟。
可能用到的相对原子质量: 2007.10,12
H -1 C- 12 O-16 N -14 Na-23 Cl 35.5 K-39 Ca-40 Ba 137
I卷选择题(共57分)
一、选择题(本题包括10小题,每小题3分,共30分,每小题只有一个选项符合题意)
1.自然界里常见金属元素存在最多的是Al,其次是铁,铜的含量较少。然而人类冶炼金属获得成功最早的反而是含量少的铜,含量最多的铝最迟冶炼出来。金属是当今社会最不可缺少的材料之一。下列有关金属的说法不正确的是 ( )
A.铜比铝先获得成功冶炼原因是,铜矿较易还原,铝矿很难还原。
B.目前已制得的纯金属只有90多种,但制得的合金已达几千种,大量使用的不是纯金属而是它们的合金。
C.生铁易生锈不耐蚀,但纯铁具有耐蚀性,所以不锈钢应是最纯的铁。
D.废弃铝质包装既浪费金属材料又造成环境污染
2、利用新技术能将不锈钢加工成柔软的金属丝,它可以和棉纤维一起编织成为防辐射的劳防服装,这是利用了金属的
A.耐腐蚀性 B.还原牲 C.热传导性 D.延展性
3、环境污染问题越来越受到人们的关注,造成环境污染的主要原因大多是由于人类生产活动中过度排放有关物质引起的。下列环境问题与所对应的物质不相关的是 ( )
A、温室效应——二氧化碳 B、光化学污染——二氧化氮
C、酸雨——二氧化碳 D、臭氧层破坏——氟氯烃
4、小华家中有如下生活用品:碘酒、食盐、食醋、84消毒液(内含NaClO),小华利用上述用品不能完成的任务是
A.检验买来的奶粉中是否加有淀粉 B.检验自来水中是否含有Cl-
C.除去保温瓶中的水垢 D.洗去白色衣服上的番茄汁
5.“空对空”响尾蛇导弹头部的“红外眼睛”,能分辩出0.001℃的温差变化,它是由热敏陶瓷材料和热释电陶瓷材料做成的。下列叙述中不正确的是 ( )
A.“红外眼睛”对热非常敏 B.“红外眼睛”的热目标是敌机发动机或尾部喷口高温区
C.“红外眼睛”的电阻值随温度明显变化 D.“红外眼睛”的工作原理与人眼相同
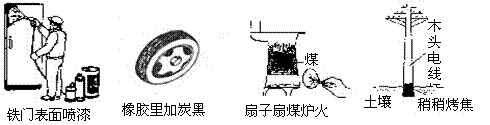
6.通过控制或改变反应条件可以加快、减缓甚至阻止反应的进行,使化学反应有利于人类的生存和提高生活质量。下列各图所示的措施中,能加快化学反应速率的是
|
铁门表面喷漆 |
|
橡胶里加炭黑 |
|
扇子扇煤炉火 |
|
煤 |
|
土壤 |
|
稍稍烤焦 |
|
木 头 电 线 杆 |
 |
A B C D
7、下面有关硅的叙述中,正确的是( )
A. 光导纤维是以硅酸盐为主要原料制成的
B.硅是构成矿物和岩石的主要元素,硅在地壳中的含量在所有的元素中居第一位
C.硅的化学性质不活泼,在自然界中可以以游离态存在
D.硅在电子工业中,是最重要的半导体材料
8.某工厂用CaSO4、NH3、H2O、CO2制备(NH4)2SO4,其工艺流程如下:
|
CaSO4悬浊液 |
|
甲 |
|
足量NH3 |
|
乙 |
|
适量CO2 |
|
过滤 |
|
滤液 |
|
CaCO3 |
|
提纯 |
|
煅烧 |
|
生石灰 |
|
(NH4)2SO4 |
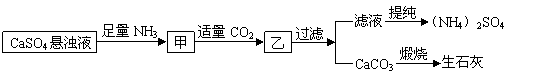 |
下列推断不合理的是 ( )
A.直接蒸干滤液得到纯净的(NH4)2SO4
B.生成1mol(NH4)2SO4至少消耗2molNH3
C.CO2可被循环使用
D.往甲中通CO2有利于(NH4)2SO4生成
9.泽维尔用飞秒(时间单位:1飞秒=10-15秒)激光技术研究了氰化碘(ICN)的分解反应 ICN→I+CN,发现该变化可在200飞秒内完成。已知(CN)2和卤素的性质相似。以下有关ICN的叙述中正确的是( )
A ICN不能和NaOH溶液反应 B ICN是一种共价化合物
C 将ICN加入到氯水中可生成I2 D ICN的晶体是离子晶体
10.一些盐的结晶水合物,在温度不太高时就有熔化现象,即熔溶于自身的结晶水中,又同时吸收热量。它们在塑料袋中经日晒就熔化,又在日后缓慢凝聚而释放热量。故可用于调节室内的温度,或作夏日防暑用枕垫或座垫,这些物质可称之为潜热材料。现有几种盐的结晶水合物有关数据如下:
|
物 |
|
质 |
|
数 |
|
据 |

① ![]()
② ![]()
③ ![]()
④ ![]()
熔点(℃)
40~50
29.92
32.38
35.1
溶化热
(kJ·mol-1)
49.7
37.3
77
100.1
根据上述数据,实际应用时最常采用的(由来源和成本考虑)应该是
A.① B.② C.③ D.④
二、选择题(本题共9小题,每小题3分,共27分。每小题有一或两个选项符合题意)
11、蛇纹石由MgO、A12O3、SiO2、Fe2O3组成。现取一份蛇纹石试样进行实验,首先将其溶于过量的盐酸,过滤后,在所得的沉淀X和溶液Y中分别加入NaOH溶液至过量。下列叙述不正确的是
A.沉淀X的成分是SiO2
B.将蛇纹石试样直接溶于过量的NaOH溶液后过滤,可得到红色颜料Fe2O3,
C.在溶液Y中加入过量的NaOH溶液,过滤得到的沉淀的主要成分是Fe(OH)3和Mg(OH)2
D.溶液Y中的阳离子主要是Mg2 、Al3 、Fe3 、H
12.下列离子方程式,正确的是 ( )
A.在溶液中亚硫酸氢铵与等物质的量氢氧化钠混合
![]()
B.碳酸钠溶液中加入二氧化硅:CO32- SiO2==SiO32- CO2↑
C.二氧化硅与烧碱溶液反应:SiO2 2OH- === SiO32- H2O
D.硅酸与烧碱溶液中和:H2SiO3 2OH- === SiO32- 2H2O
13.某同学用一小块铝片和盐酸反应制取H2,实验现象如下表:
|
时间 |
1 min |
2 min |
5 min |
15 min |
20 min |
|
现象 |
少量气泡 |
较多气泡 |
大量气泡 |
反应剧烈 |
铝片耗尽 |
反应1~15min内,铝与盐酸的反应速率变化的可能原因是 ( )
A.该反应是放热反应,温度升高 B.反应过程中盐酸的浓度增大
C.随着反应的进行,铝片表面积变小 D.Cl-离子是该反应的催化剂
14.用NA表示阿伏加德罗常数的值,下列说法中正确的是
A.0.36 g水中所含中子数一定为0.2 NA
B.4.48 L N2与CO的混合物所含分子数一定为0.2 NA
C.6.4 gS6与S8的混合物中所含S原子数一定为0.2 NA
D.标准状况下,2.24 L氧气所含原子数一定为0.2 NA
15.实验室需配制一种仅含四种离子(不包括水电离出的离子)的无色混合溶液,且在混合溶液中四种离子的物质的量浓度均为lmol·L-1。下面四个选项中能达到此目的的是
A.NH4+、Na+、NO3-、Cl- B.Cu2+、K+、SO42—、NO3—
C.H+、K+、HCO3-、Cl— D.Mg2+、Na+、Cl—、SO42—
16.已知酸性条件下有如下反应:2Cu =Cu2 Cu。由于反应温度不同,用氢气还原氧化铜时,可能产生Cu或Cu2O,两者都是红色固体。一同学对某次用氢气还原氧化铜实验所得的红色固体产物作了验证,实验操作和实验现象记录如下 ( )
加入试剂
稀硫酸
浓硫酸、加热
稀硝酸
浓硝酸
实验现象
红色固体
和蓝色溶液
无色气体
无色气体
和蓝色溶液
红棕色气体
和绿色溶液
由此推出本次氢气还原氧化铜实验的产物是
A.Cu B.Cu2O
C.一定有Cu,可能有Cu2O D.一定有Cu2O,可能有Cu
17.t℃时CuSO4的溶解度是S g,其饱和溶液密度d g.cm-3、物质的量浓度为c mol.L-1。向足量饱和溶液中加入m g无水CuSO4或蒸发掉n g水后恢复t℃,均能获得W g胆矾晶体,下列关系式正确的是( )
A. ![]() B.
B. ![]()
C. ![]() D.
D. ![]()
18.有10 g不纯CaCO3样品与足量盐酸作用后生成4.44 g CO2,且溶液中残留难溶物质。则对于此样品中是否存在①MgCO3 ②K2CO3 ③SiO2杂质的判定正确的是( )
A.肯定含①③,不含② B.肯定含①③,可能含②
C.肯定含②③,不含① D.肯定含②③,可能含①
19.某学生用NaHCO3,和KHCO3,组成的某混合物进行实验,测得如下数据(盐酸的物质的量浓度相等)
|
50mL 盐酸 |
50mL 盐酸 |
50mL 盐酸 | |
|
m(混合物) |
9.2g |
15.7g |
27.6g |
|
V(CO2)(标况) |
2.24L |
3.36L |
3.36L |
则下列分析推理中不正确的是
A.盐酸的物质的量浓度为3.0mol·L
B.根据表中数据不能计算出混合物中NaHCO3的质量分数
 C.加入混合物9.2g时盐酸过量
C.加入混合物9.2g时盐酸过量
D.15.7g混合物恰好与盐酸完全反应
|
三题(共2小题,12分)
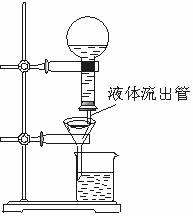
20、(6分)某学生为了使过滤操作能自动添加液体,设计
了“自动加液过滤器”,如图所示。在倒置的烧瓶中盛放
待过滤的液体,液体从“液体流出管”流入漏斗。为使液
体顺利流下,还需插入“空气导入管”与大气相通。
(1)“空气导入管”下口应在____ ,上口应在_______ 。
A.滤纸边沿下方 B.滤纸边沿上方
C.待过滤液液面上 D.待过滤液中
E.A和B项均可 F.C和D项均可
(2)试简要说明自动加液过滤的原理。
__________________________________________________
21.(6分)某研究小组拟用定量的方法测量Al和Fe分别与酸反应的快慢,设计了下图1所示的装置。
|
铝丝或 铁丝 |
|
甲 |
|
乙甲 |
|
丙 |
|
图1 |
|
v |
|
t |
|
t1 |
|
t2 |
|
t3 |
|
图2 |
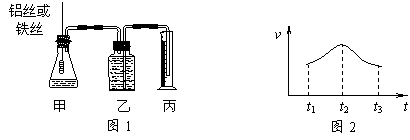 |
⑴检查图1装置气密性的方法是______________________________________。
⑵若要比较产生气体的快慢,可以测量相同时间内产生气体的体积,也可以测量___________________________________。
⑶实验测得铝丝产生气体的速率(v)与时间(t)的关系如上图2所示,则t1~t2时间内反应速率逐渐加快的主要原因是_______________________________________。
四题(共2小题,23分)
22(11分)、某校高一化学研究性学习小组对日常生活中的氯气用途进行了调查,了解到氯气可广泛地应用于衣物的漂白、水体的杀菌和消毒等。
(1)氯气可以用于漂白、消毒的原因是因为能与水作用形成具有 性的次氯酸,相关反应的离子方程式为 ;
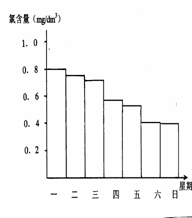 (2)在调查某室外游泳池夏季池水消毒情况时,小组成员了解到,该游泳池每周一上午8∶00换水,然后通入氯气消毒,通常游泳池水的含氯量控制在0.5 mg/L至1.0mg/L之间时,效果最好。右图是该小组测定的天天19∶00时泳池中水的氯含量,哪几天使用泳池不安全 ;
(2)在调查某室外游泳池夏季池水消毒情况时,小组成员了解到,该游泳池每周一上午8∶00换水,然后通入氯气消毒,通常游泳池水的含氯量控制在0.5 mg/L至1.0mg/L之间时,效果最好。右图是该小组测定的天天19∶00时泳池中水的氯含量,哪几天使用泳池不安全 ;
(3)你认为哪几天的天气炎热、阳光强烈 ,说出一种理由是 ;
(4)在对泳池水中通入氯气消毒时,当发生氯气泄漏时,应立即关闭氯气罐,还应采取下列自救方法 。(选填序号)
A、用湿润的毛巾捂住口鼻跑向低处
B、用浸湿小苏打或肥皂水的毛巾捂住口鼻跑向高处
C、用浸湿浓氨水的毛巾捂住口鼻匍匐跑至安全处
D、用浸湿食盐水的毛巾捂住口鼻顺风跑至安全处
(5)小型泳池通常使用漂白液(NaClO溶液)而非氯气来消毒池水,试举出使用漂白液而非氯气的一项理由 ;
(6)请再写出你能知道的能用于饮用水消毒的消毒剂(至少写三种,否则不得分)
请在你书写的药品中选择一种你认为最好的带上飞机,并说明它的原因。
选择 原因
23、(12分)胃酸过多是常见的胃病。下面是甲、乙两种常见胃药的说明摘要。
甲:①白色结晶状粉末,受热可缓缓分解;②能溶于水,水溶液呈弱碱性;灼烧时火焰为黄色;③遇酸及酸性药物则产生二氧化碳;④患者服用过量,可能引起胃胀气,甚至有引起胃溃疡穿孔的危险。
乙:①与胃酸是中和作用缓慢而持久,可维持3~4小时;②凝胶本身覆盖于溃疡面上,具有保护作用;③可溶于稀酸或氢氧化钠溶液中。
(1)请你推测,甲中含有的主要化学成份是 (填化学式);乙中含有的主要化学成份是 (填化学式)。
(2)试写出甲中含有的主要化学成份引起胃胀气反应的离子方程式:
。
(3)三硅酸镁Mg2Si3O8·nH2O也是常用胃药,被用来治疗胃溃疡,是因为该物质不溶于水,服用后中和胃酸作用持久。把三硅酸镁改写成氧化物形式为:_____ ____。
写出它中和胃酸(胃酸的主要成分是HCl)的化学方程式_______________________________。
(4)目前一种新型抗酸剂能迅速改善和缓解胃酸过多的症状,它主要由碳酸镁、氢氧化镁和氢氧化铝组成(说明:Mg(OH)2在高温下分解为MgO)。现按如下步骤测定药剂中三种主要成分的配比:
①取药剂样品,研磨后,加入50mL3.6 mol·L—1盐酸,正好完全反应并收集得到标准状况下224mL气体
②过滤,弃去其中不溶性物质(其余成分不参与反应)
③取②中滤液,加入足量的NaOH溶液后,过滤、洗涤、灼烧,所得固体2.4g。
则该药剂中三种主要成分的物质的量之比为n(MgCO3):n(Mg(OH)2):n(Al(OH)3)=_________。
五题(共2小题,25分)
24、(14分)某研究性学习小组探究下列化学反应的特征:
(I)KMnO4+KI+H2SO4→MnSO4+I2+KIO3+K2SO4+H2O
(Ⅱ)FeS+HNO3→Fe(NO3)3+Fe2(SO4)3+NO2↑+N2O4↑+NO↑+H2O
(Ⅲ)CuSO4→CuO+SO3↑+SO2↑+O2↑
(Ⅳ)CO2+KOH→KHCO3+K2CO3+H2O
⑴大多数化学反应中物质的化学计量数之比是固定的,但上述化学反应的化学计量数之比是不确定的,即物质的化学计量数有多组。根据上述实例,请用一句话归纳化学计量数有多组的化学反应的特点: 。
⑵反应(Ⅱ)中还原产物是 ,若其物质的量之比确定,该反应的化学计量数也随之确定。
⑶有人认为反应(Ⅲ)是两个反应式加合的结果,请分析它是哪两个化学反应加合而成的:______________________________________、_____________________________。
在反应(Ⅲ)中,根据电子转移守恒,物质_______和 的物质的量之比是固定的。
⑷若将16gCuSO4固体粉末按反应(Ⅲ)完全分解,最终气体产物的物质的量的取值
范围是: 。
⑸若反应(Ⅳ)中KHCO3、K2CO3的化学计量数分别为a、b,则用a、b表示该反应
的化学计量数的化学方程式是 。
25、(11分)下图中所有物质均为中学化学常见物质,F、H是气体单质,Z是固体金属单质,Y中阳离子与阴离子个数比为2:1 ,化合物X、Y、A、D、E、G的焰色反应为黄色,I是白色沉淀。
|
(1)写出X、E、I的化学式。X E I 。
(2)写出Y的电子式 。
(3)关于Y的说法正确的是 。
A.Y是氧化物 B.Y是过氧化物
C.Y是含有非极性键的离子化合物 D.Y是碱性氧化物
(4)写出B和Y反应的化学方程式: 。
(5)X和G的溶液能反应吗?如能反应,写出反应的离子方程式;如不能反应,请说明理由:
六题(共1小题,9分)
26.(9分)在一定量的石灰乳中通入一定量的氯气,二者恰好完全反应(发生反应的反应均为放热反应)。生成物中有三种含氯元素的离子,其中两种离子的物质的量(n)与反应时间(t)的曲线如图所示。已知,生成C1O3-离子的反应为:
6Ca(OH)2 6C12 5CaC12 Ca(C1O3)2 6H2O。
试回答:
(1)t2时,Ca(C1O)2与Ca(C1O3)2的物质的量之和为 mol,该石灰乳中含有的Ca(OH)2的质量是 g。
|
度升高引起的,通过氯气的速度不同,
C1O-和C1O3-的比例也不同。若在原石
灰乳中通入氯气的速度加快,则反应后
![]() 将 2(填“>”“<”
将 2(填“>”“<”
或“=”);若 ![]() =a,则n(C1-)= mol(用含a的代数式来表示)。
=a,则n(C1-)= mol(用含a的代数式来表示)。
附加题:本题仅供有有爱好的同学参考,不计入本次考试的成绩中。
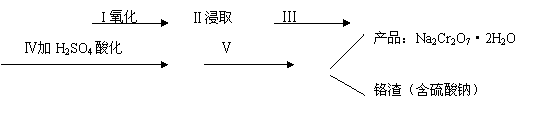
27.(14分)红矾钠(重铬酸钠:Na2Cr2O7·2H2O)是重要的基本化工原料,在印染工业、电镀工业和皮革工业中作助剂,在化学工业和制药工业中也用作氧化剂,应用领域十分广泛。
(1)实验室中红矾钠可用铬铁矿(主要成分:FeO·Cr2O3)利用以下过程来制取。
|
Ⅱ浸取 |
|
I氧化 |
|
Ⅲ |
|
Ⅳ加H2SO4酸化 |
|
Ⅴ |
|
产品:Na2Cr2O7·2H2O |
|
铬渣(含硫酸钠) |
 |
![]() 铬铁矿等原料 Na2CrO4溶液
铬铁矿等原料 Na2CrO4溶液
①步骤I中反应的化学方程式为:
![]() 该反应的化学平衡常数的表达式为 ,在常温下该反应速度极慢,下列措施中能使反应速率增大的是 。
该反应的化学平衡常数的表达式为 ,在常温下该反应速度极慢,下列措施中能使反应速率增大的是 。
A.升高温度 B.通入过量的空气 C.将原料粉碎 D.增加纯碱的用量
② 步骤Ⅱ中所得溶液显碱性,其中除含有Na2CrO4外还含有铝、硅元素的化合物,它们的化学式可能是 、 。
③ 步骤Ⅲ需将溶液的pH调至7~8并煮沸,其目的是 。
④ 步骤Ⅳ中发生反应的离子方程式为: 。
(2)将红矾钠与KCl固体1:2(物质的量比)混合溶于水后经适当操作可得到K2Cr2O7晶体。请填写表中空格。完成上述过程。
序号
实验步骤
简述实验操作(不必叙述如何组装实验装置)
①
溶解
将混合物放入烧杯中,加水,充分搅拌直到固体不再溶解。
②
③
④
⑤
过滤、干燥
得到K2Cr2O7晶体
© 2004-2010 中国哲士网版权所有 引用本站内容请指明来源 给本站投稿 备案序号 蜀ICP备05009253号