命题:朱凤琴 仲淑娴 组卷:周炳兴
可能用到的相对原子质量:H 1; C 12;O 16; Na 23;S 32;Cl 35.5;K 39;Ca 40;
Cu 64;Fe 56;Zn 65;Br 80;Ba 137
第Ⅰ卷(选择题,共48分)
一、单项选择题(本题包括8小题,每题3分,共24分。每题只是一个选项符合题意)
1. “纳米材料”(1nm=10-9m)是当今材料科学研究的前沿,其研究成果广泛应用于催化及军事科学中。“纳米材料”是指研究开发直径为几纳米至几十纳米的材料,如将“纳米材料”分散到液体分散剂中,对于所得分散系的叙述正确的是
①一定是溶液 ②能全部透过半透膜 ③有丁达尔现象 ④可以全部透过滤纸
A.①② B.②③ C.①④ D.③④
2.已知两瓶气体分别是HCl 和Cl2 ,可以区别它们的方法或试剂是
①观察颜色 ②打开瓶盖看有无白雾 ③湿润的淀粉试纸 ④湿润的红色石蕊试纸
⑤湿润的蓝色石蕊试纸 ⑥AgNO3 溶液
A.①②③④ B.①②⑤⑥ C.①②④⑤ D.①②③⑥
3.为达到预期的实验目的,下列操作正确的是
A.欲配制质量分数为10%的ZnSO4溶液,将l0 g ZnSO4·7H2O溶解在90 g水中
B.为鉴别KCl、AlCl3和MgCl2溶液,分别向三种溶液中滴加NaOH溶液至过量
C.欲制备F(OH)3胶体,向盛有沸水的烧杯中滴加FeCl3饱和溶液并长时间煮沸
D.为减小中和滴定误差,锥形瓶必须洗净并烘干后才能使用
4.设NA代表阿伏加德罗常数的数值,下列说法中正确的是
①常温常压下,17g甲基(—14CH3)所含的中子数为9NA
②常温常压22.4L NO气体的分子数小于NA
③64g的铜发生氧化还原反应,一定失去2NA个电子
④常温常压下,100mL 0.5mol/L 的乙酸溶液中,乙酸的分子数目小于0.05NA
⑤标况时,22.4L二氯甲烷所含有的分子数为NA
⑥常温常压下,1mol氦气含有的核外电子数为4NA
 A.①② B.③④ C.②④ D.⑤⑥
A.①② B.③④ C.②④ D.⑤⑥
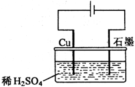
5.某同学按右图所示的装置进行电解实验。下列说法不正确的是
A.电解过程中,铜电极上有H2产生
B.电解初期,主反应方程式为: ![]()
C.电解一定时间后,石墨电极上有铜析出
D.电解过程中,溶液会出现蓝色絮状沉淀
6.一定条件下,碘单质与砹单质以等物质的量进行反应,可得AtI。它与Zn、NH3都能发生反应,化学方程式分别如下:
2AtI 2Zn==ZnI2 ZnAt2 AtI 2NH3(1)===NH4I At NH2
下列关于AtI性质的叙述正确的是
A.ZnI2既是氧化产物,又是还原产物
B.ZnAt2既是氧化产物,又是还原产物
C.AtI与液氨反应,AtI既是氧化剂,又是还原剂
D.AtI与液氨的反应中,得失电子数相等
7.进行化学实验,观察实验现象,通过分析推理得出正确的结论是化学学习方法之一。下列对有关实验事实的解释正确的是
A.溴水中通入SO2后,颜色褪去,说明SO2表现了漂白性
B.用惰性电极电解相同浓度的Cu(NO3)2和AgNO3混合溶液,阴极首先析出的是Ag,说明Ag+ 的还原性比Cu2+ 强
C.常温下,将铝片放入浓硫酸中无明显现象,说明铝不和冷的浓硫酸反应
D.浓硝酸在光照条件下变黄,说明浓硝酸易分解生成有色产物且溶于浓硝酸
8.向某二价金属M的M(OH)2溶液中加入过量的NaHCO3溶液,生成了MCO3沉淀,过滤,将沉淀置于足量的稀盐酸中,充分反应后,在标准状况下收集到V L气体,假如计算金属M的相对原子质量,你认为还必需提供下列哪项数据
A.M(OH)2溶液的物质的量浓度 B.与MCO3反应的盐酸的物质的量浓度
C.MCO3的质量 D.题给条件充足,不需要再补充数据
二、不定项选择题(本题包括8小题,每小题3分,共24分。每小题有一个或两个选项符合题意。)
9.有M、N两溶液,各含下列14种离子中的7种:Al3 、Cl-、Na 、K 、NO3-、OH-、S2-、MnO4-、Fe3 、AlO2-、CO32-、NH4 、SO42-、H 。已知两溶液所含离子各不相同,M溶液里的阳离子只有两种,则N溶液里的阴离子应该是
A.OH-、S2-、CO32- B.MnO4-、SO42-、NO3-
C.Cl-、NO3-、SO42- D.AlO2-、MnO4-、SO42-
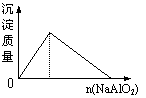
10.下列实验过程中产生的现象与对应的图形符合的是
|
n(SO2) |
|
0 |
|
pH |
|
7 |
|
n(NaAlO2) |
|
沉 淀 质 量 |
|
0 |
 | |||
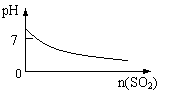 | |||
A.盐酸中加入NaAlO2溶液 B.SO2气体通入溴水中
|
n(H2O) |
|
pH |
|
0 |
|
醋酸 |
|
盐酸 |
|
1 |
|
7 |
 |
|
n(NH3) |
|
导 电 能 力 |
|
0 |
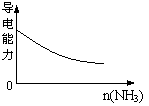
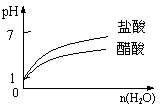
C.pH=1的醋酸与盐酸分别加水稀释 D.氨气通入醋酸溶液中
11.Na3N与NaH均为离子化合物,都能与水反应放出气体。下列有关叙述正确的是
A.二者中Na+半径都比阴离子大
B.与水反应时,水都作氧化剂
C.与水反应所得溶液均能使酚酞试液变红
D.二者与盐酸反应,前者可产生两种盐,后者只有一种盐生成。
12.下列反应的离子方程式错误的是
A.等物质的量的Ba(OH)2与NH4HSO4在稀溶液中反应:
Ba2 2OH— 2H SO42—=BaSO4↓ 2H2O
B.氢氧化铁与足量的氢溴酸溶液反应:Fe(OH)3 3H =Fe3 3H2O
C.足量的CO2通入饱和碳酸钠溶液中:CO2 2Na CO32— H2O=2NaHCO3↓
D.向碳酸氢钙溶液中滴入过量澄清石灰水:
Ca2 2HCO3— 2OH— =CaCO3↓ CO32— 2H2O
13.下列数据是对应物质的熔点
Na2O
NaCl
AlF3
AlCl3
920
801
1291
190
BCl3
Al2O3
CO2
SiO2
-107
2073
-57
1723
据此做出的下列判定中错误的是
A.铝的化合物的晶体中有的是离子晶体
B.表中只有BCl3和干冰是分子晶体
C.同族元素的氧化物可形成不同类型的晶体
D.不同族元素的氧化物可形成相同类型的晶体
14.短周期元素X、Y、Z的原子序数依次递增,其原子的最外层电子数之和为13。X与Y、Z位于相邻周期,Z原子最外层电子数是X原子内层电子数的3倍或者Y原子最外层电子数的3倍。下列说法正确的是
A.X的氢化物溶于水显酸性
B.Y的氧化物是离子化合物
C.Z的氢化物的水溶液在空气中存放不易变质
D.X和Z的最高价氧化物对应的水化物都是弱酸
15.下列各溶液中,微粒的物质的量浓度关系正确的是
A.10mL 0.5mol/L CH3COONa溶液与6mL 1mol/L盐酸混合:
c(Cl-)>c(Na+)>c(H+)>c(OH-)
B.0.1mol/L pH为4的NaHB溶液中:c(HB-)>c(H2B)>c(B2-)
C.在NaHA溶液中一定有:c(Na+)+c(H+)=c(HA-)+c(OH-)+c(A2-)
D.c(NH4+)相等的(NH4)2SO4溶液、(NH4)2CO3溶液和NH4Cl溶液:
c[(NH4)2SO4]<c[(NH4)2CO3]<c(NH4Cl)
16.某化学科研小组研究在其他条件不变时,改变某一条件对A2(g)+3B2(g) ![]() 2AB3(g)化学平衡状态的影响,得到如下图所示的变化规律(图中T表示温度,n表示物质的量),
2AB3(g)化学平衡状态的影响,得到如下图所示的变化规律(图中T表示温度,n表示物质的量),
|
n(B2)起始 |
|
AB3的平衡体积分数 |
|
a |
|
b |
|
c |
|
T1 |
|
T2 |
 根据如图可得出的判定结论正确的是
根据如图可得出的判定结论正确的是
A.正反应一定是放热反应
B.达到平衡时A2的转化率大小为:b>a>c
C.若T2>T1,则正反应一定是吸热反应
D.b点时,平衡体系中A、B原子数之比接近1∶3
08届高三化学上册六校联考试题
命题:朱凤琴 仲淑娴 组卷:周炳兴
第Ⅰ卷(选择题,共48分)
一、单项选择题(本题包括8小题,每题3分,共24分。每题只是一个选项符合题意)
题号
1
2
3
4
5
6
7
8
答案
二、不定项选择题(本题包括8小题,每小题3分,共24分。每小题有一个或两个选项符合题意。)
题号
9
10
11
12
13
14
15
16
答案
第Ⅱ卷(非选择题,共72分)
三、(本题包括2小题,共18分)
17.(8分)(1)指出下列实验仪器和用品(已洗涤干净)使用时的第一步操作:
①淀粉碘化钾试纸检验Cl2的性质 ;
②分液漏斗(分液) ;
(2)下列有关实验的叙述中,合理的是 ( 多选倒扣分)
A.用碱式滴定管量取25.00mL溴水
B.不宜用瓷坩埚灼烧氢氧化钠或碳酸钠
C.测定溶液的pH值时用干燥、洁净的玻璃棒蘸取溶液,滴在用蒸馏水湿润过的pH试纸上,再与标准比色卡比较
D.圆底烧瓶、锥形瓶、烧杯加热时都应垫在石棉网上
E.使用容量瓶配制溶液时,俯视刻度线定容后所得溶液浓度偏高
F.滴定用的锥形瓶和滴定管都要用所盛溶液润洗
G.配制硫酸溶液时,可先在量筒内加入一定体积的水,再在搅拌下慢慢加入浓硫酸
H.分液时,分液漏斗中下层液体从下口流出,上层液体从上口倒出
18.(10分)饱和氯水与石灰石的反应是制取较浓HClO溶液的方法之一。2005年的《化学教育》报道了如下实验研究:
实验一、定性研究:
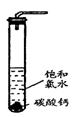 ①在试管中加入过量的块状碳酸钙,再加入约20mL饱和氯水,充分反应,有少量气泡产生,溶液浅黄绿色褪去;
①在试管中加入过量的块状碳酸钙,再加入约20mL饱和氯水,充分反应,有少量气泡产生,溶液浅黄绿色褪去;
②过滤,将滤液滴在有色布条上,发现其比氯水的漂白性更强;
③为了确定反应产物,将滤液分为三份,分别进行以下实验:
第一份与石灰水混合,立即产生大量白色沉淀;
第二份与稀盐酸混合,立即产生大量无色气体;
将第三份加热,看到溶液变浑浊且有大量无色气体产生。
经检测,上述实验中产生的无色气体均为CO2。
请回答:
(1)反应后所得的溶液漂白性增强的原因是______ ___________ ___
_ ________ 。
(2)依据上述实验可推知:②的滤液中的溶质除CaCl2、HClO外,还含有______ ___。
实验二、定量研究:
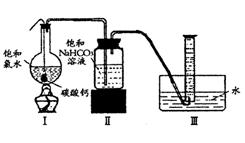 在圆底烧瓶底部,有一用塑料网包住的过量块状碳酸钙和150mL饱和氯水,按如图所示装置实验,待不再产生气泡后,将塑料网中剩余的石灰石提出液面,密封后再加热、煮沸烧瓶中的液体,直到量筒中的气体不再增加(不考虑HClO的分解)。
在圆底烧瓶底部,有一用塑料网包住的过量块状碳酸钙和150mL饱和氯水,按如图所示装置实验,待不再产生气泡后,将塑料网中剩余的石灰石提出液面,密封后再加热、煮沸烧瓶中的液体,直到量筒中的气体不再增加(不考虑HClO的分解)。
请回答:
(3)为减少用装置Ⅲ收集气体过程中CO2因溶解而造成的损失,且水槽中仍然为水,请你对装置Ⅲ进行改进,最简单的方法是 。
(4)用改进后的装置进行上述实验,测得塑料网内的碳酸钙质量减少Ag,总共收集到标准状况下的CO2气体BL,发现 ![]() 明显小于
明显小于 ![]() 。若不考虑实验操作和CO2的溶解等因素造成的误差,从化学反应原理来看,导致这一大小关系的原因是____________
。若不考虑实验操作和CO2的溶解等因素造成的误差,从化学反应原理来看,导致这一大小关系的原因是____________
。
(5)实验后发现,装置Ⅱ中的液体增多了,其原因是________ ________ 。
四、(本题包括1小题,共12分)
19.氧化铜是一种黑色固体,可溶于稀硫酸。某同学想知道是稀硫酸的哪种粒子(H2O,H ,SO42-)能使氧化铜溶解。请你和他一起通过如图Ⅰ、Ⅱ和Ⅲ三个实验完成这次探究活动。
|
CuO |
|
水 |
|
CuO |
|
稀硫酸 |
|
CuO |
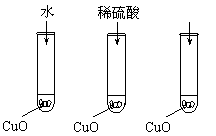 (1)某同学提出的假设是
(1)某同学提出的假设是
;
(2)通过实验Ⅰ可以证实
;
|
Ⅰ Ⅱ Ⅲ |
实验Ⅱ和Ⅲ,在Ⅱ中加入稀硫酸后氧化铜溶解,则
进一步所做的确认实验为:在Ⅲ中先加入 ,再加入 。
(4)探究结果为 。
你认为除实验Ⅱ和Ⅲ所用的试剂外,还能溶解氧化铜的一种常见物质是 。
五、(本题包括2小题,共20分)
20.(8分)短周期元素的单质X、Y、Z在通常状况下均为气态,并有下列转化关系(反应条件略去):
|
单质X |
|
单质Y |
|
单质Z |
|
共价化合物甲 |
|
共价化合物乙 |
|
离子化合物丙 |
 |
已知: a.常见双原子单质分子中,X分子含共价键最多。
b.甲分子中含10个电子,乙分子含有18个电子。
(1)X的电子式是 。
(2)磷在Z中燃烧可生成两种产物,其中一种产物丁分子中各原子最外层不全是8电子结构,丁的化学式是 。
(3)n mol丁与n mol丙在一定条件下反应,生成4n mol乙和另一化合物,该化合物蒸气的密度是相同状况下氢气的174倍,其化学式是 。
21.(12分) 物质之间的转化关系如下图所示,A可作为工业生产J的原料,B、C、H、I为非金属单质,X的水溶液为一种常见的无色医用消毒液,F为常见的红棕色防锈油漆颜料的主要成分,O是常见氮肥,且反应⑦中L与M的物质的量之比为1∶2,A、E、J、N中含有同一种元素。
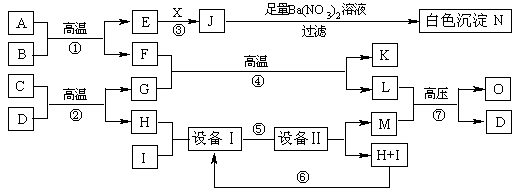
回答下列问题:
⑴X的化学式为_______________,C D的反应方程式为____ _______________
⑵考虑到综合经济效益,工业生产M时,可采取的措施有_______________(填序号)。
a.使用催化剂 b.适当降低温度 c.选择合适的温度 d.适度增大压强 e.及时分离出产物 f.对原料进行循环利用 g.充分利用反应本身放出的热量 h.工厂地址尽可能选择在交通发达的城市 i.工厂地址可选择在盛产天然气的地区
设备Ⅰ的名称_______________。工业生产中为了节约资源、降低成本和保护环境,经常对某些物质进行循环利用。上述转化关系中能达到该目的的是___________(填序号)。
⑶写出反应⑦的化学方程式________________________________________________。
⑷现有1molA参加反应,假设各步反应均完全,生成N的质量为1165g,生成K的质量为224g,则反应①的化学方程式为_________________________________________。
六、(本题包括1小题,共10分)
|
CO2体积 (mL) |
|
盐酸体积(mL) |
|
5 |
|
15 |
|
25 |
|
35 |
|
45 |
|
0 |
|
A |
|
B |
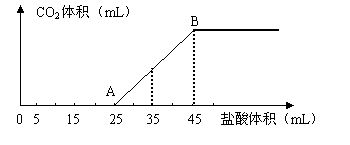 22.将2.5g碳酸钠、碳酸氢钠和氢氧化钠的固体混合物完全溶解于水,制成稀溶液,然后向该溶液中逐滴加入1mol·L-1的盐酸,所加入盐酸的体积与产生CO2的体积(标准状况)关系如下图所示:
22.将2.5g碳酸钠、碳酸氢钠和氢氧化钠的固体混合物完全溶解于水,制成稀溶液,然后向该溶液中逐滴加入1mol·L-1的盐酸,所加入盐酸的体积与产生CO2的体积(标准状况)关系如下图所示:
(1)写出OA段所发生反应的离子方程式______________________________________。
(2)当加入35mL盐酸时,产生CO2的体积为___________mL(标准状况)。
(3)计算原混合物中NaOH的质量及碳酸钠的质量分数。
七、(本题分A、B两题,考生只要选其中一题作答。若两题都作答,则以A题得分计入总分。本题共12分)
23A.(物质结构与性质,12分)有A、B、C、D四种元素,其中A元素和B元素的原子都有1个未成对电子,A 比B-少一个电子层,B原子得一个电子后3p轨道全满;C原子的p轨道中有3个未成对电子,其气态氢化物在水中的溶解度在同族元素所形成的氢化物中最大;D的最高化合价和最低化合价的代数和为4,其最高价氧化物中含D的质量分数为40%,且其核内质子数等于中子数。R是由A、D两元素形成的离子化合物,其中A与D离子数之比为2∶1。请回答下列问题:
(1)A单质、B单质、化合物R的熔点大小顺序为下列的 (填序号):
①A单质>B单质>R; ②R>A单质>B单质;
③B单质>R >A单质; ④A单质>R>B单质。
(2)在CB3分子中C元素原子的原子轨道发生的是________杂化,其固体时的晶体类型为 。
(3)写出D原子的核外电子排布式 _,C的氢化物比D的氢化物在水中溶解度大得多的可能原因 。
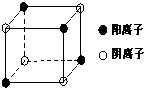 (4)右图是D和Fe形成的晶体FeD2最小单元“晶胞”,FeD2晶体中阴、阳离子数之比为 ,FeD2物质中具有的化学键类型为 。
(4)右图是D和Fe形成的晶体FeD2最小单元“晶胞”,FeD2晶体中阴、阳离子数之比为 ,FeD2物质中具有的化学键类型为 。
23B.(实验化学,12分)实验室需要制备纯净的氯化钾。现有含少量KBr和K2SO4的氯化钾样品,按照下图所示的实验方案进行提纯。
|
称取 样品 W g |
|
加水 溶解 |
|
沉淀甲 |
|
溶液 |
|
适量BaCl2溶液 操作 = 1 \* ROMAN I |
|
滤 液 |
|
过量氯气 操作 = 2 \* ROMAN II |
|
固体乙 |
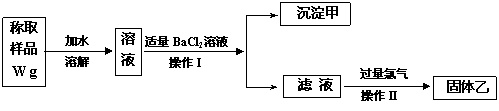
请回答下列问题:
(1)操作 = 1 \* ROMAN I的名称为 ,操作 = 2 \* ROMAN II所需要的玻璃仪器有 。
(2)若用硝酸钡来代替氯化钡,是否可行?请说明理由。
。
(3)若实验所得固体甲、乙的质量分别为W 1g和W 2g,则样品中KBr的质量分数计算式为 。
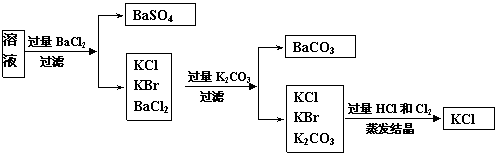
(4)某同学对该实验方案提出质疑,他认为加适量氯化钡溶液不轻易控制,应该加入过量氯化钡溶液,请你按照他的思路,用上述实验流程图表示出他后面的实验过程,要注明所用试剂和所得产物的化学式以及相应操作的名称。
|
溶液 |
|
过量BaCl2 过滤 |
参考答案
第Ⅰ卷(选择题,共48分)
一、单项选择题(本题包括8小题,每题3分,共24分。每题只是一个选项符合题意)
题号
1
2
3
4
5
6
7
8
答案
D
C
B
C
A
B
D
C
二、不定项选择题(本题包括8小题,每小题3分,共24分。每小题有一个或两个选项符合题意。)
题号
9
10
11
12
13
14
15
16
答案
B
C
CD
AD
B
B
AD
CD
第Ⅱ卷(非选择题,共72分)
三、(本题包括2小题,共18分)
17.(8分) (1)①用蒸馏水湿润(2分) ②检查是否漏水(2分)
(2)BDEH(4分)(错一个倒扣1分,至扣完为止)
18.(10分)
(1) CaCO3 消耗了氯水中的 HC1, 使 Cl2 H2O ![]() HCl HClO 平衡向右移动 , HClO 浓度增大(2分)
HCl HClO 平衡向右移动 , HClO 浓度增大(2分)
(2) Ca(HCO3)2( 写名称正确同样得分 ) (2分)
(3) 在导管末端再连接长导管 , 使导管的出口接近量筒底部(2分)
(4) 碳酸钙与氯水反应生成的Ca(HCO3)2再受热时,除生成CO2外,还生成了CaCO3(2分)
(5) 从圆底烧瓶蒸出的水蒸气在广口瓶中冷凝、聚集(2分)
四、(本题包括1小题,共12分)
19.(12分)
(1)H2O、H 、SO42-中的某一种粒子能够使CuO溶解(2分)
(2)水不能使氧化铜溶解,而是另外的H 、SO42-两种粒子中的一种粒子使CuO溶解(2分)
(3)Na2SO4(或K2SO4等)(2分), 稀硫酸(2分)
(4)氧化铜固体溶于稀H2SO4是稀硫酸H 在起作用,而H2O,SO42-两种粒子都不能使CuO溶解。(2分) 硝酸或盐酸等 (2分)
五、(本题包括2小题,共20分)
20.(8分)
(1) SHAPE \* MERGEFORMAT
|
N |
|
N |
(2)PCl5 (3分) (3)P3N3Cl6 (3分)
【提示】(4)根据题意可以写出如下表达式:nNH4Cl nPCl5→4nHCl A,根据原子守恒(质量守恒)A的分子式为 (PNCl2)n,而A的相对分子量为174×2=348,所以n= ![]() ,所以此化合物的化学式为(PNCl2)3,即为P3N3Cl6。
,所以此化合物的化学式为(PNCl2)3,即为P3N3Cl6。
21.(12分)
⑴ H2O2 (2分) C H2O ![]() CO H2 (2分)
CO H2 (2分)
⑵ acdefgi (2分) 合成塔 (1分) ⑥ (1分)
⑶CO2 2NH3 ![]() CO(NH2)2 H2O (2分) ⑷Fe4S5 8O2
CO(NH2)2 H2O (2分) ⑷Fe4S5 8O2 ![]() 2Fe2O3 5SO2(2分)
2Fe2O3 5SO2(2分)
六、(本题包括1小题,共10分)
22.(10分)
(1)H OH— = H2O, CO32— H = HCO3— (2分)
(2)224 (3分)
(3)设碳酸钠、碳酸氢钠和氢氧化钠的物质的量分别为x、y、z,则
![]() x y = 1mol/L×(0.045-0.025)L
x y = 1mol/L×(0.045-0.025)L
z - y = 1mol/L×[0.025-(0.045-0.025)]L
84g/mol·x 106g/mol·y 40g/mol·z = 2.5g
x=0.01mol,y=0.01mol,z=0.015mol
所以,NaOH的质量为0.6g,(2分)
Na2CO3的质量分数为 ![]() (3分)
(3分)
七、(本题分A、B两题,考生只要选其中一题作答。若两题都作答,则以A题得分计入总分。本题共12分)
23A.(物质结构与性质,12分)
(1)② (2分)
(2)SP3 (1分) 分子晶体 (1分)
(3)1S22S22P63S23P4 (2分) NH3与水分子形成氢键且更易发生化学反应 (2分)
(4)1:1 (2分) 离子键、非极性键 (2分)
23B.(实验化学,12分)
(1)过滤 (1分),玻璃棒、酒精灯 (3分)
(2)否,会引入硝酸钾杂质。 (2分)
(3) ![]() (2分)
(2分)
(4)(4分,要害是写出过量K2CO3一步的实验流程,否则不给分)
|
BaSO4 |
|
溶液 |
|
过量BaCl2 过滤 |
|
KCl KBr BaCl2 |
|
过量K2CO3 过滤 |
|
KCl |
|
BaCO3 |
|
KCl KBr K2CO3 |
|
过量HCl和Cl2 蒸发结晶 |
 |
