| 高考化学复习热点内容专题训练(十)-水的电离和溶液的pH值 | |||||||||||||
|
1.室温下,在pH=12的某溶液中,由水电离的[OH-]为 A.1.0×10-7mol/L B.1.0×10-6mol/L C.1.0×10-2mol/L D.1.0×10-12mol/L 2.pH=5的盐酸和pH=9的氢氧化钠溶液以体积比11∶9混合,混合液的pH为 4.25℃时,某强酸溶液pH=a,强碱溶液pH=b,且a+b=12,酸碱溶液混合后溶液的pH=7,则酸溶液的体积(V1)与碱溶液的体积(V1)的关系是 A.V1=102V2 B.V2=102V1 C. V1=2V2 D. V2=2V1
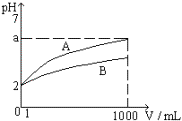
5.pH = 2的A、B两种酸溶液各1mL, 分别加水稀释到1000mL, 其溶液的pH与溶液体积(V)的关系如右图所示, 则下列说法正确的是 A.A、B两种酸溶液物质的量浓度一定相等 B.稀释后A酸溶液的酸性比B酸溶液强 C.a = 5时, A是强酸, B是弱酸 D.若A、B都是弱酸, 则5 > a > 2 6.取pH=4的某电解质溶液1.0L,用Pt电极进行电解,经过一段时间后,测得溶液pH=1,且阴、阳两极产物的物质的量之比为2:1,则该电解质溶液是 A.盐酸 B.氢氧化钾溶液 C.硝酸银溶液 D.硫酸铜溶液 7.在室温条件下,酸和碱的溶液等体积混合后,pH值一定大于7的是 A pH=3的盐酸和pH=11的氢氧化钡溶液 B pH=3的醋酸(电离度约为1%)和pH=12的氢氧化钠溶液 C pH=3的硝酸和pH=11的氨水(电离度约为1%) D pH=3的硫酸和pH=12的氢氧化钾溶液 8.t℃时饱和石灰水的密度为p(g·Cm-3),其pH=12,则t℃时氢氧化钙的溶解度为 A. C. 9.四种水溶液①HCI,②FeCI3,③KOH,④Na2CO3其 PH值依次为4、4、10、10,而溶液中水的电离度依次为α1、α2、α3、α4,则它们的关系正确的是 A.α1=α2=α3=α4 B.α1>α3>α2>α4 C.α4=α2>α3=α1 D.α1=α3>α2=α4 10.下面的各说法中正确的是 A.在1000C时,纯水中的pH=6,呈中性 B.pH=5的稀醋酸,再加水冲稀100倍,溶液的pH=7 C.0.3mol/L和0.1mol/L的两醋酸溶液中H+离子浓度之比为3 :1 D.在Na3PO4溶液中[Na+] :[PO43-]=3 :1 11.向一定体积的0.1摩/升的醋酸溶液中加入等体积的蒸馏水后,则下列叙述正确的是 A.溶液的pH值变小 B.醋酸的电离度增大 C.溶液的导电能力减弱 D.中和此溶液所需的0.1摩/升NaOH溶液的体积增加 12.将pH=3的盐酸溶液和pH=11的氨水等体积混和后,溶液中离子浓度关系正确的是 A.NH4+]>[Cl-]>[H+]>[OH-] B.[NH4+]>[Cl-]>[OH-]>[H+] C.[Cl-]>[NH4+]>[H+]>[OH-] D.[Cl-]>[NH4+]>[OH-]>[H+] 13.pH值为4的FeCl3溶液和pH值为10的K2CO3溶液中,水的电离度分别为α1和α2,则它们的大小关系是 A.α1>α2 B.α1<α2 C.α1=α2 D.无法判断 14.下列溶液,一定呈中性的是 A 由等体积、等物质的量浓度的一元酸跟氢氧化钠溶液混合后所形成的溶液 B [H+]=1×10-7mol·L-1 的溶液 C pH=14-pOH 的溶液 D pH=pOH 的溶液 15.若室温时pH=a的氨水与pH=b的盐酸等体积混合,恰好完全反应,则该氨水的电离度可表示为 A.10(a+b-12)% B.10(a+b-14)% C.10(12-a-b)% D.10(14-a-b)% 16.用水稀释0.1摩/升氨水时,溶液中随着水量的增加而减小的是 17.PH=13的强碱溶液与PH=2的强酸溶液混和,所得混和液的PH值=11,则强酸与强碱的体积比是 18.在pH值都等于9的NaOH和CH3COONa两种溶液中,设由水电离产生的OH- 离子浓度分别为A摩/升与B摩/升,则A和B关系为 A .A>B B .A=10-4 B C. B=10-4 A D. A=B 19.在下列叙述中,能说明盐酸是强酸,醋酸是弱酸的是 A.将pH=4的盐酸和醋酸稀释成pH=5的溶液,醋酸所需加入的水量多 B.盐酸和醋酸都可用相应的钠盐与浓酸酸反应制取 C .相同pH值的盐酸和醋酸溶液中分别加入相应的钠盐固体,醋酸的pH值变化大 D.相同pH值的盐酸和醋酸分别跟锌反应时,产生氢气的起始速度相等
A.X是正极,Y是负极 B.X是负极,Y是正极 C.硫酸铜溶液的PH值逐渐减小 D.硫酸铜溶液的PH值保持不变 21.某二元弱酸(简写为H2A)溶液,按下式发生一级和二级电离: H2A 22. 25℃时,若体积为Va、pH=a的某一元强酸与体积Vb、pH=b的某一元强碱混合,恰好中和,且已知Va<Vb和a=0.5b,请填写下列空白; (1)a值可否等于3(填“可”或“否”)_________,其理由是___________________ (2)a值可否等于5(填“可”或“否”)________,其理由是____________________ (3)a的取值范围是_______________________________________。 23.已知25℃时0.1mol·L-1醋酸溶液的pH约为3。向其中加入少量醋酸钠晶体, 待晶体溶解后发现溶液的pH增大。对上述现象有两种不同的解释: 甲同学认为醋酸钠水解呈碱性, 增大了[OH-], 因而溶液的pH增大; 乙同学认为醋酸钠溶于水电离出大量醋酸根离子, 抑制了醋酸的电离, 使[H+]减小, 因此溶液的pH增大。你认为上述两种解释中 (“甲”或“乙”)正确。 (1)为了验证上述哪种解释正确, 继续做如下实验: 向0.1mol·L-1的醋酸溶液中加入少量下列物质 (填写编号), 然后测定溶液的pH。 A.固体CH3COOK B.固体CH3COONH4 C.气体NH3 D.固体NaHCO3 (2)若 (填“甲”或“乙”)的解释正确, 溶液的pH应 (填“增大”、“减小”或“不变”)。(已知: 25℃时, 0.1mol·L-1氨水的电离度为1.3%, 0.1mol·L-1醋酸的电离度为1.3%) 4.酸雨主要是燃烧含硫燃料时释放出SO2所造成的。现取一份雨水样品,每隔一定的时间测定其pH值,测定结果见附表: 附表:雨水样品pH值随时间的变化值
试说明雨水样品pH值减小的原因 |
教育最重要的是使人变得更聪明。教育就是要开启人的心智,使人身体好,更主动、积极,行动能力强,更能干。
中文域名: 古今中外.com
英文域名: www.1-123.com
丰富实用的教育教学资料
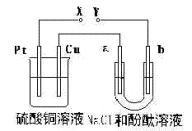 20.下图装置中,a、b都是惰性电极,通电一段时间后,b极附近溶液呈红色。下列说法正确的是
20.下图装置中,a、b都是惰性电极,通电一段时间后,b极附近溶液呈红色。下列说法正确的是