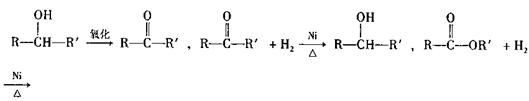化 学 试 题
本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分,共100分,考试时间90分钟。
第Ⅰ卷(选择题 共44分)
注重事项:
1.答第I卷前,考生务必将自己的姓名、准考证号、试题科目用2B铅笔涂写在答题卡上。
2.每小题选出答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑,如需改动,用橡皮擦干净后,再选涂其它答案,不能答在试题卷上。
3.考试结束,监考人将第II卷和答题卡一并收回,第I卷不收回。
相对原子质量:C:12 N:14 O:16 Na:23 Cl:35.5 K:39 Fe:56 Ag:108
第Ⅰ卷(选择题 共44分)
一、选择题(本题包括10小题,每小题2分,共20分,每小题只有一个选项符合题意。答案填入答题栏内)
1.下列说法正确的是 ( )
A.钢铁在海水中比在河水中更易腐蚀,主要原因是海水含氧量高于河水
B.废弃的塑料、金属、纸制品及玻璃等都是可回收再利用的资源
C.凡含有食品添加剂的食物对人体健康均有害,不宜食用
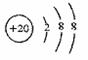
D.某些不合格大理石装潢材料中含有严重超过规定标准,对人体有害的放射性同位素氡 ![]() ,其原子中的质子数为136
,其原子中的质子数为136
2.在加入铝粉产生氢气的溶液中,下列各组离子可能大量共存的是 ( )
A.NH ![]() 、NO
、NO ![]() 、CO
、CO ![]() 、Na B.Ba2 、Mg2 、HCO
、Na B.Ba2 、Mg2 、HCO ![]() 、Na
、Na
C.H 、F一、K 、Cl- D.K 、AlO ![]() 、OH一、NO
、OH一、NO ![]()
|
|
|
|
|
C.碳-12原子: ![]() C D.Ar原子的结构示意图为:
C D.Ar原子的结构示意图为:
4.下列物质性质的变化规律,与共价键的强弱有关的是 ( )
A.F2、Cl2、Br2、I2的熔点、沸点逐渐升高
B.Li、Na、K、Rb、Cs的熔点、沸点逐渐降低
C.金刚石的硬度、熔点、沸点都高于晶体硅
D.KF、KCl、KBr、KI的熔点依次降低
5.下列说法正确的是 ( )
A.O3和O2互为同位素
B.HF、HCl、HBr、HI熔点、沸点依次升高
C.等质量的O3和O2含有相同的质子数
D.O3和O2的相互转化是物理变化
A.在萃取操作的演示实验中,将CCl4萃取溴水中的溴改为CCl4萃取碘水中的碘
B.在铜和浓硝酸反应的实验中,将铜片改为可调节高度的铜丝
C.将实验室的废酸液和废碱液中和后再排放
D.将实验室用KMnO4加热分解制氧气后的残余物倒入下水道
7.设NA为阿佛加德罗常数,下列叙述中不正确的是 ( )
A.18 g NH ![]() 中所含的电子数为10NA
中所含的电子数为10NA
B.0.1mol Fe与足量的I2充分反应,转移的电子数为0.2NA
C.标准状况下,1 L辛烷完全燃烧产生8L的CO2
D.28g C3H6与C2H4的混合物完全燃烧可生成88g CO2
8.下列反应的离子方程式书写正确的是 ( )
A.将Al条投入稀硝酸溶液中:2Al 6H ====2Al3 3H2↑
B.向碳酸氢钙溶液中加入少量的氢氧化钠溶液:
Ca2 2HCO ![]() 2OH
2OH ![]() ====CaCO3↓十CO
====CaCO3↓十CO ![]() 十2 H2O
十2 H2O
C.氨水与三氧化铁溶液反应:3OH ![]() Fe3 ====Fe(OH)3↓
Fe3 ====Fe(OH)3↓
D.向碳酸钠溶液中逐滴加入与之等体积等物质的量浓度的乙酸:
CO ![]() CH3COOH====CH3COO一 HCO
CH3COOH====CH3COO一 HCO ![]()
9.在l体积pH=12的Ba(OH)2溶液中,逐滴加入某H 2SO4溶液,当溶液中的Ba2 恰好完全沉淀时,H2SO4溶液恰为1体积。若反应后溶液的体积为两溶液体积之和,则反应后溶液pH为 ( )
A.1 B.7 C.8 D.0
|
A.某二元弱酸的酸式盐NaHA溶液中:
c(H )十c(Na )=c(OH—) c(HA—) c(A2—)
B.一定量的(NH4)2SO4与NH·H2O混合所得的碱性溶液中:c(NH ![]() )>2c(SO
)>2c(SO ![]() )
)
C.在物质的量浓度均为0.01mol/L的CH3COOH和CH3COONa的混合溶液中:
c(CH3COOH) c(CH3COO一)=0.01mol/L
D.相同温度下物质的量浓度相等的NH4HSO4溶液、NH4HCO3溶液、NH4Cl溶液中
c(NH ![]() ):c(NH4HSO4)>c(NH4HCO3)>c(NH4Cl)
):c(NH4HSO4)>c(NH4HCO3)>c(NH4Cl)
二、选择题(本题共8小题。每小题3分,共24分。每小题只有一个选项符合题意。)
![]() 11.反应2A(g) B(g) xC(g) 2D(s),在2升容器中一定条件下,1mol A与0.5molB反应达平衡时A为0.3mol/L,在1升容器中1mol A与0.5mol B在相同温度下反应达平衡时A为0.5mol/L,则x值最合适为 ( )
11.反应2A(g) B(g) xC(g) 2D(s),在2升容器中一定条件下,1mol A与0.5molB反应达平衡时A为0.3mol/L,在1升容器中1mol A与0.5mol B在相同温度下反应达平衡时A为0.5mol/L,则x值最合适为 ( )
A.2 B.1 C.大于2 D.小于3
|
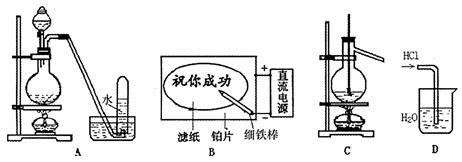
A.二氧化锰与浓盐酸反应制干燥氯气
B.滤纸先用氯化钠、无色酚酞的混合液浸湿,然后平铺在一块铂片上,接通电源后,用外加保护膜的细铁棒做笔在滤纸上写字显红色字迹。
C.石油的分馏
D.用水吸收氯化氢气体
13.把一定量的NaHCO3和Na2O2的混合物放在密闭容器中加热。关于混合物加热前后消耗盐酸的物质的量,下列结论判定正确的是 ( )
A.加热前消耗的多 B.加热后消耗的多
C.加热前加热后消耗的一样多 D.不知NaHCO3和Na2O2含量无法确定
14.下列叙述正确的是 ( )
A.95℃纯水的pH<7,说明加热可导致水呈酸性
B.pH=3的醋酸溶液,稀释至10倍后PH=4
C.氯化钙溶液中通二氧化碳气体可产生白色沉淀
D.水中加入某固体单质,经化学反应能够促进水的电离
15.下列说法不正确的是 ( )
A.电解精炼铜时,同一时间内阳极溶解铜的质量比阴极析出铜的质量小
B.蔗糖、硫酸钡和水分别属于非电解质、强电解质和弱电解质
C.天然气、沼气和水煤气分别属于化石能源、可再生能源和二级能源
D.Mg、Al、Cu可以分别用还原法(置换反应)、直接加热法和电解法冶炼得到
16.已知:(1)Zn(s) ![]() O2(g)====ZnO(s),△H=-348.3kJ/mol
O2(g)====ZnO(s),△H=-348.3kJ/mol
(2)2Ag(s) ![]() O2(g)====Ag2O(s),△H=-31.0kJ/mol
O2(g)====Ag2O(s),△H=-31.0kJ/mol
则Zn与Ag2O反应生成ZnO和Ag的热化学方程式为
A.Zn(s)十Ag2O(s)====ZnO(s) 2Ag(s),△H=317.3kJ/mol
B.Zn Ag2O=====ZnO 2Ag,△H=317.3kJ/mol
C.Zn(s) Ag2O(s)=====ZnO(s) 2Ag(s),△H=-317.3kJ/mol
D.2Zn(s) 2Ag2O(s)=====2ZnO(s) 4Ag(s),△H=-317.3kJ
17.向含铜粉的硝酸亚铁溶液中滴加足量稀硫酸,下列说法正确的是 ( )
A.能反应,但不产生气体 B.铜粉完全溶解
C.实验过程中溶液会变色 D.铜粉不会溶解
18.2,2,4—四甲基戊烷与氯气发生取代反应时,生成的一氯代物可能有 ( )
A.2种 B.3种 C.4种 D.5种
|
三、填空题(本题共3小题,19题13分,20题11分,21题11分,共35分)
19.(13分)有A、B、C、D、E五种短周期元素,其元素特征信息如下表
元素编号
元素特征信息
A
其单质是密度最小的物质。
B
阴离子带两个单位负电荷,单质是空气的主要成分之一。
C
其阳离子与B的阴离子有相同的电子层结构,且与B可以形成两种离子化合物。
D
其氢氧化物和氧化物都有两性,与C同周期
E
与C同周期,原子半径在该周期最小
回答下列问题:
(1)写出下列元素的名称:C ,E
(2)写出A、B、C形成的化合物的电子式
(3)B、C、D的简单离子半径由大到小的顺序是(用化学式表示)
(4)①写出E单质与A、B、C形成的化合物反应的化学方程式:
②D单质与A、B、C形成的化合物的水溶液反应的离子方程式:
③B、C元素形成的化合物与A2B反应的二个化学方程式:
|
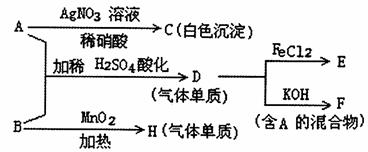
请回答:
(1)写出A、B的化学式 、 。
(2)写出D与FeCl2溶液反应的化学方程式 。
(3)写出A、B反应生成D的离子方程式 。
(4)H的一种同素异形体的化学式为 。
|
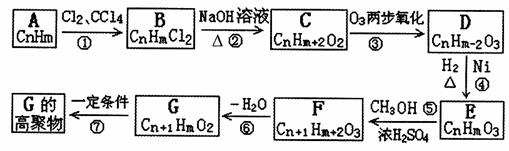
|
在上述转化中,已知:C的分子式为C3H8O2,2个E分子间可脱去水分予缩合生成六元环状化合物C6H8O4,试填写下列空白:
(1)写出链烃A的名称
(2)在反应①-⑦中属于取代反应的是
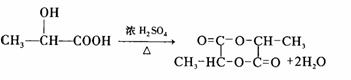
(3)写出2分子E脱去水分子缩合生成六元环C6H8O4化合物的化学方程式
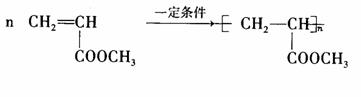
(4)写出反应⑦的化学方程式:
四、实验题(本题13分)
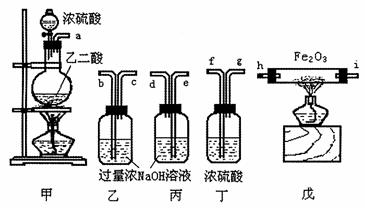
|
![]() CO2↑ CO↑ H2O来制取,与Fe2O3反应的CO需纯净、干燥。
CO2↑ CO↑ H2O来制取,与Fe2O3反应的CO需纯净、干燥。
|
(1)若所制气体从左向右流向时,上述仪器组装连接的顺序是(用a,b……表示)
a接b,c接 , 接 , 接 ;
(2)装置丙的作用是
(3)怎样除去尾气中的CO气体
(4)实验前氧化铁矿粉末为x g,经充分反应实验后测得乙、丙质量分别增加y g和z g,则该矿石中氧化铁的质量分数为 。
五、计算题(本题8分)
23.(8分)等物质的量的NaHCO3和KHCO3的混合物4.60g,与l.00mol/L的盐酸反应:
(1)试分析,欲求标准状况下生成的CO2气体的体积时,还需要什么数据 (用a表示,并注明单位)
(2)利用所确定的数据,求标准状况下CO2气体的体积(填写下表):
所需数据取值范围
生成CO2气体的体积
盐酸不足量时
盐酸足量时
(3)若NaHCO3和KHCO3的物质的量不相等,则4.60g的混合物与足量盐酸完全反应时,在标准状况下生成的CO2气体的体积大于 L,小于 L.
参考答案
一、二选择题(l-10每小题2分,1l-18每题3分,共44分)
1.B 2.D 3.D 4.C 5.C 6.D 7.C 8.D 9.B 10.B 11.D 12.B 13.C
14.D 15.D 16.C 17.C 18.A
|
19.(共13分)
|
|
(3)r(O2—)>r(Na )>r(Al3 )(2分)
(4)①Cl2 2NaOH====NaCl NaClO H2O(2分)
②2 Al 2OH— 2H2O====2AlO ![]() 3H2↑(2分)
3H2↑(2分)
③2Na2O2 2H2O====4 NaOH O2↑(2分) Na2O H2O====2NaOH(1分)
20.(共11分)
(1)KCl,KClO3(4分)
(2)2FeCl2 Cl2====2FeCl3(2分)
(3)5Cl一 ClO ![]() 6H ====3Cl2↑ 3H2O(3分)
6H ====3Cl2↑ 3H2O(3分)
(4)O3(2分)
21.(共11分)(1)丙烯(3分)(2)②⑤(2分)
|
(3)(3分)2
|
(4)(3分)
四、实验题(共13分)
22.(1)接f,g接h,i接e,(h与i顺序可颠倒)(4分)
(2)吸收CO2,以便于用燃烧法除去尾气CO(2分)(答案合理给分)
(3)将点燃的酒精灯放在d处。(3分)
(4) ![]() ×100%(4分)
×100%(4分)
五、计算题(8分)
23.(1)盐酸的体积a L(2分)
(2)当a<0.0500L时;22.4a L。 a≥0.0500L时:1.12 L。(4分)
(3)1.03,l.23(2分)