| ��������: �Ž�����.com������������
Ӣ��������www.1-123.com�����������ḻʵ�õĽ�����ѧ���� |
| |
| |
| |
|
|
�ġ����������2С�⣬��22�֣� 24. ��12�֣�1943���ҹ������Ļ���ר�Һ�°�ʿ�����������Ƽ��������Ϊ�����Ƽ����°��Ƽԭ��������ά��������ͬ����֮ͬ����������̼�����ƺ��ĸҺ�м�������ʳ�Σ�ͨ�백����ʹ�Ȼ���������Ӷ��õ����������ʣ�̼���ɺ��Ȼ�泥������Ƽ����ȫ���磬Ϊ�й���Ӯ�������������ء������Ƽ��ѭ�������������£�
��ϸ�Ķ���ͼ������������⣺ (1) д��̼����Ӧ����ʽ�� ��
(3) �����з���������ʵ��������ʳ��ˮ�� ͨ������B��װ��ͼ�� (4) ������������� ��������� ������ �����в���������Ҫ�IJ����� ���ǣ��������ձ��� ����ʵ������� ���������õ���Ҫ������ �� (5) ����������������ѭ��ʹ�õ������ǣ�C��B��F�� �� ��������ʱ�ţ� 25. (10��)��������͵����������dz��õĻ���ԭ�ϣ���Ҳ�Ǵ�������Ҫ��Ⱦ��ۺ���������Ⱦ�ǻ�����ѧ��ǰ����Ҫ�о�����֮һ��
�ٽ�2.0 mol SO2��1.0 mol O2����10 L�ܱ������У���Ӧ��ƽ�����ϵ��ѹǿΪ0.10 MPa���÷�Ӧ��ƽ�ⳣ������____________�� ��ƽ��״̬��A�䵽Bʱ��ƽ�ⳣ��K(A)_______K(B)(���������������=��)�� (2)��CH4����ԭNOx�������������������Ⱦ�����磺 CH4(g)��4NO2(g) = 4NO(g)��CO2(g)��2H2O(g)��DH =��574 kJ/mol CH4(g)��4NO(g) = 2N2(g)��CO2(g)��2H2O(g)��DH =��1160 kJ/mol ���ñ�״����4.48 L CH4��ԭNO2��N2������������ת�Ƶĵ�������Ϊ_____________(�����ӵ�������ֵ��NA��ʾ)���ų�������Ϊ_________kJ�� (3)�������ײ�����ȱλ������(MFe2Ox��3��x��4��M = Mn��Co��Zn��Ni)��������(MFe2O4)�����»�ԭ���ã������£�����ʹ��ҵ�����е�����������ֽ��ȥ��ת��������ͼ��ʾ��
��д��MFe2Ox�ֽ�SO2�Ļ�ѧ����ʽ______________________________________(������ƽ)�� 26. ��10�֣����ᣨH3PO4������Һ���ܹ���H3PO4��H2PO4����HPO42������PO43������������ʽ���ڣ�����Һ��pH�����仯ʱ��������һ�����ӵ����ʵ���ռ�������������ʵ����ķ�����Ҳ���ܷ����仯����ͼ��H3PO4��Һ�У��������ӵ����ʵ�����������pH�ı仯���ߣ�
��1����������Ũ��Ϊc���ܣ���д��c���ܣ��������Ũ�ȼ�Ĺ�ϵʽ �� ��2����Na3PO4��Һ����ε���ϡ��������pH��9����6�Ĺ����з�������Ҫ��Ӧ�����ӷ���ʽΪ ����pH=7ʱ����Һ����Ҫ���ڵ������ӣ�OH�����ӳ��⣩�� �� ��3����ͼ���ƶ�NaH2PO4��Һ�� �ԣ���ᡱ����������С�������ԭ���� �� ��4����Na3PO4��Һ�У�c��Na ��/ c��PO43���� 3���>������==������<�����������Һ�е��뼸��ŨKOH��Һ��c��Na ��/ c��PO43������ֵ��С��ԭ���� �� �塢���������1С�⣬��10�֣� 27.�����ᣨ��ʽ�е�A����ij�ֿ��������ɷ�֮һ��A��FeCl3��Һ��Ӧ����ɫ��

��1���������к��������ŵ�����Ϊ �� ��2����������Է����ķ�Ӧ�� ����д��ţ��� ��������Ӧ �ڼӳɷ�Ӧ ��������Ӧ �ܼӾ۷�Ӧ ����ȥ��Ӧ ��3��������ɿ���1��3��4һ��ȡ����������������ͬ�Ĺ�����λ����λ��ȡ �����в���֧��������Ľṹ��ʽΪ �� ��4��3.6g������������̼�����Ʒ�Ӧ�������壨��״���� mL�� ��5���佺����Ҫ���Գɷ�ΪCPAE������ʽΪC12H16O4����������һ�������� ��ˮ�����ɿ������һ�ִ����ô�Ϊ���㴼���ҷ��ӽṹ�������ȸ��÷��㴼��һ�������·�Ӧ����CPAE�Ļ�ѧ����ʽΪ �� ����ѡ���⣨�������2С�⣬ÿС��10�֣�����ֻ��ѡ��һ�⡣28С��Ϊ���л���ѧ���������ݵ����⣬29��Ϊ�����ʽṹ�����ʡ����ݵ����⣩ ����ע�أ� 28��29��Ϊѡ���⣬��������ѡһ�⡣���ڴ��ָ��λ����д����ѡ�������ţ��ٰ�Ҫ����⣬���粻������ţ�һ�ɰ�0�ּơ�28���ʺ�ѡ�ޡ��л���ѧ������ģ��Ŀ������29���ʺ�ѡ�ޡ����ʽṹ�����ʡ�ģ��Ŀ������ 28.��ϸ��������л��ϳɹ�����̼�ǼܵĹ����������ŵ������ת����������⣺ ���ȩF������ʽΪC9H8O������Ȼ������ڹ����У���һ�ֳ��õ�ֲ���ζ�ͣ���ҵ����Ҫ�ǰ�����·�ߺϳɵģ�
��֪����Ӧ = 5 \* GB3 ��Ϊ��ȩ���Ϸ�Ӧ����ش� ��1�����ȩF�Ľṹ��ʽΪ�� ��E�к��������ŵ�����Ϊ �� ��2����Ӧ = 1 \* GB3 �١� = 6 \* GB3 ���з���ԭ�Ӿ����Ե��� �� ��3��д������ת���Ļ�ѧ����ʽ�� = 2 \* GB3 �� �� = 3 \* GB3 �� �� д���йط�Ӧ�����ͣ� = 2 \* GB3 �� = 6 \* GB3 �� �� ��4����������Ҫ���E���ʵ�ͬ���칹���� �֣�������������ȡ������������һ�����ڶ�λ���������ࣩ�� 29��X��Y��Z��WΪ��ԭ��������С�������е����ֶ�����Ԫ�أ���֪�� ��XԪ��ԭ�Ӽ۵����Ų�ʽΪns2np2����ԭ�Ӱ뾶��ͬ��Ԫ������С�ġ� ��YԪ���ǵؿ��к�������Ԫ�أ�WԪ�صĵ縺����С��YԪ�أ���Wԭ�ӵĵ����Ų��У�p�����ֻ��1��δ�ɶԵ��ӡ� ��ZԪ�صĵ��������ݼ��±���kJ��mol��1����
| I1
| I2
| I3
| I4
| ��
| 496
| 4562
| 6912
| 9540
| �� |
��4��ZW����Ľṹʾ��ͼ���¡���֪����(ZW)=2.2 g��cm��3��NA=6.02��1023 mol��1 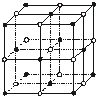 ����ZW���������������Z�������ļ�ľ���Ϊ
����ZW���������������Z�������ļ�ľ���Ϊ
���
|
��� |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
|
�� |
||||||||||
|
��� |
11 |
12 |
13 |
14 |
15 |
16 |
17 |
18 |
19 |
20 |
|
�� |
�������������2С�⣬��29�֣�
21����ÿ��2�֣���10�֣�
��1��û�г������� �����õĻ�ɫ�����еμ�ŨKI��Һ����ɫ�����ܽ�
��2������������Һ��HNO3��I-������ʹI-Ũ�ȼ�С��ƽ��AgI I- ![]() [AgI2]�������ƶ�
[AgI2]�������ƶ�
��3��AgI��AgCl���ܽ�� �ڻ�ɫ��AgI�����еμ�NaCl��Һ������δת��Ϊ��ɫ
22. (8��) ��100mL����ƿ����ͷ�ιܣ�����1�֣��ƻ���̿�����ˣ�����1�֣�
����Һ��ɫ�����ʵ���Ũ�ȳ����ȣ�2�֣�
��2CH3CHOHCOOH Fe �� ��CH3CHOHCOO��2Fe H2 ��2�֣�
23. (11��) ( l ) ��Һ©��(1��) B(1��)
��2������Һ����Ӧ���Ũ�Ȳ�ͬ����Ӧ�¶Ȳ�ͬ(1��) M(1��) ����(1��)
��3��Cl2 2OH����ClO�� Clһ��H2O (2��)
��4��
��(1��)
������ˮ��Ӧ���ɵ�HClO��ʯ������Ϊ��ɫ����(1��)
����(1��)
����ͨ�����������ˮʹ��Һ�ʻ���ɫ(1��)
�ġ����������2С�⣬��31�֣�
24. ��11�֣���1��NaC1 H2O NH3 CO2��NaHCO3�� NH4C1��1�֣���2��NH3��1�֣���B��C��1�֣�����ͨ����ʹ��Һ������ǿ�����ܽ����Ķ�����̼�����ɽ϶��̼�����ƣ�ʹ̼�����ƾ�����������2�֣�
��3��  ��1�֣���4�����ˣ�1�֣���©����1�֣���������1�֣���5��A��D��2�֣�
��1�֣���4�����ˣ�1�֣���©����1�֣���������1�֣���5��A��D��2�֣�
25. ��10�֣�
(1)��800 L��mol��1��3�֣�δ����λ��1�֣����� =��1�֣���
(2)1.60NA(��1.6NA) ��2�֣���173.4��2�֣���
(3)MFe2Ox��SO2 ![]() MFe2O4��S����2�֣�
MFe2O4��S����2�֣�
26����10�֣�
��1��c���ܣ�== c��H3PO4�� c��H2PO4���� c��HPO42���� c��PO43������2�֣�
��2��HPO42�� H == H2PO4����1�֣� H2PO4����1�֣���HPO42����1�֣�
��3���ᣨ1�֣�H2PO4������Һ�еĵ���̶ȴ���ˮ��̶ȡ���2�֣�
��4��>��1�֣���KOH������PO43����ˮ�⣨1�֣�
27. ��1��
�Ȼ���1�֣����ǻ���1�֣� ��2���٢ڢۢܣ�1�֣�
|
��3�� ��1�֣� ��4��448��2�֣�
��5��
|
|
һ������ |
28.�𰸣���1�� ![]() ��CH��CHCHO �ǻ���ȩ��
��CH��CHCHO �ǻ���ȩ��
��2�� = 1 \* GB3 �� = 5 \* GB3 ��
��3��2C2H5OH O2 ![]() 2CH3CHO 2H2O
2CH3CHO 2H2O
![]() ��CH2Cl��H2O
��CH2Cl��H2O ![]()
![]() ��CH2OH��HCl ������Ӧ����ȥ��Ӧ
��CH2OH��HCl ������Ӧ����ȥ��Ӧ
��4��3
��3�����ʯ NaClΪ���Ӿ����CCl4Ϊ���Ӿ��壨4��4.0��10-8 cm
| |