1.本卷总分120分,考试时间100分钟。
2.可能使用的相对原子质量:H-1 O-16 Na-23 Mg-24 Al-27 S-32 Fe-56
第Ⅰ卷(选择题,共56分)
一、单项选择题(本题包括8小题,每小题3分,共24分。每小题只有一个选项符合题意)
1.化学与生活是紧密相联的,下列关于生活化学的说法正确的是
A.随着人们生活节奏的加快,方便的小包装食品已被广泛接受,为了防止中秋月饼等富脂食品氧化变质,延长食品的保质期,在包装袋中常放入生石灰
B.现在用的清洁燃料主要有两类:一类是压缩天然气,另一类为液化石油气,它们属于碳氢化合物
C.福尔马林是一种良好的杀毒剂,也可用来消毒自来水
D.保护加酶洗衣粉的洗涤效果,应用沸水溶解洗衣粉
2.目前人类已发现的非金属元素除稀有气体外,共有16种。下列对这16种非金属元素的相关判定:①都是主族元素,最外层电子数都大于4;②单质在反应中都只能作氧化剂;③氢化物常温下都是气态,所以又都叫气态氢化物;④氧化物常温下都可以与水反应生成酸( )
A.只有②③正确 B.只有①③正确
C.只有④正确 D.①②③④均不正确
3.元素的性质包含金属性和非金属性,其强弱可以通过该元素对应的某些化学性质体现出 来。某同学认为铝元素是金属元素,但是有一定的非金属性。下列化学反应中,你认为能支持该同学观点的是( )
A.铝片与盐酸反应生成氢气 B.氢氧化铝溶于强碱溶液
C.氢氧化铝溶于强酸溶液 D.铝热反应
4.吸进人体内的O2有2%转化为氧化性极强的活性氧副产物,如 ![]() \* MERGEFORMAT 等,这些活性氧能加速人体衰老,被称为“夺命杀手”。我国科学家尝试用含硒化合物Na2SeO3消除人体内的活性氧,在消除活性氧时,Na2SeO3的作用是( )
\* MERGEFORMAT 等,这些活性氧能加速人体衰老,被称为“夺命杀手”。我国科学家尝试用含硒化合物Na2SeO3消除人体内的活性氧,在消除活性氧时,Na2SeO3的作用是( )
A.氧化剂 B.还原剂
C.既是氧化剂又是还原剂 D.以上均不是
5.生产、生活离不开各种化学物质,下列说法不正确的是 ( )
A.不需要通过化学反应就能从海水中获得食盐和淡水
B.潜水艇在紧急情况下可用过氧化钠供氧
C.氯气与烧碱溶液或石灰乳反应都能得到含氯消毒剂
D.工业上常用硅制造光导纤维;用铝粉还原一些金属氧化物来制金属
6.NA表示阿伏加德罗常数。下列说法中正确的是( )
A.23 g Na和足量的O2完全反应,无论是常温,还是燃烧,都失去NA个电子
B.203gMgCl2·6H2O晶体中含有的Mg2 离子不足NA个
C.200mL1mol/LAl2(SO4)3溶液中,Al3 和SO42-离子数的总和是NA
D.Na2O2与H2O反应生成11.2L O2(标准状况),反应中转移的电子数为2NA
7.下列4组连线中,完全正确的一组是( )
A.  B.
B. 
C.  D.
D. 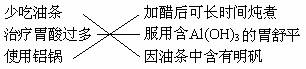
8.氧化还原反应广泛应用于金属的冶炼。下列说法不正确的是 ( )
A.冶炼铁的主要原料有铁矿石、焦炭、空气、石灰石等,其中石灰石的作用是除去铁矿石中的脉石(二氧化硅)的。
B.湿法炼铜与火法炼铜的反应中,铜元素都发生还原反应
C.用磁铁矿炼铁的反应中,1mol Fe3O4被CO还原成Fe,转移9mole—
D.铝热法还原铁的反应中,放出的热量能使铁熔化
二、不定项选择题(本题包括8小题,每小题4分,共32分。每小题有一个或两个选项符合题意。若正确答案只包括一个选项,多选时,该题为0分;若正确答案包括两个选项,只选一个且正确的得2分,选两个且都正确的得满分,但只要选错一个该小题就为0分)
|
浓硫酸 |
|
亚硫酸 |
|
钠晶体 |
|
湿润蓝色石蕊试纸 |
|
湿润淀粉KI试纸 |
|
湿润品红试纸 |
|
沾有KMnO4溶液的滤纸 |
|
NaOH |
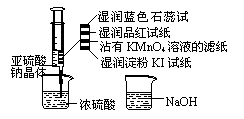 9.如图,在注射器中加入少量Na2SO3晶体,并吸入少量浓硫酸(以不接触纸条为准)。则下列有关说法正确的是
9.如图,在注射器中加入少量Na2SO3晶体,并吸入少量浓硫酸(以不接触纸条为准)。则下列有关说法正确的是
A.蓝色石蕊试纸先变红后褪色
B.品红试纸、沾有KMnO4溶液滤纸均褪色证实了SO2漂白性
C.湿润淀粉KI试纸未变蓝说明SO2的氧化性弱于I2
D.NaOH溶液可用于除去实验中多余的SO2
10.下列有关实验的叙述中,不正确的有
①蒸干AlCl3溶液可得纯净的无水氯化铝;②试管里加入少量淀粉,再加入一定量稀硫酸,加热3~4分钟,然后加入银氨溶液,片刻后管壁上有“银镜”出现;③无法用分液漏斗将甘油和水的混合液体分离;④用酸式滴定管量取20.00mL高锰酸钾酸性溶液;⑤为了测定某溶液的pH,将未经湿润的pH试纸浸入到待测溶液,过一会取出,与标准比色卡进行对比;⑥苯与溴水在铁粉的催化作用下制备溴苯;⑦配制银氨溶液时,将稀氨水慢慢滴加到硝酸银溶液中,产生沉淀后继续滴加到沉淀刚好溶解为止;⑧在苯酚溶液中滴入少量稀溴水溶液中立即出现白色沉淀。
A.4句 B.5句 C.6句 D.7句
11.下列各组离子,在指定的环境中一定能大量共存的是( )
A.滴加石蕊试液显红色的溶液:Fe3+、NH4+、C1-、SCN-
B.含有大量HCO3-的溶液:NH4 、Ca2 、Mg2+、I-
C.在加入铝粉能产生H2的溶液中:NH4 、Fe2 、SO42-、NO3-
D.含有大量ClO-的溶液:H 、Mg2 、I-、SO42-
12.科技日报2007年1月30日讯 美、德两国科学家日前成功合成出具有独特化学特性的氢铝化合物(AlH3)n,其结构类似由硼和氢组成的硼烷,有关研究报告发表在最新出版的美国《科学》杂志上。最简单的氢铝化合物为Al2H6,它的熔点为150℃,燃烧热极高。Al2H6球棍模型如右图。下列有关说法肯定不正确的是
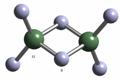 A.Al2H6中H为 1价,Al为-3价
A.Al2H6中H为 1价,Al为-3价
B.Al2H6在空气中完全燃烧,产物为氧化铝和水
C.Al2H6分子是非极性分子
D.氢铝化合物可能成为是未来的储氢材料和火箭燃料
13.能正确表示下列反应离子方程式的是( )
A.过氧化钠固体与水反应:2O22— 2H2O == 4OH- O2↑
B.FeSO4酸性溶液暴露在空气中:4Fe2++O2+4H+=4Fe3++2H2O
C.次氯酸钙溶液中通入少量SO2:Ca2 2 ClO- H2O SO2 == CaSO3↓ 2HClO
D.向明矾[KAl(SO4)2]溶液中逐滴加入Ba(OH)2溶液至SO42-恰好沉淀完全:
2Al3++3SO42-+3Ba2++6OH-=2Al(OH)3↓+3BaSO4↓
14.Br2与水可发生反应:Br2 H2O ![]() HBr HBrO,HBrO与HClO一样具有强氧化性,柠檬醛的结构简式为:(CH3)2C=CHCH2CH2CH=CHCHO,为了检验其中含有C=C键,下列设计中可以达到目的的是( )
HBr HBrO,HBrO与HClO一样具有强氧化性,柠檬醛的结构简式为:(CH3)2C=CHCH2CH2CH=CHCHO,为了检验其中含有C=C键,下列设计中可以达到目的的是( )
A.将柠檬醛加入盛有溴水的试管中
B.将柠檬醛加入盛有紫色酸性KMnO4溶液的试管中
C.将柠檬醛中加入盛有溴的CCl4溶液的试管中
D.向柠檬醛中加过量新制的Cu(OH)2,加热,过滤,再向滤液中加酸性KMnO4溶液
15.将氨水滴加到盛有AgC1的试管中,AgC1逐渐溶解,对上述过程,下列叙述或解释中正确的有
A.所得溶液中c(Ag )×c(C1-)<KSP(AgC1)
B.所得溶液中形成了难电离的物质
C.上述实验说明C1—与NH4 间有很强的结合力
D.上述过程中NH3·H2O的电离程度增大
16.把一定量的Na2O2和NaHCO3混合粉末分为两等份,将其中一份加入到100mL稀盐酸中恰好完全反应,生成干燥的气体2.24L(标准状况),再将此气体通入到另一份混合物中,充分反应后,气体减少为2.016L(标准状况),则原混合粉末中Na2O2和NaHCO3的物质的量之比及原稀盐酸的物质的量浓度可能是( )
|
A |
B |
C |
D | |
|
Na2O2和NaHCO3的 物质的量之比 |
8﹕1 |
9﹕2 |
1﹕8 |
2﹕9 |
|
原稀盐酸的 物质的量浓度(mol/L) |
3.4 |
1.1 |
1.8 |
1.3 |
第Ⅱ卷(非选择题,共64分)
三、(本题包括2小题,共18分)
17.(8分)在足量的稀氯化亚铁溶液中加入1~2滴液溴,振荡后溶液变为黄色。
(1) 甲同学认为是Br2溶于水变成黄色溶液 ; 乙认为是Fe2 被氧化成Fe3 使溶液变成黄色。
(2)现提供试剂: A.酸性高锰酸钾溶液 B.氢氧化钠溶液
C.四氯化碳 D.硫氰化钾溶液
请判定 (填“甲”或“乙”)的推断正确,并用两种方法加以验证,写出选用的试剂编号及实验中观察到的现象:
选用试剂
实验现象
第一种方法
第二种方法
(3)若选用淀粉碘化钾溶液判定哪位同学的推断正确,是否可行?(填“可行”或“不可行”): 理由: ;
18.(10分)某研究性学习小组为探究铜、锌与浓盐酸反应,设计实验探究方案如下:
(一) 实验用品:纯锌片、铜片、37%的浓盐酸、蒸馏水、氯化铜溶液
(二) 实验记录:
交流卡片
主题:Zn、Cu与浓盐酸间的实验
A.将锌放入浓盐酸的实验
B.将锌与铜片贴在一起,一同放入浓盐酸中,反应快速放出气体
C.当实验B中锌片完全溶解后,将溶液加热,又产生大量气体,得到无色溶液
D.将实验C反应后的溶液隔绝空气,加入适量水,出现白色沉淀
(三)背景资料
资料卡片
主题:生成一价铜的反应
![]() ① 必修一,P116:4CuO === 2Cu2O O2↑
① 必修一,P116:4CuO === 2Cu2O O2↑
②《无机化学》下册,p705:2Cu2 4I- == 2CuI(白色)↓ I2
③《无机化学》下册,p706:氯化亚铜(CuCl)在不同浓度的KCl溶液中可形成[CuCl4]3 等无色离子。
(四)请你参与以下探究
(1)实验A反应速度明显比B小,原因是 。
(2)根据“铜位于金属活动顺序表氢之后,与稀盐酸不反应,而在实验C中加热时又产生气体”的事实,作出如下推断:
①有同学认为“实验C中加热时产生的气体是溶解在溶液中的H2”,你认为是否有道理,理由是 。
②某同学作了如下猜想:是否成立?请你设计实验方案加以验证。
猜想
验证方法
猜测现象及结论
认为铜片中可能含有锌等杂质
(3)某同学对实验D中的白色沉淀进行分析:“不可能是CuCl2,因为CuCl2能溶于水且溶液显蓝色;也不可能是ZnCl2,因为稀释后溶液更稀,不会析出ZnCl2晶体。若利用资料卡片资料①②大胆猜想,白色沉淀可能是CuCl。请你帮他设计验证方案。
猜想
预设验证方法
猜想的现象与结论
白色沉淀
是氯化亚铜
(4)指导老师肯定了实验D中的白色沉淀是CuCl;并指出生成沉淀的原因,实际上是[CuCl4]3-等离子与CuCl(s)、Cl-三者之间所形成的沉淀溶解平衡移动的结果。请写出这一平衡关系式(用离子方程式表示) 。
四、(本题包括2小题,共21分)
19.(10分)氧族元素的各种性质可归纳整理出如下(部分):
元素
性质
8O
16S
Se
52Te
单质沸点(℃)
-183
444.6
685
1390
主要化合价
-2
-2, 4, 6
-2, 4, 6
原子半径(nm)
0.074
0.102
0.116
0.143
单质与H2反应
点热易化合
加热化合
加热难化合
不能直接化合
回答下列问题:
|
(2)H2O2可以作脱氯剂,用于消除水中的Cl2,写出该反应的化学方程式:
。
 (3)碲的主要化合价可能有 。
(3)碲的主要化合价可能有 。
(4)工业上可用Al2Te3制备H2Te,化学方程式为:
。
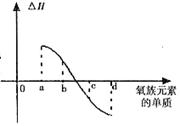
(5)右图所示为上述氧族元素单质与H2反应过程中的能量变化示意图,其中a、b、c、d分别表示氧族中某一元素的单质,△H为相同物质的量的单质与H2反应过程中的能量变化(反应的热效应)。则:b代表 ,d代表 (写化学式)。
20.(11分)镉是银白色或有蓝色光泽的软质金属,具延展性,密度:8.642克/厘米3。熔点:320.9℃。沸点765℃。常见化合价为 2价。不溶于水,溶于大多数酸中。在元素周期表中,锌(30Zn)、镉(48Cd)、汞(80Hg)同属于锌族,锌和汞在自然界中常共生,镉的金属活动性介于锌和汞之间。湿法炼锌过程中产生的铜镉渣中含有Cu、Cd、Zn等多种金属,可用于生产金属镉。镉的主要用途可以用作镍—镉电池,以及用于颜料生产,镉化合物还在PVC稳定剂、发光材料、半导体材料、杀菌剂等方面有广泛的应用。镉的生产流程如图示意如下:

请回答下列问题:
(1)写出步骤①反应的离子方程式 。
(2)步骤②所加入的金属的名称是 ,为了实现绿色化学的目标,应如何处理“溶液1”? 。
(3)步骤④用“溶液2”作电解液,镉在 极析出,该电极反应式是
(4)“电解废液”中含有镉,不能直接作为污水排放。目前含镉的废水处理的方式有两种,一种是在含镉污水中加入硫化钠沉淀镉离子,另一种是加入聚合硫酸铁和聚合氯化铝沉淀镉离子。写出加入硫化钠溶液沉淀镉离子的离子方程式 。
五、(本题包括1小题,共9分)
21.(9分)茶是我国人民喜爱的饮品。某校化学爱好小组的同学设计以下实验来定性检验茶叶中含有Ca、A1、Fe三种元素。
【查阅部分资料:草酸铵[(NH4)2C2O4]属于弱电解质;Ca、A1、Fe完全沉淀的pH:Ca(OH)2:pH≥13;A1(OH)3;pH≥5.5;Fe(OH)3:pH≥4.1)
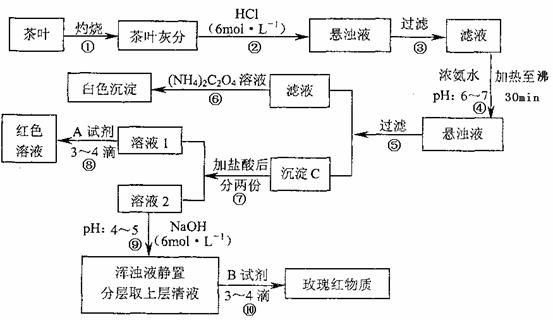
试根据上述过程及信息填空:
(1)步骤④用浓氨水调节pH后,加热至沸30min的作用是 。
(2)写出检验Ca2 的离子方程式 。
(3)写出沉淀C所含主要物质的化学式 。
(4)写出步骤⑧用A试剂生成红色溶液的离子方程式 。
(5)步骤⑨的作用是 ,猜测步骤⑩的目的是 。
六、(本题包括2小题,共16分)
22.(8分)用化学方法测定微量碘化物时,必须利用“化学放大”反应将碘的量“放大”,然后再进行测定。下面是“化学放大”反应的实验步骤:
①向含微量I-并且呈中性或弱酸性溶液里加入溴水,将I-完全氧化成IO ![]() ,煮沸去掉过量的Br2;
,煮沸去掉过量的Br2;
②向由①制得的水溶液中加入过量的酸性KI溶液,振荡使反应进行完全;
③在②得到的水溶液中加入足量的CCl4,振荡,把生成的I2从水溶液里全部转移到CCl4中,用分液漏斗分液去掉水层;
④将③得到的CCl4层加入肼(即联氨H2N—NH2)的水溶液,振荡,使I2完全以I-形式从CCl4层进入水层,用分液漏斗分液去掉CCl4层。
经过以上四步得到的水溶液里,含有通过反应而“放大”了的碘,请回答下列问题:
 (1)写出步骤②的离子方程式,并标出下列反应的电子转移的方向和数目:
(1)写出步骤②的离子方程式,并标出下列反应的电子转移的方向和数目:
(2)将右图所示的分液漏斗中下层液体放出的操作步骤为:
① 。
②旋开活塞,使下层液体流出到一个烧杯里,当下层液体全部流出活塞的细孔时, 。
③从漏斗上口倒出上层液体。
④旋开活塞,将留在颈部的下层液体放出到盛接下层液体的烧杯里。
(3)若忽略实验过程中出现的损失,经过一次“化学放大”的溶液里,I-的量是原溶液里I-的量的 倍。经过n次“化学放大”的溶液里,I-的量是原溶液里的量的 倍。
23.(8分)在隔绝空气的条件下,某同学将一块部分被氧化的钠块用一张已除氧化膜、并用针刺一些小孔的铝箔包好,然后放入盛满水且倒置于水槽中的容器内。待钠块反应完全后,在容器中仅收集到2.24 L氢气(标准状况),此时测得铝箔质量比反应前减少了0.54g,水槽和容器内溶液的总体积为2.0 L,溶液中NaOH的浓度为0.09mol·L-1(忽略溶液中离子的水解和溶解的氢气的量)。
(1)写出该实验中发生反应的化学方程式。
(2)试通过计算确定该钠块中钠元素的质量分数。
参考答案和评分标准
一、单项选择题(本题包括8小题,每小题3分,共24分)
1、B 2、D 3、B 4、B 5、D 6、A 7、A 8、C
二、不定项选择题(本题包括8小题,每小题4分,共32分)
9、CD 10、B 11、B 12、A 13、B 14、CD 15、B 16、AD
三、(本题包括2小题,共18分)
17.(8分)
(2) 乙 (1分)
选用试剂
实验现象
第一种方法
C (1分)
有机层无色 (1分)
第二种方法
D (1分)
溶液变红 (1分)
(3)不可行(1分),因为Br2和Fe3 都能把I— 氧化成I2 (2分)
18.(10分)(1)铜锌及浓盐酸一起组成了原电池,加快了反应速率(2分)
(2)①没道理,因为H2本身难溶于水(2分)
②(2分)
将铜片加入稀硫酸中,并微热
若无气体放出,则不含锌等活泼金属杂质;若有气体则有锌等杂质
(3)(2分)
白色沉淀是氯化亚铜
向白色沉淀中加入稀HNO3等强氧化剂
溶液变蓝色,说明是一价铜
向氯化亚铜悬浊液中加入氯化钾溶液
如白色沉淀消失且得无色溶液,则原溶液为氯化亚铜,否则不是
![]() (4)[CuCl4]3-(aq) CuCl(s) 3Cl-(aq) (2分)
(4)[CuCl4]3-(aq) CuCl(s) 3Cl-(aq) (2分)
四、(本题包括2小题,共21分)
19.(10分)
(1)  (2分)
(2分)
(2)Cl2 H2O2==2HCl O2(2分)
(3)-2、 4、 6(2分)
(4)Al2Te3 6H2O==2Al(OH)3↓ 3H2Te↑(或其它合理答案(2分)
(5)Se(1分)O2(1分)
20.(11分)
(1)Zn 2H =Zn2 H2↑ Cd 2H =Cd2 H2↑(3分)
(2)Zn(1分),电解回收金属Zn (或者加入适量的生石灰,过滤;或者加入适量的氢氧化钡,过滤) (2分)(3)阴极(1分);Cd2 2e- =Cd(2分)(4)Cd2 S2- =CdS↓(2分)
五、(本题包括1小题,共9分)
21.(9分)(1)使Al3 、Fe3 完全沉淀(1分)
(2)Ca2 (NH4)2C2O4 CaC2O4↓ 2NH4 (2分)
(3)Fe(OH)3、Al(OH)3(各1分,共2分)
(4)Fe3 3SCN— Fe(SCN)3(写成其它正确的络合离子形式给分,2分)
(5)使Fe3 转化为Fe(OH)3沉淀;检验Al3 (或铝元素)存在。(各1分,共2分)
六、(本题包括2小题,共16分)
22.(8分)(1) ![]()
(2)①取下漏斗口上的塞子。②迅速关闭活塞
(3)6;6n
23.(8分)
(1)① 2Na 2H2O == 2NaOH H2↑
② Na2O H2O == 2NaOH
③ 2Al 2NaOH 2H2O == 2NaAlO2 3H2↑
(2)n (Al)=0.54g÷27 g·mol 一l=0.02 mol
根据反应③ 可得由铝消耗NaOH 的物质的量为n ( NaOH ) =0.02 mol
生成的氢气的物质的量为n (H2)=0.03mol
那么由金属钠生成的氢气的物质的量为
n (H2)=2.24L/22.4L·mol 一l -0.03 mol = 0. 07 mol
根据反应① 可得金属钠的物质的量为n (Na)=2×0.07 mol = 0.14mol
又因为反应后溶液中的NaOH 的物质的量为
n (NaOH)= 2.0 L×0.09mol·L一= 0.18mol
所以溶液中Na 的总物质的量即原金属钠的总物质的量为
n (Na )= 0.18 mol 0.02 mol = 0.2 mol
n (Na2O)= (0.2 mol-0.14 mol)/2= 0.03 mol
该钠块中钠元素的质量分数为
![]() 90.6%
90.6%
