| 中文域名: 古今中外.com
英文域名:www.1-123.com 丰富实用的教育教学资料 |
| |
| |
| |
|
|
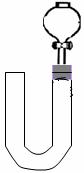
五、(本题包括2小题,共22分) 26.(12分) 为清楚地看到无色NO遇空气变为红棕色(或浅棕色)的过程。某化学爱好小组的甲、乙两位同学分别设计如下两个实验: (1)甲同学实验如图一,步骤如下:①取大试管,放入适量大理石,加入过量稀硝酸②如图塞好疏松的棉花和铜丝③一段时间后,使铜丝浸入过量的硝酸反应④慢慢向试管底部推入棉花,可见明显现象。第①步放入大理石的作用是: 。 (2)乙同学则用图二装置,他的设想是这样:从分液漏斗注入稀硝酸,直到浸没铜丝,然后,关闭分液漏斗活塞, NO产生的压强将排开稀硝酸,达一定体积后,打开分液漏斗活塞,硝酸液体将NO气体压入空分液漏斗,在分液漏斗球部空间因接触空气而变色。但按他的方法实际操作的丙同学发现此法至少存在两个问题:
②反应开始后,因为随着NO的体积增加,由于 影响铜丝与硝酸的继续反应。 (3)丙同学将分液漏斗下端管口上提至与塞子下端齐平,解决了第①个问题,再用一个与U形管配套的单孔塞和另一个分液漏斗,仍用前述乙的仪器和思路,从左边顺利地将硝酸加到分液漏斗活塞处,请在左图中补齐装置并非凡画出铜丝的适当位置: (4)丁同学根据丙的思路,认为可以测定一下NO的体积并计算其产率(不考虑有其它气体),假如给你图三所示的仪器及一个酸式滴定管,用一根橡胶皮管将它们连接起来。为成功量取产生NO的体积,此实验中注入的硝酸在滴定管中至少应到达 ,设定有条件精确称量,还需要的数据是 。 (5)计算知:将等体积NO和O2通入倒置于水槽中的盛满水的试管中,充分反应后剩余气体的体积为原气体总体积的1/8,但准确的实验表明:余气体积比计算结果要大,实事求是的科学精神,要求我们应认真思考。已知氢氧化钠溶液可以吸收NO2,方程式为
27.(10分)聚合氯化铝晶体的化学式为[Al2(OH)nCl6-n・xH2O]m,它是一种高效无机水处理剂,它的制备原理是调节增大AlCl3溶液的pH,通过促进其水解而结晶析出。其制备原料主要是铝加工行业的废渣――铝灰,它主要含Al2O3、Al,还有SiO2等杂质。聚合氯化铝生产的工艺流程如下:
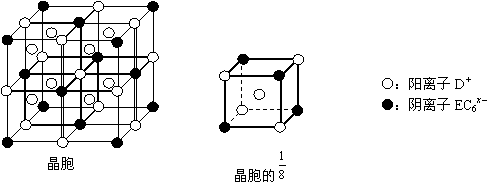
(5)如图,铁有δ、γ、α三种同素异形体,三种晶体在不同温度下能发生转化。下列说法正确的是 A.γ-Fe晶体中与每个铁原子距离相等且最近的铁原子有6个 B.α-Fe晶体中与每个铁原子距离相等且最近的铁原子有6个 C. 若δ-Fe晶胞边长为acm,α-Fe晶胞边长为bcm,则两种晶体密度比为2b3:a3
 试题答卷 试题答卷
22. (10分) ①____________ ___。 ②_______ _ _______。 ③______________ ___。 ④_____________ ______。 ⑤_____________ ______。 23.(12分) (1)a电极材料为_______,其电极反应式为_______________________。 (2)电解液d可以是_______;也可以是_______。 (3)其作用是__________ 目的是________________ 。 (4) ______________________。 (5) _______________________________。 24.(10分)(1) 。 (2) ① ;② ;③ 。 (3) ① 。 ② ,B的化学式为 。 ③ 25.(10分) (1) ②→⑥_____________________________________ ⑦→④_____________________________________ (2)
| 组合
| A
| B
| nA与nB的关系
| Ⅰ
|
|
|
| Ⅱ
|
|
|
| Ⅲ
|
|
| |
26.(12分) (1) 。
(2)① 。② 。
 (3)
(3)
(4) , 。
(5)
27.(10分)
|
|
。
(2) (3) (4)
(5) (6) 。
28(A).(10分)
(1)重氮甲烷的电子式为 。
(2)碳烯的电子式是 。
(3) 。
(4) 或 。
(5) ① ;
= 2 \* GB3 ②
28(B).(10分)
⑴________________ ,__________________。
⑵__________。
⑶_____________ ________ __
⑷_________ 。
(5)
参考答案
1
2
3
4
5
6
7
8
9
10
A
D
C
D
D
B
B
D
B
B
11
12
13
14
15
16
17
18
19
20
A
CD
A
AD
B
C
C
AD
B
C
三、(本题包括2小题,共22分)
21.(6分)
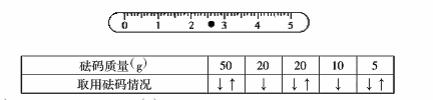
22.⑴①用蒸馏水湿润试纸;②检漏;③检查活塞旋转是否灵活(检漏);④干燥。⑤将游码拨回零点,调零(各2分)
23.(12分) ①Fe;Fe-2e=Fe2 (2分) ②C;B(2分)
③隔绝空气防止Fe(OH)2被空气氧化;排尽溶液中的氧气,防止生成的Fe(OH)2在溶液中氧化 (4分) ④B、C (2分) ⑤白色沉淀迅速变成灰绿色,最后变成红褐色(2分)
24.(10分)
(1)S1>S3>S2>S4(2分)
(2)①b ②c ③a(各1分,共3分)
(3)①HClO4(1分)②离子键、(极性)共价键(2分,各1分) NaClO(1分)
③SiO2 2C ![]() Si 2CO↑(1分)
Si 2CO↑(1分)
25 (10分)(1)H2S 2 ![]() =S2- 2H2O (2分) SO
=S2- 2H2O (2分) SO ![]() Br2 H2O=SO
Br2 H2O=SO ![]() 2Br― 2H (2分)
2Br― 2H (2分)
(2)Na2S,Na2SO3, ![]() (3分) Na2S,Na2S2O3,
(3分) Na2S,Na2S2O3, ![]() (3分)
(3分)
26. (12分)
(1)与稀硝酸作用生成CO2排出试管中的空气 (1分)
(2) ①如图二所示的铜丝所在空间中被封闭一段空气; (1分)
②产生的NO排开酸液而与大部分铜丝脱离接触。(1分)
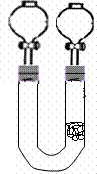 (3)(2分)正确画出如右图得2分。左边下端漏斗口露出橡皮塞也正确。若左边画一普通漏斗,亦给分。
(3)(2分)正确画出如右图得2分。左边下端漏斗口露出橡皮塞也正确。若左边画一普通漏斗,亦给分。
![]() (4)酸式滴定管最大量程刻度处。铜丝反应前后的质量(4分)
(4)酸式滴定管最大量程刻度处。铜丝反应前后的质量(4分)
![]()
![]() (5) (3分)
(5) (3分)
在此反应条件下,氮氧化物(NO、 ![]() )的最终产物并非HNO3一种,实际存在着较低价态的
)的最终产物并非HNO3一种,实际存在着较低价态的 ![]() ,实际消耗氧气的量将要减少。
,实际消耗氧气的量将要减少。
(答出一条以上反应,讲出耗氧量减小的意思,都给满分。)
27.(10分)
(1)Al2O3 6H =2Al3 3H2O, 2Al 6H =2Al3 3H2↑ (2分,各1分)
(2)过滤(1分) (3)H2 (1分) (4)HCl(2分)
(5)促进AlCl3水解,使晶体析出。(2分) (6)BD(2分,少一个扣一分,扣完为止)
28(A)(10分)略
28(B).(10分)(1)⑴ ![]() (1分) 第二周期、第ⅦA族 (2分)
(1分) 第二周期、第ⅦA族 (2分)
⑵ Na (1分)
⑶ 2Al+2NaOH+2H2O=2NaAlO2+3H2↑ (2分) ⑷ Na3AlF6 (2分)
(5) B C(2分,选1个且正确的给1分,错选一个该题0分,)
| |