化 学 试 题
命题人:储方飞
注重事项:
1.本试卷共6页,满分100分,考试时间100分钟
2.本卷可能涉及的相对原子质量:H—1;O—16;Na—23;Cl—35.5;K—39;Fe—56
第 = 1 * ROMAN I卷(共45分)
一、选择题(本题共15小题,每题只有一个正确选项,每小题3分,共45分)
1.2007年6月,“八国峰会”再次就温室气体减排问题展开磋商并初步达成共识。为减少二氧化碳这种温室气体的排放,下列措施不切实际的是 ( )
A.大力开发氢能源 B.充分利用太阳能
C.不使用含碳能源 D.提高能源利用率
2.用固体NaOH配制物质的量浓度溶液时,下列操作导致溶液浓度偏高的是 ( )
A.在烧杯中溶解时,有少量液体溅出 B.样品中混有Na2O杂质
C.容量瓶使用前未经干燥 D.定容时眼睛在容量瓶刻度线下方
3.100g质量分数为3.65%的盐酸与11.6gNa2CO3·xH2O刚好完全反应,则x值是( )
A.1 B.3 C.7 D.9
4.阿伏加德罗常数约为6.02×1023mol-1,下列叙述正确的是 ( )
A.100g98%的浓硫酸中含氧原子个数为4×6.02×1023
B.5.6 g铁粉与硝酸反应失去的电子数一定为3×6.02×1022
C.标准状况下,22.4LCH4和CH3Cl的混合物所含有的分子数目约为6.02×1023
D.6.2g氧化钠和7.8g过氧化钠的混合物中所含有的离子总数约为7×6.02×1022
5.下列说法正确的是 ( )
A.摩尔是6.02×1023个结构微粒的集体
B.0.012kg12C所含的原子数精确值是6.02×1023
C.1mol H就是1mol氢 D.1molH2SO4的质量是98g
6.标准状况下,13g某气体的分子数与14g一氧化碳分子数相等,则该气体的密度为( )
A.11.6g/L B.1.16g/L C.12.5g/L D.1.25g/L
7.下列各组离子,在指定的环境中一定能大量共存的是 ( )
A.滴加石蕊试液显红色的溶液:Fe3+、NH4+、C1-、SCN-
B.含有大量HCO3-的溶液:NH4 、Ca2 、Mg2+、I-
C.在加入铝粉能产生H2的溶液中:NH4 、Fe2 、SO42-、NO3-
D.含有大量ClO-的溶液:H 、Mg2 、I-、SO42-
8.将a g钠投入b g水中(足量水),反应后所得溶液中溶质的质量分数是 ( )
A. ![]() B.
B. ![]() C.
C. ![]() D.
D. ![]()
9.下列实验操作中错误的是 ( )
A.用分液漏斗分液时,下层液体从下口放出,上层液体从上口倒出
B.蒸发结晶时,应将溶液蒸干,并放在干燥器中冷却
C.无锈的细铁丝可以代替铂丝,做焰色反应的工具
D.蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处
10.苹果酸是一种常见的有机酸,结构简式为 ![]() ,它可能发生的反应是:①与NaOH溶液反应;②与石蕊试液作用变红;③与金属钠反应放出气体;④一定条件下与乙酸酯化 ⑤一定条件下与乙醇酯化 ( )
,它可能发生的反应是:①与NaOH溶液反应;②与石蕊试液作用变红;③与金属钠反应放出气体;④一定条件下与乙酸酯化 ⑤一定条件下与乙醇酯化 ( )
A.①②③ B.①②③④ C.①②③⑤ D.①②③④⑤
11.有KOH和KHCO3混合物26.2g,在250℃下煅烧,冷却后称量,质量减少4.65g,则原混合物中KOH和KHCO3的物质的量的关系是 ( )
A.KOH>KHCO3 B.KOH<KHCO3 C.KOH = KHCO3 D.任意比混合
12.将标准状况下的aLHCl(气)溶于1000g水中,得到的盐酸密度为bg/cm3,则该盐酸的物质的量浓度是 ( )
A. ![]() mol/L B.
mol/L B. ![]() mol/L
mol/L
C. ![]() mol/L D.
mol/L D. ![]() mol/L
mol/L
13.向0.1 mol/L的NaOH溶液中加入0.1 mol/L的盐酸。若用X代表加入盐酸的体积,Y代表溶液中离子的总数,则下列曲线中正确的是 ( )
SHAPE * MERGEFORMAT
|
X |
|
Y |
|
X |
|
Y |
|
X |
|
Y |
|
X |
|
Y |
|
A |
|
B |
|
C |
|
D |
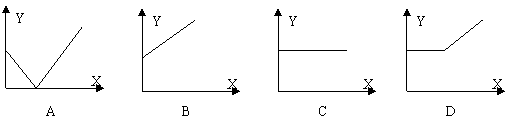
14.从矿物学资料查得,一定条件下自然界存在如下反应:
14CuSO4 5FeS2 12H2O ==== 7Cu2S 5FeSO4 12H2SO4
下列说法正确的是 ( )
A.Cu2S既是氧化产物又是还原产物 B.5mol FeS2发生反应,有10mol电子转移
C.产物中的SO42-离子有一部分是氧化产物 D.FeS2只作还原剂
15.关于锂、钠、钾、铷、铯的性质递变规律,不正确的叙述是 ( )
A.单质的密度依次增大 B.单质的熔沸点依次降低
C.单质的还原性依次增强 D.离子的氧化性依次减弱
第 = 2 * ROMAN II卷(共55分)
二、填空题(本题共3小题,共26分)
16(11分)有一瓶溶液只含Cl-、CO32-、SO42-、Na 、NH4 、K 、Mg2 七种离子中的某几种。经如下实验:
(1) 原溶液 ![]() 白色沉淀
白色沉淀
(2) 将(1)所得溶液 ![]() 放出使湿润的红色石蕊试纸变蓝的气体
放出使湿润的红色石蕊试纸变蓝的气体
(3) 原溶液中加BaCl2溶液不产生沉淀
(4)原溶液中加AgNO3溶液产生白色沉淀,再加稀硝酸白色沉淀不溶解
回答下列问题:
(1)原溶液中一定含有的离子是___________________,一定不含有的离子是
可能含有的离子是
(2)有同学认为实验(4)可以省略,你认为呢?(填“可以”或“不可以”) ,说明理由
(3)可能含有的离子如何加以确定?
17(3分)80mLNaOH溶液,蒸发掉20g水后溶质的质量分数由40%变为50%,则原溶液
的物质的量浓度是 。
18 (12分)有一类无机化合反应的通式可以表示为:单质 化合物(1)=化合物(2),请写出满足以下要求的四个此类无机化合反应的化学方程式: = 1 * GB3 ①所涉及的元素的原子序数都小于30 = 2 * GB3 ②4种单质分属4个不同族
(1) ;
(2) ;
(3) ;
(4) 。
三、实验题(本题共1小题,共11分)
1 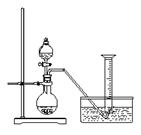 9 (11分) 某同学设计了如下方案,来测定过氧化钠样品的纯度(杂质不参加反应,条件为标准状况)。
9 (11分) 某同学设计了如下方案,来测定过氧化钠样品的纯度(杂质不参加反应,条件为标准状况)。
实验原理:2Na2O2 + 2H2O = 4NaOH + O2↑
通过测定生成的氧气的体积,经计算可确定样品中过氧化钠的含量。
实验步骤:
①称取过氧化钠样品2.00 g ;
②把这些过氧化钠样品放入气密性良好的气体发生装置中;
③向过氧化钠样品中滴入水,用量筒排水集气,量筒内液面准确读数为110.0 mL;
④ 作为反应器的烧瓶中有54.0 mL液体;
⑤ 将烧瓶内的液体转移到250 mL的容量瓶内,并加水定容。
请回答下列问题:
(1)有1000 mL、 500 mL 、250 mL的量筒备用,则应选用 mL的量筒。
(2)生成气体体积是 mL, 为保证生成气体体积的准确性.读取量筒刻度时应注重的问题是 。
(3)据研究,与上述反应同时发生的反应还有:Na2O2 + 2H2O = 2NaOH + H2O2,H2O2的生成会使测定结果 (填“偏高”或“偏低”)。
(4)为校正实验结果,该学生补做了如下实验:用移液管移取20.00 mL容量瓶中的液体,放入锥形瓶中,用0.0100 mol/L的KMnO4溶液去测定,至溶液中刚好出现浅浅的紫红色,停止滴定,用去了24.00 mLKMnO4溶液。配平化学反应式方程式:
KMnO4 + H2O2 + H2SO4 —— K2SO4 + MnSO4 + O2↑ + H2O
该实验应选用 式滴定管。
(5)通过以上数据计算,该过氧化钠的纯度为 。
(6)如何避免因为生成H2O2造成的误差? 。
四、推断题(本题共1小题,共10分)
20(10分)江苏省东临大海,利用海水等可制得多种化工产品。下图是以海水、贝壳等为原料制取几种化工产品的转化关系图,其中海水晒盐后的母液的主要成份俗称苦卤,E是一种化肥,N是一种常见的金属单质。
|
④ |
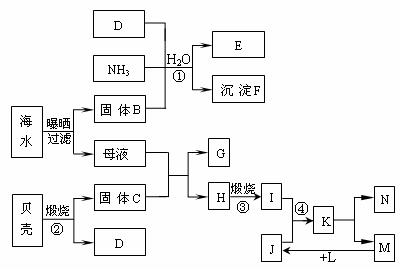 |
试填写下列空白:
⑴N的化学式为:_________________;E的电子式____________________。
⑵写出反应①的化学方程式: 。
⑶反应④的离子方程式 。
⑷由K溶液经如何处理才能制得N?
_ 。
五、计算题(本题共1小题,共8分)
21(8分)向一定量的Fe、FeO、Fe2O3混合物中加入1.00mol/L的盐酸100mL,可恰好使混合物完全溶解,放出标准状况下224 mL的气体。向所得溶液中加入KSCN溶液,无血红色出现。
(1)若用足量的CO在高温条件下还原相同质量的此混合物,能得到单质铁的质量是多少?
(2)若原混合物是Fe和Fe3O4,求原混合物中铁元素的质量分数。
高三第一学期第二次段考
化学参考答案
一、选择题(本题共15小题,每题只有一个正确选项,每小题3分,共45分)
1C 2 B 3C 4C 5D 6B 7B 8D 9B 10 D 11B 12C 13D 14C 15A
16.(11分)(1)Mg2 、 ![]() 、Cl-(2分);
、Cl-(2分); ![]() 、
、 ![]() (2分); Na 、 K (2分)
(2分); Na 、 K (2分)
(2)可以(1分);溶液显电中性有阳离子存在必有阴离子存在(2分,其他答案合理给分)
(3) 经焰色反应,若显黄色,说明含有Na ,否则不含Na ;焰色反应时透过蓝色的钴玻璃观察,若显紫色说明含有K ,否则不含K 。(2分)
17.12.5mol/L (3分)
18.(12分)(1)2NO O2= 2NO2或 2CO O2= 2CO2或2Na2SO3 O2 = 2Na2SO4 (3分)
(2) C CO2 === 2CO(高温条件下) (3分)
(3) 2FeCl2 Cl2 === 2FeCl3 (3分)
(4) 2FeCl3 Fe === 2FeCl2 (3分)
本题答案无先后顺序,其它合理答案也给分。
19(11分)(1)250 mL (1分)
(2)56 mL (1分); 使量筒内外液面持平(1分)
(3)偏低(1分)
(4)2、5、3-1、2、5、8(2分); 酸式滴定管(1分)
(5)48.75 %(2分)
(6)在过氧化钠与水反应之前加少量的二氧化锰(2分)
20(10分).⑴Mg (2分); ![]() (2分)
(2分)
⑵NaCl(饱和) NH3 CO2 H2O=NaHCO3↓ NH4Cl (2分)
⑶MgO+2H+=H2O+Mg2+ (2分)
⑷MgCl2溶液必须在HCl气体中进行蒸发结晶制得MgCl2晶体,熔融后电解才能制取金属镁(2分)
21(8分) (1) 2.8g(3分); (2)81.4%(5分)
解析:(1)依题意,最终所得溶液为FeCl2,根据:FeCl2 ~ 2HCl ~ Fe (1分)
m(Fe)= 1.00mol/L×0.1L× ![]() ×56g/mol = 2.8g (2分)
×56g/mol = 2.8g (2分)
(2) 因为Fe3O4~FeO Fe2O3,故设Fe、FeO、Fe2O3的物质的量分别为x、y、y,则有:
![]()
![]() (x y 2y) ×56 = 2.8 质量关系 x=0.02mol (1分)
(x y 2y) ×56 = 2.8 质量关系 x=0.02mol (1分)
(x -y )×22.4 = 0.224 气体关系 解得: y=0.01mol (1分)
或2x = 2y 0.01×2 电子守恒
![]() (2分)
(2分)
