学科:化学
教学内容:化学反应速率 化学平衡
一、考纲要求
1.了解化学反应速率的概念,反应速率的表示方法,外界条件(浓度、温度、压强、催化剂等)对反应速率的影响。
2.了解化学反应的可逆性,理解化学平衡的含义,把握化学平衡与反应速率之间的内在联系。
3.理解勒沙特列原理的涵义,把握浓度、温度、压强等条件对化学平衡移动的影响。
二、知识结构
1.化学反应速率的表示方法及特点。
(1)表示方法:
用单位时间内反应物浓度的减少或者生成物浓度的增加来表示。
表达式: ![]() =
= ![]()
单位:由浓度的单位和时间的单位决定。mol/L·h、mol/L·min、mol/L·s等。
(2)特点:
①化学反应速率是平均速率,且均取正值。
②同一反应选用不同物质浓度的改变量表示速率,数值可能不同,但表示的意义相同。 ③各物质表示的速率比等于该反应方程式的系数比。
例:对于反应:mA nB ![]() pC qD
pC qD
VA∶VB∶VC∶VD=m∶n∶p∶q
2.影响化学反应速率的因素。
决定化学反应速率的主要因素是反应物的结构,性质,反应历程。除此之外,外部条件,为反应物的浓度、压强、温度、催化剂以及固体反应物表面积的大小、溶剂、光、电磁波、激光、超声波等都会影响化学反应的速率。
(1)浓度:在其它条件不变时,增大反应物浓度,化学反应速率加快;反之则慢。
注重:固体,纯液体的浓度均可视作常数。因固体物质间的反应只与接触面积有关,故固体物质的量的改变对反应速率无影响。
(2)压强:在其它条件不变时,增大气体反应体系压强,化学反应速率加快;反之则慢。
注重:改变压强,对化学反应速率产生影响的根本原因是引起浓度改变。所以,在讨论压强对反应速率的影响时,应区分引起压强改变的原因。
对于气体反应体系,有以下几种情况:
①恒温时:增加压强 ![]() 体积缩小
体积缩小 ![]() 浓度增大
浓度增大 ![]() 反应速率加快。
反应速率加快。
②恒容时:
a.充入气体反应物 ![]() 浓度增大
浓度增大 ![]() 总压增大
总压增大 ![]() 反应速率加快。
反应速率加快。
b.充入“惰气” ![]() 总压增大,但各物质浓度不变,反应速率不变。
总压增大,但各物质浓度不变,反应速率不变。
③恒压时:充入“惰气” ![]() 体积增大
体积增大 ![]() 各反应物浓度减少
各反应物浓度减少 ![]() 反应速率减慢。
反应速率减慢。
(3)温度:其它条件不变时,升高温度,反应速率加快。
温度每升高10℃,化学反应速率增大到原来的2—4倍。升高反应体系的温度,是提高反应速率的有效途径。
(4)催化剂:使用正催化剂,能加快化学反应速率。反之则反,未非凡指明时,均指正催化剂。
3.化学平衡状态
(1)概念:在一定条件下的可逆反应里,正反应速率和逆反应速率相等,反应混合物中各组分的质量分数保持不变的状态。
(2)特征
①逆:研究对象可逆反应。
②等:V(正)=V(逆)≠O
③动:化学平衡是动态平衡。虽然V(正)=V(逆),但正、逆反应仍在进行,其反应速率不等于零。
④定:各组分的质量分数一定。
⑤变:外界条件改变,平衡也随之改变。
⑥无:化学平衡的建立与反应从哪个方向(正向、逆向、双向)开始无关。
4.化学平衡移动
(1)当外界条件改变时,可逆反应从一种平衡状态向另一种平衡状态转化的过程。
(2)平衡发生移动的根本原因:V正、V逆发生改变,导致V正≠V逆。
(3)平衡发生移动的标志:新平衡与原平衡各物质的百分含量发生了变化。
注重:
①新平衡时: ![]() ,但与原平衡速率不等。
,但与原平衡速率不等。
②新平衡时:各成分的百分含量不变,但与原平衡不同
③通过比较速率,可判定平衡移动方向
当V正>V逆时,平衡向正反应方向移动
当V正<V逆时,平衡向逆反应方向移动
当V正=V逆时,平衡不发生移动
5.可逆反应进行程度的描述方法——转化率、产率。
(1)反应物的转化率=反应物的转化量/该反应物起始量×100%
(2)产物的产率=产物的实际量/该产物的理论量×100%
6.外界条件对化学平衡的影响。
(1)浓度:其它条件不变时,增大反应物浓度或减小生成物浓度都会使平衡向正反应方向移动。
改变物质浓度不包括固体和纯液体,即固体或纯液体物质的量的增加和减少,不影响浓度, 从而不影响化学反应速率,也不影响化学平衡。
(2)压强:其它条件不变时,增大压强,会使平衡向气体体积缩小的方向移动。
注重:
①若反应前后气体体积无变化,改变压强,能同时改变正、逆反应速率,V正=V逆,平衡不移动。
②压强变化是指平衡混合物体积变化而引起的总压变化,若平衡混合物的体积不变,而加入“惰气”,虽然总压变化了,但平衡混合物的浓度仍不变,速率不变,平衡不移动。
③若加入“惰气”,保持总压不变,此时只有增大体系体积,这就相当于降低了平衡体系的压强,平衡向气体体积增大的方向移动。
(3)温度:在其它条件不变时,升高温度,化学平衡向吸热反应方向移动。降低温度,平衡向放热反应方向移动。
(4)催化剂:催化剂能同等程度地改变正、逆反应速率,因此不影响化学平衡,但可大大地缩短反应达到平衡所需的时间。
(5)勒沙特列原理:假如改变影响平衡的一个条件,平衡就向能够减弱这种改变的方向移动。
注重:勒沙特列原理的适用范围是:化学平衡,电离平衡,溶解平衡,水解平衡,状态平衡等。
7.合成氨的反应原理:N2(g) 3H2(g) ![]() 2NH3(g) 92.4KJ
2NH3(g) 92.4KJ
合成氨是一个气体体积缩小的放热可逆反应。
8.原料气的制备:
①空气中取氮:分离液态空气或用炽热的炭处理空气后再净化。
②水中取氢:水和焦炭反应。
9.合成氨适宜条件的选择。
①选择原则:能加快反应速率;提高原料的利用率;提高单位时间的产量;对设备条件要求不能太高。
②合成氨的适宜条件:使用催化剂;500℃;2×107~5×107Pa。
10.合成氨的简要流程
原料气的制备 ![]() 净化
净化 ![]() 压缩
压缩 ![]() 合成
合成 ![]() 分离
分离 ![]() 液氨
液氨
三、知识点、能力点提示


【同步达纲练习】
1.100ml 6mol/L H2SO4与过量锌粉反应,一定温度下,为了减缓反应进行的速率,但又不影响生成氢气的总量,可向反应物中加入适量的( )
A.Na2SO4(s) B.H2O C.K2SO4溶液 D.(NH4)2SO4(s)
知识点:本题考查浓度对反应速率的影响
能力点:培养学生正确理解和应用能力
2.设C CO2 ![]() 2CO-Q1,反应速率为V1;N2 3H2
2CO-Q1,反应速率为V1;N2 3H2 ![]() 2NH3 Q2,反应速率为V2,对于上述反应,当温度升高时,V1和V2的变化情况为( )
2NH3 Q2,反应速率为V2,对于上述反应,当温度升高时,V1和V2的变化情况为( )
A.同时增大 B.同时减少
C.V1增大,V2减小 D.V1减小,V2增大
知识点:本题考查温度对反应速率的影响
能力点:培养学生理解能力
3.以真空密闭容器中盛有1 mol PCl5加热到200℃时发生的如下反应:PCl5(气) ![]() PCl3(气) Cl2(气),反应达平衡后,PCl5所占体积分数为M%。若在同一温度和同一容器中,最初投入的是2 mol PCl5(气),反应达平衡时,PCl5所占体积分数为 N%。则M和N的正确关系是( )
PCl3(气) Cl2(气),反应达平衡后,PCl5所占体积分数为M%。若在同一温度和同一容器中,最初投入的是2 mol PCl5(气),反应达平衡时,PCl5所占体积分数为 N%。则M和N的正确关系是( )
A.M>N B.M<N
C.M=N D.无法比较
知识点:反应物的物质的量对化学平衡的影响。
能力点:比较能力。
4.下图为装有活塞的密闭容器,内盛22.4mL一氧化氮,若通入11.2mL氧气(气体体积均在标准状况下测定),保持温度压强不变,则容器内的密度( )
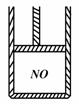
A.等于1.369 g·L-1 B.等于2.054 g·L-1
C.在1.369g·L-1和2.0 54g·L-1之间 D.大于2.054g·L-1
知识点:本题考查气体密度的计算及2NO2 ![]() N2O4平衡
N2O4平衡
能力点:培养学生计算能力和综合思维能力
5.下列措施肯定能使化学反应速率增大的是( )
A.增大反应物的量 B.增大压强
C.升高温度 D.使用催化剂
知识点:本题考查外界条件对化学反应速率的影响
能力点:培养学生思维能力
6.将固体NH4I置于密闭容器中,在某温度下发生下列反应:( )
NH4I(固) ![]() NH3(g) HI(g),2HI(g)
NH3(g) HI(g),2HI(g) ![]() H2(g) I2(g),当达到平衡时 ,[H2]=0.5mol/L,[HI]=4mol/L,则NH3的浓度为
H2(g) I2(g),当达到平衡时 ,[H2]=0.5mol/L,[HI]=4mol/L,则NH3的浓度为
A.3.5mol/L B.4mol/L C.4.5mol/L D.5mol/L
知识点:本题考查关于化学平衡的有关计算
能力点:培养学生计算能力和理解能力
7.在一密闭容器中进行下列反应:2SO2 O2 ![]() 2SO3(g),已知反应过程中某一时刻SO2、O2、SO3的浓度分别为0.2mol/L,0.1mol/L,0.2mol/L,当反应达到平衡时,可能存在的数据是( )
2SO3(g),已知反应过程中某一时刻SO2、O2、SO3的浓度分别为0.2mol/L,0.1mol/L,0.2mol/L,当反应达到平衡时,可能存在的数据是( )
A.SO2为0.4mol/L,O2为0.2mol/L
B.SO2为0.25mol/L
C.SO2,SO3均为0.15mol/L
D.SO3为0.4mol/L
知识点:本题考查关于化学平衡的有关计算
能力点:培养学生综合思维能力
8.反应4A(s) 3B(g) ![]() 2C(g) D(g),经2 min,B的浓度减少0.6 mol/L。对此反应速率的表示,正确的是( )
2C(g) D(g),经2 min,B的浓度减少0.6 mol/L。对此反应速率的表示,正确的是( )
A.用A表示的反应速率是0.4 mol/(L·min)
B.分别用B、C、D表示反应的速率,其比值是3∶2∶1
C.在2 min末的反应速率,用B表示是0.3 mol/(L·min)
D.在这2 min内用B和C表示的反应速率的值都是逐渐减小的
知识点:本题考查化学反应速率的概念及其计算方法。
能力点:培养学生知识再现能力。
9.下列说法正确的是( )
A.可逆反应的特征是正反应速率总是和逆反应速率相等。
B.在其它条件不变时,使用催化剂只能改变反应速率,而不能改变化学平衡状态。
C.在其它条件不变时,升高温度可以使化学平衡向吸热反应的方向移动。
D.在其它条件不变时,增大压强一定会破坏气体反应的平衡状态。
知识点:本题考查外界条件对化学平衡的影响
能力点:培养学生理解能力
10.在一定条件下,可逆反应N2 3H2 ![]() 2NH3正反应是放热反应,达到平衡后,当单独改变下列条件时,有关叙述错误的是( )
2NH3正反应是放热反应,达到平衡后,当单独改变下列条件时,有关叙述错误的是( )
A.加催化剂,正、逆反应速率都发生变化,且变化的倍数相等
B.加压,正、逆反应速率都增大,且正反应速率增大倍数大于逆反应速率增大倍数
C.降温,正、逆反应速率都减小,且正反应速率减小倍数小于逆反应速率减小倍数
D.加氩气,正逆反应速率都增大,且正反应速率增大倍数大于逆反应速率增大倍数
知识点:本题考查影响化学反应速率的一些因素,如催化剂、温度、压强、体积等。
能力点:培养学生综合思维能力。
11.某体积可变的密闭容器,盛有质量的A和B的混合气体,在一定条件下发生反应:A 3B ![]() 2C,若维持温度和压强不变当达到平衡时,容器的体积为VL,其中C的气体体积占10% ,下列推断正确的是( )
2C,若维持温度和压强不变当达到平衡时,容器的体积为VL,其中C的气体体积占10% ,下列推断正确的是( )
①原混合气体的体积为1.2VL
②原混合气体的体积为1.1VL
③反应达到平衡时气体A消耗掉0.05VL
④反应达到平衡时气体B消耗掉0.05VL
A.②③ B.②④ C.①③ D.①④
知识点:本题考查有关平衡的计算。
能力点:培养学生计算能力。
12.在一密闭容器中,用等物质的量的A和B发生如下反应:
A(g) 2B(g) ![]() 2C(g),反应达到平衡时,若混合气体A和B的物质的量之和与C的物质的量相等,则这时A的转化率为:( )
2C(g),反应达到平衡时,若混合气体A和B的物质的量之和与C的物质的量相等,则这时A的转化率为:( )
A.40% B.50% C.60% D.70%
知识点:本题考查有关化学平衡及其转化率的相关计算
能力点:培养学生计算能力
13.对于达到平衡的反应:2A(g) B(g) ![]() nC(g),符合下图所示的结论是( )
nC(g),符合下图所示的结论是( )
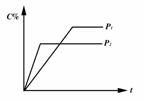
A.P1>P2,n>3 B.P1>P2,n<3
C.P1<P2,n>3 D.P1<P2,n<3
知识点:本题考查外界条件对化学平衡的影响。
能力点:培养学生正确识图能力。
14.在密闭容器中发生如下反应:mA(g) nB(g) ![]() pC(g),达到平衡后,保持温度不变,将气体体积缩小到原来的一半,当达到新平衡时,C的浓度为原来浓度的1.9倍,下列说法错误的是( )
pC(g),达到平衡后,保持温度不变,将气体体积缩小到原来的一半,当达到新平衡时,C的浓度为原来浓度的1.9倍,下列说法错误的是( )
A.m n>p B.平衡向逆反应方向移动
C.A的转化率降低 D.C的体积分数增加
知识点:本题考查体积对化学平衡的影响。
能力点:培养学生多角度思考问题的能力。
15.在一定温度下,把2体积N2和6体积H2通入一个带活塞的体积可变的容器中,活塞的一端与大气相通。容器中发生以下反应:N2 3H2 ![]() 2NH3,正反应是放热反应。若达到平衡后,测得混合气体的体积为7体积,据此回答下列问题:
2NH3,正反应是放热反应。若达到平衡后,测得混合气体的体积为7体积,据此回答下列问题:
(1)保持上述反应温度不变,设a、b、c分别代表初始加入的N2、H2和NH3的体积,反应达到平衡时,各物质的百分含量与上述平衡时完全相同,那么:①若a=1,c=2,则b= ,在此情况下,反应起始时将向 进行;② 若需规定起始时反应向逆反应方向进行,则c的范围是 。
(2)在上述容器中,若需控制平衡后混合气体为6.5体积,则可采取的措施是 。
知识点:本题考查反应物物质的量对化学平衡的影响。
能力点:培养学生综合分析能力。
16.把氮气和氢气按1∶1(物质的量之比)混合均匀后分成四等份,分别充入A、B、C、D四个装有铁触媒的真空密闭容器中(容积不变),在保持相同温度的条件下,四个容器相继达到平衡状态,分析下表中的数据,回答下列问题:
(1)平衡时, 容器中氨气所占的比例最大。
(2)达到平衡时反应速率最小的容器是 。
(3)四个容器的压强由小到大的排列次序是 。
容器代号
A
B
C
D
平衡时混合物平均式量
16
17
平衡时氮气的转化率
20%
平衡时氢气的转化率
30%
知识点:本题考查的是影响化学平衡的一些因素,如温度、浓度、体积、压强。
能力点:考查学生综合思维能力。
17.在一个容积固定的反应器中,有一个可左右滑动的隔板,两侧分别进行如图所示的可逆 反应。各物质的起始加入量如下:A、B、C均为4.0mol,D为6.5mol,F为2.0mol。设E为Xmol 。当X在一定范围内变化时,均可以通过调节反应器的温度,使两侧反应都达到平衡,并且隔板恰好处于反应器的正中位置。请填写如下空白:
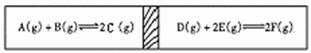
(1)若X=4.5时,则右侧反应在起始时间 (填“正反应”“逆 反应”)方向进行。欲使起始反应维持向该方向进行,则X的最大取值应小于 。
(2)若X分别为4.5和5.0时,则在这两种情况下,为反应达平衡时,A的物质的量是否相等? (填“相等”、“不相等”或“不能确定”)。其理由是 。
知识点:本题是一道信息试题,涉及到外界条件对化学平衡的影响及关于化学平衡的相关计算。
能力点:培养学生自学能力、综合能力。
18.Fe3 和I-在水溶液中的反应如下:2I- 2Fe3 ![]() 2Fe2 I2(水溶液)。
2Fe2 I2(水溶液)。
(1)该反应的平衡常数K的表达式为:K= 。当上述反应达到平衡后 ,加入CCl4萃取I2,且温度不变,上述平衡 移动(选填:向右、 向左、不)。
(2)上述反应的正向反应速率和I-、Fe3 的浓度关系为:V=K[C ![]() ]m[C
]m[C ![]() ]n(K为常数)
]n(K为常数)
C ![]() mol/L
mol/L
C ![]() mol/L
mol/L
V(mol/L·S)
(1)
0.20
0.80
0.032K
(2)
0.60
0.40
0.144K
(3)
0.80
0.20
0.128
通过所给的数据计算得知:在V=K K[C ![]() ]m[C
]m[C ![]() ]n中m、n的值为 。
]n中m、n的值为 。
A.m=1 n=1 B.m=1 n=2
C.m=2 n=1 D.m=2 n=2
I-浓度对反应速率的影响 Fe3 浓度对反应速率的影响 。(选填:大于、小于、等于)
知识点:本题是一信息试题。
能力点:培养学生自学能力,理解能力和应用能力。

参考答案
【同步达纲练习】
1.BC 2.A 3.B 4.D 5.CD 6.D 7.B 8.BD 9.BC
10.CD 11.A 12.A 13.C 14.AD
15.(1)①3 逆反应方向 ②1<c≤4 (2)降低反应温度
16.(1)C;(2)C;(3)PA<PD<PB<PC。
17.①正反应 7.0 ②不相等。因为两种情况是在两个不同温度下建立的化学平衡,平衡状态不同,所以物质的量也不相同。
18.(1) ![]() ,向右 (2)C 大于
,向右 (2)C 大于
