化学反应速率和化学平衡
【专题目标】
1.了解化学反应速率的概念及表示方法,把握同一反应中不同物质的化学反应速率与化学方程式中各物质的化学计量数的关系。
(1)概念:通常用单位时间内反应物浓度的减小或生成物浓度的增加来表示。
(2)表达式: ![]() ;单位:mol/(L·min)或mol/(L·s)。
;单位:mol/(L·min)或mol/(L·s)。
(3)在同一反应中,用不同的物质表示反应速率的数值之比等于它们在化学方程式中的化学计量数之比。
2.了解化学反应的可逆性,理解化学平衡的特征,了解化学平衡与化学反应速率之间的内在联系。
(1)概念:在一定条件下的可逆反应里,正反应和逆反应速率相等,反应混合物中各组分的浓度保持不变的状态叫做化学平衡状态,简称化学平衡。
(2)化学平衡状态的特征:
①“动” :化学平衡是动态平衡,即:v正=v逆≠0
②“等” :达到化学平衡时v正=v逆,即同一物质的消耗速率等于生成速率
③“定” :外界条件不变时,处于化学平衡状态的各物质的浓度、质量分数或体积分数保持不变
④“变” :可逆反应的平衡状态是相对的,暂时的,当影响平衡的条件改变时,化学平衡即被破坏,并在新的条件下建立新的平衡状态
3.理解浓度、压强和温度等条件对化学平衡的影响,理解平衡移动原理的涵义。
理解勒夏特列原理:假如改变影响化学平衡的一个条件(如浓度、压强或温度等),平衡就会向着能够减弱这种改变的方向移动。
4.学会应用建立等效平衡的思维方式解决化学平衡中的常见问题。
【经典题型】
一、化学反应速率
题型一:根据化学计量数之比,计算反应速率
【例1】反应4NH3(g) 5O2(g) ![]() 4NO(g) 6H2O(g)在10L密闭容器中进行,半分钟后,水蒸气的物质的量增加了0.45mol,则此反应的平均速率
4NO(g) 6H2O(g)在10L密闭容器中进行,半分钟后,水蒸气的物质的量增加了0.45mol,则此反应的平均速率 ![]() (反应物的消耗速率或产物的生成速率)可表示为( C )
(反应物的消耗速率或产物的生成速率)可表示为( C )
A. ![]() B.
B. ![]()
C. ![]() D.
D. ![]()
题型二:以图象形式给出条件,计算反应速率

题型三:根据已知的浓度、温度等条件,比较反应速率的大小
【例3】把下列四种X溶液分别加入四个盛有10mL 2mol/L盐酸的烧杯中,均加水稀释到50mL,此时,X和盐酸缓慢地进行反应,其中反应最快的是( B )
A.10℃20mL 3mol/L的X溶液
B.20℃30mL 2mol/L的X溶液
C.20℃10mL 4mol/L的X溶液
D.10℃10mL 2mol/L的X溶液
二、化学平衡
题型四:已知一个可逆反应、一种起始状态
【例4】把6 mol A气体和5 mol B气体混合放入4 L密闭容器中,在一定条件下发生反应:3A(g) B(g) ![]() 2C(g) xD(g)经5min达到平衡,此时生成C为2mol,测定D的平均反应速率为0.1mol/(L·min),下列说法中错误的是 ( BD )
2C(g) xD(g)经5min达到平衡,此时生成C为2mol,测定D的平均反应速率为0.1mol/(L·min),下列说法中错误的是 ( BD )
A.A的平均反应速率为0.15mol/(L·min)
B.恒温达到平衡时容器内压强为开始时的85%
C.B的转化率为20%
D.平衡时A的浓度为0.8mol/L
【方法点拨】有关化学平衡的计算可按“起始、转化、平衡”列出各自的量,若碰到未知量则设出,再从题目中寻找已知关系列出等式求解。
【例5】某温度下,在一容积可变的容器中,反应2A(g) B(g) ![]() 2C(g) 达到平衡时,A、B和C的物质的量分别为4 mol、2 mol和4 mol。保持温度和压强不变,对平衡混合物中三者的物质的量做如下调整,可使平衡右移的是(C )
2C(g) 达到平衡时,A、B和C的物质的量分别为4 mol、2 mol和4 mol。保持温度和压强不变,对平衡混合物中三者的物质的量做如下调整,可使平衡右移的是(C )
A.均减半 B.均加倍 C.均增加1 mol D.均减少1 mol
【方法点拨】涉及化学平衡移动的问题可按下图去思考:
反应特征
影响因素![]()
![]()
![]()
![]() 速率变化
速率变化
移动方向
题型五:已知一个可逆反应、两种起始状态
【例6】可逆反应A(g)+B(g) ![]() 2C(g)在固定容积的容器中进行,假如向容器中充入1mol A和1mol B,在某温度下达到平衡时,C的体积分数为m%;若向容器中充入1mol C,在同样的温度下达到平衡时,C的体积分数为n%,则m和n的关系正确的是( C )
2C(g)在固定容积的容器中进行,假如向容器中充入1mol A和1mol B,在某温度下达到平衡时,C的体积分数为m%;若向容器中充入1mol C,在同样的温度下达到平衡时,C的体积分数为n%,则m和n的关系正确的是( C )
A.m>n B.m<n C.m=n D.无法比较
【例7】在一密闭的容器中充入2mol A和1mol B发生反应:2A(g)+B(g) ![]() xC(g),达到平衡后,C的体积分数为w%;若维持容器的容积和温度不变,按起始物质的量A:0.6mol、B:0.3mol、C:1.4mol充入容器,达到平衡后,C的体积分数仍为w%,则x的值为( C )
xC(g),达到平衡后,C的体积分数为w%;若维持容器的容积和温度不变,按起始物质的量A:0.6mol、B:0.3mol、C:1.4mol充入容器,达到平衡后,C的体积分数仍为w%,则x的值为( C )
A.只能为2 B.只能为3
C.可能为2,也可能为3 D.无法确定
【例8】在一个盛有催化剂容积可变的密闭容器中,保持一定温度和压强,进行以下反应:N2+3H2 ![]() 2NH3。已知加入1mol N2和4mol H2时,达到平衡后生成a mol NH3(见下表已知项)。在相同温度、压强下,保持平衡时各组分的体积分数不变。对下列编号①~③的状态,填写表中空白。
2NH3。已知加入1mol N2和4mol H2时,达到平衡后生成a mol NH3(见下表已知项)。在相同温度、压强下,保持平衡时各组分的体积分数不变。对下列编号①~③的状态,填写表中空白。
已知
编号
起始状态物质的量 n/mol
平衡时NH3的物质的量
n/mol
N2
H2
NH3
1
4
0
a
①
1.5
6
0
②
1
0.5a
③
m
g(g≥4m)
【方法点拨】已知一个可逆反应、两种起始状态可从以下角度考虑:
![]() 两边系数相等:若对应物质成比例则从等效平衡;若对应物质相等则从等同平衡角度考虑
两边系数相等:若对应物质成比例则从等效平衡;若对应物质相等则从等同平衡角度考虑
恒温恒容
两边系数不等:从等同平衡角度考虑
恒温恒压:若对应物质成比例则从等效平衡角度考虑;若对应物质相等则从等同平衡角度考虑;
题型六:通过建立等效平衡的中间状态,比较反应物
转化率的大小以及平衡时某物质体积分数、浓度的大小
【例9】体积相同的甲、乙两个容器中,分别充有等物质的量的SO2和O2,在相同温度下发生反应:2SO2+O2 ![]() 2SO3并达到平衡。在这过程中,甲容器保持体积不变,乙容器保持压强不变,若甲容器中SO2的转化率为p%,则乙容器中SO2的转化率为( B )
2SO3并达到平衡。在这过程中,甲容器保持体积不变,乙容器保持压强不变,若甲容器中SO2的转化率为p%,则乙容器中SO2的转化率为( B )
A.等于p% B.大于p% C.小于p% D.无法判定
【例10】在相同温度下,有相同体积的甲、乙两容器,甲容器中充入1g N2和1g H2,乙容器中充入2g N2和2g H2。下列叙述中,错误的是( BD )
A.化学反应速率:乙>甲 B.平衡后N2的浓度:乙>甲
C.H2的转化率:乙>甲 D.平衡混合气中H2的体积分数:乙>甲
题型七:已知两个可逆反应
【例11】在一个容器固定的反应器中,有一可左右滑动的密闭隔板,两侧分别进行如图所示的可逆反应。各物质的起始加入量如下:A、B和C均为4.0mol,D为6.5mol,F为2.0mol,设E为xmol,当x在一定范围内变化时,均可以通过调节反应器的温度,使两侧反应都达到平衡,并且隔板恰好处于反应器正中位置。请填写以下空白:
|
A(g) B(g) 2C(g) D(g) 2E(g) 2F(g) |
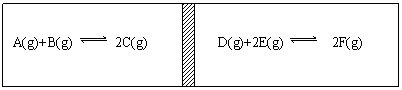 |
⑴若x=4.5,则右侧反应在起始时向 正反应 (填“正反应“或”逆反应“)方向进行。欲使起始反应维持向该方向进行,则x的最大取值应小于 7 。
⑵若x分别为4.5和5.0,则在这两种情况下,当反应达平衡时,A的物质的量是否相等?(填“相等”、“不相等”或“不能确定”)。其理由是: 不相等 。
【方法点拨】当已知两个可逆反应时,应着力去找两平衡间的关系,然后再去计算。
【巩固练习】
1.反应4NH3(g) 5O2(g) ![]() 4NO(g) 6H2O(g)在5L的密闭容器中进行,半分钟后NO的物质的量增加了0.3mol,则此反应的平均速率
4NO(g) 6H2O(g)在5L的密闭容器中进行,半分钟后NO的物质的量增加了0.3mol,则此反应的平均速率 ![]() 为
为
A. ![]() B.
B. ![]()
C. ![]() D.
D. ![]()
2.把下列四种X溶液分别加入四个盛有10mL 2mol/L盐酸的烧杯中,均加水稀释到50mL,此时X与盐酸和缓地进行反应。其中反应速率最大的是
A.20mL 3mol/L的X溶液 B.20mL 2mol/L的X溶液
C.10mL 4mol/L的X溶液 D.10mL 2mol/L的X溶液
3.将固体NH4Br置于密闭容器中,在某温度下,发生下列可逆反应:
NH4Br(s) ![]() NH3(g)+HBr(g) 2HBr(g)
NH3(g)+HBr(g) 2HBr(g) ![]() Br2(g)+H2(g)
Br2(g)+H2(g)
2min后,测得c(H2)=0.5mol/L,c(HBr)=4mol/L,若上述反应速率用 ![]() (NH3)表示,下列反应速率正确的是
(NH3)表示,下列反应速率正确的是
A.0.5mol/(L·min) B.2.5 mol/(L·min)
C.2 mol/(L·min) D.5 mol/(L·min)
4.在一定温度下的固定容积的密闭容器中,当下列物理量不再变化时,表明反应:A(s)+2B(g) ![]() C(g)+D(g)已达平衡的是
C(g)+D(g)已达平衡的是
A.混合气体的压强 B.混合气体的密度
C.B的物质的量浓度 D.气体的总物质的量
5.在温度不变下,在恒压容器a与恒容容器b中,分别充入体积比为1∶3的N2和H2。若开始时两容器的体积相等,且在相同条件下达到平衡时,两容器中N2的转化率应当是
A.a中大 B.b中大 C.a、b中一样大 D.无法判定
6.恒温条件下,将NO2装入带活塞的密闭容器中,当反应2NO2(g) ![]() N2O4(g)达到平衡后,慢慢压缩气体体积,下列叙述正确的是
N2O4(g)达到平衡后,慢慢压缩气体体积,下列叙述正确的是
A.若体积减小一半,则压强为原来的两倍
B.平衡向右移动,混合气体颜色一定会变浅
C.若体积减小一半,压强增大,但小于原来的两倍
D.平衡向右移动,混合气体密度增大
7.在一定温度下,容器中加入CO和H2O(g)各1mol,发生反应:
CO+H2O ![]() CO2+H2,达到平衡时生成0.7mol的CO2,若其他条件不变,一开始就加入4mol H2O(g),则达到平衡可能生成的CO2是
CO2+H2,达到平衡时生成0.7mol的CO2,若其他条件不变,一开始就加入4mol H2O(g),则达到平衡可能生成的CO2是
A.0.6mol B.0.95mol C.1mol D.1.5mol
8.可逆反应A(g)+B ![]() C(g)+D 达到平衡时,下列说法不正确的是
C(g)+D 达到平衡时,下列说法不正确的是
A.若增大A的浓度,平衡体系颜色加深,D不一定是有颜色的气体
B.增大压强,平衡不移动,说明B、D必定是气体
C.升高温度,C的百分含量减少,说明正反应是放热反应
D.若B是气体,增大A的浓度会使B的转化率增大
9.在一密闭容器中充入1mol NO2,建立如下平衡:2NO2 ![]() N2O4,此时NO2的转化率为x%,在其他不变的情况下,再充入1mol NO2,待新平衡建立时测得NO2的转化率为y%,则下列大小关系正确的是
N2O4,此时NO2的转化率为x%,在其他不变的情况下,再充入1mol NO2,待新平衡建立时测得NO2的转化率为y%,则下列大小关系正确的是
A.x>y B.x=y C.x<y D.不能确定
10.将2molSO2和2molSO3气体混合于容积一定的密闭容器中,在一定条件下发生反应:2SO2+O2 ![]() 2SO3,达平衡时SO3为n mol。在相同温度下,按下列配比在该容器中放入起始物质,达平衡时,SO3的物质的量将大于n mol的是
2SO3,达平衡时SO3为n mol。在相同温度下,按下列配比在该容器中放入起始物质,达平衡时,SO3的物质的量将大于n mol的是
A.2molSO2和1molO2
B.2molSO2、1molO2和2molSO3
C.4molSO2和1molO2
D.3molSO2、1molO2和1molSO3
11.在四个同样密闭容器中发生反应:A(g)+3B(g) ![]() 2C(g),在同一时间内测得容器内的反应速率:甲为:
2C(g),在同一时间内测得容器内的反应速率:甲为: ![]() (A)=3 mol/(L·min);乙为
(A)=3 mol/(L·min);乙为 ![]() (B)=4.5 mol/(L·min);丙为
(B)=4.5 mol/(L·min);丙为 ![]() (C)=4 mol/(L·min);丁为
(C)=4 mol/(L·min);丁为 ![]() (A)=0.75mol/(L·s)。若其它条件相同,温度不同,则温度由低到高的顺序是___________________。
(A)=0.75mol/(L·s)。若其它条件相同,温度不同,则温度由低到高的顺序是___________________。
12.一定温度下,在一个固定容积的密闭容器中,可逆反应:A(g)+2B(g) ![]() C(g)达到平衡时,
C(g)达到平衡时, ![]() (A)=2mol·L-1,
(A)=2mol·L-1, ![]() (B)=7mol·L-1,
(B)=7mol·L-1, ![]() (C)=3mol·L-1。试确定B的起始浓度
(C)=3mol·L-1。试确定B的起始浓度 ![]() (B)的取值范围是______________;若往容器中继续注入一定量的氦气(不参加反应),足够长的时间后,体系中B的物质的量浓度_________(填“增大”、“减小”或“不变”,下同),混合气体的密度_________。
(B)的取值范围是______________;若往容器中继续注入一定量的氦气(不参加反应),足够长的时间后,体系中B的物质的量浓度_________(填“增大”、“减小”或“不变”,下同),混合气体的密度_________。
13.在一定条件下,x A+y B ![]() z C的反应达到平衡。
z C的反应达到平衡。
(1)已知A、B、C都是气体,在减压后平衡向逆反应方向移动,则x、y、z之间的关系是__________________;
(2)已知C是气体,且x+y=z,在增大压强时,假如平衡发生移动,则平衡一定向_____________移动;
(3)已知B、C是气体,当其他条件不变,增大A的物质的量时,平衡不发生移动,则A是_____________态物质。
(4)若加热后C的质量分数减少,则正反应是_________(填“放热”或“吸热” )反应。
14.有两只密闭容器A和B。A容器有一个可以移动的活塞能使容器内保持恒压,B容器能保持恒容。起始时向这两个容器中分别充入等物质的量的体积比为2∶1的SO2和O2的混合气体,并使A和B容积相等(如下图所示)。在保持400℃的条件下使之发生如下反应:2SO2+O2 ![]() 2SO3。试填写下列空格:
2SO3。试填写下列空格:
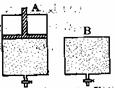
(1)A容器达到平衡时所需的时间比B容器__________;平衡时A容器中SO2的转化率比B容器_______;
(2)达到(1)所述平衡后,若向两容器中通入数量不多的等物质的量的氩气,A容器中化学平衡_________移动,B容器中化学平衡__________;
(3)达到(1)所述平衡后,若向两容器中通入等物质的量的原反应气体,达到平衡时,A容器的混合气体中SO3的体积分数_________(填“增大”、“减小”或“不变”,下同);B容器的混合气体中SO3的体积分数_________。
【答案】
1.D 2.A 3.B 4.BC 5.A 6.CD 7.B 8.B 9.C 10.BD
11.丁乙丙甲(提示:温度越高,化学反应速率越快)。
12.3mol·L-1~13mol·L-1;不变;增大。
13.(1)x+y>z;(2)逆反应方向;(3)固态或液态;(4)放热。
14.(1)短;大;(2)向逆反应方向;不移动;(3)不变;增大。
