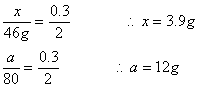|
ИпвЛЩЯбЇЦкЛЏбЇЦкжаВтЪд
ЛЏ бЇ
дзгСПЃКNaЁЊ23 HЁЊ1 CЁЊ12 OЁЊ16 ClЁЊ35.5 MnЁЊ55
вЛЁЂЕЅЯюбЁдёЬтЃК
1ЃЎЯТСаЗДгІЪєгкЗЧбѕЛЏЛЙдЗДгІЕФЪЧ ЃЈ ЃЉ
AЃЎFe2O3 3CO 2Fe 3CO2 BЃЎNH4NO3 N2OЁќ 2H2O
CЃЎ2NaHCO3 Na2CO3 CO2Ёќ H2O DЃЎCuO CO Cu CO2
2ЃЎдкЗДгІ 2KMnO4 K2MnO4 MnO2 O2ЁќжаЃЌбѕЛЏВњЮяЪЧ
AЃЎK2MnO4 BЃЎMnO2 CЃЎO2 DЃЎKMnO4
3ЃЎдкЗДгІ3Cl2 6KOH 5KCl KClO3 3H2OжаЃЌТШЦј ЃЈ ЃЉ
AЃЎжЛБЛбѕЛЏ BЃЎжЛБЛЛЙд
CЃЎМШБЛбѕЛЏгжБЛЛЙд DЃЎМШВЛБЛбѕЛЏгжВЛБЛЛЙд
4ЃЎдкбѕЛЏЛЙдЗДгІ3S 6KOH K2SO3 2K2S 3H2OжаЃЌБЛбѕЛЏгыБЛЛЙдЕФСђдзгЪ§жЎ
БШЮЊ ЃЈ ЃЉ
AЃЎ1ЃК2 BЃЎ2ЃК1 CЃЎ1ЃК1 DЃЎ3ЃК2
5ЃЎдкЪРНчЩЯЪзДЮгУШЫЙЄЗНЗЈКЯГЩСЫвЛжжОпгагыЬьШЛЗжзгЯрЭЌЕФЛЏбЇНсЙЙКЭЭъећЩњЮяЛюадЕФ
КЫЬЧКЫЫсЕФЙњМвЪЧ ЃЈ ЃЉ
AЃЎУРЙњ BЃЎЖэТоЫЙ CЃЎжаЙњ DЃЎЕТЙњ
6ЃЎгУЯТСаЗНЗЈОљПЩжЦЕУбѕЦјЃК
ЃЈ1ЃЉ2KClO3 2KCl 3O2Ёќ ЃЈ2ЃЉ2Na2O2 2H2O 4NaOH O2Ёќ
ЃЈ3ЃЉ2HgO 2Hg O2Ёќ ЃЈ4ЃЉ2KMnO4 K2MnO4 MnO2 O2Ёќ
ШєвЊжЦЕУЯрЭЌжЪСПЕФбѕЦјЃЌЗДгІжаЕчзгзЊвЦЪ§ФПжЎБШЮЊ ЃЈ ЃЉ
AЃЎ3ЃК2ЃК1ЃК4 BЃЎ1ЃК1ЃК1ЃК1 CЃЎ2ЃК1ЃК2ЃК2 DЃЎ1ЃК2ЃК1ЃК1
7ЃЎЯТСаЮяжЪЪєгкЕчНтжЪЕФЪЧ ЃЈ ЃЉ
ЂйNaOH ЂкBaSO4 ЂлCu ЂмесЬЧ ЂнSO2
AЃЎЂйЂк BЃЎЂйЂкЂн CЃЎЂлЂм DЃЎЂйЂн
8ЃЎЯТСаЮяжЪжаЃЌЪєЧПЕчНтжЪЕФЪЧ ЃЈ ЃЉ
AЃЎCH3COOH BЃЎCu(OH)2 CЃЎH2O DЃЎBaSO4
9ЃЎЯТСаРызгЗНГЬЪНДэЮѓЕФЪЧ ЃЈ ЃЉ
AЃЎСђЫсгыЧтбѕЛЏБЕШмвКЗДгІ H OHЃ=H2O
BЃЎЯѕЫсгыЧтбѕЛЏФЦШмвКЗДгІ H OHЃ=H2O
CЃЎАБЫЎгыДзЫсШмвКЗДгІ CH3COOH NH3ЁЄH2O=CH3COOЃ NH 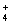 H2O H2O
DЃЎNa2CO3ШмвКзуСПЕФбЮЫсЗДгІ CO 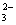 2H =CO2Ёќ H2O 2H =CO2Ёќ H2O
10ЃЎЯТСаИїзщРызгдкШмвКжаПЩвдДѓСПЙВДцЕФЪЧ ЃЈ ЃЉ
AЃЎH ЁЂ CO 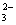 ЁЂSO ЁЂSO 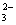 ЁЂSO ЁЂSO 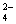 BЃЎCu2 ЁЂClЃЁЂNO BЃЎCu2 ЁЂClЃЁЂNO 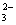 ЁЂCO ЁЂCO 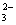
CЃЎMg2 ЁЂH ЁЂSO 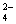 ЁЂClЃ DЃЎMg2 ЁЂOHЃЁЂCO ЁЂClЃ DЃЎMg2 ЁЂOHЃЁЂCO 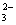 ЁЂH ЁЂH
11ЃЎЯТСаИїзщжаСНжжЮяжЪдкШмвКжаЕФЗДгІЃЌПЩгУЭЌвЛРызгЗНГЬЪНБэЪОЕФЪЧ ЃЈ ЃЉ
AЃЎCu(OH)2 HCl;Cu(OH)2 CH3COOH
BЃЎNaHCO3 H2SO4;Na2CO3 HCl
CЃЎNaHCO3 NaOH;Ca(HCO3)2 NaOH
DЃЎBaCl2 H2SO4;Ba(OH)2 Na2SO4
12ЃЎЯђБЅКЭЕФЪЏЛвЫЎШмвКжаВЛЖЯЭЈШыЖўбѕЛЏЬМЃЌЦфШмвКЕФЕМЕчадЕФБфЛЏЪЧ ЃЈ ЃЉ
AЃЎгЩШѕБфЧП BЃЎгЩЧПБфШѕ
CЃЎгЩЧПБфШѕдйБфЧП DЃЎгЩШѕБфЧПдйБфШѕ
13ЃЎNa ЕФбѕЛЏадКЭRb ЕФбѕЛЏад ЃЈ ЃЉ
AЃЎаЁгк BЃЎДѓгк CЃЎЕШгк DЃЎВЛФмПЯЖЈ
14ЃЎ1.06gNa2CO3КЭ0.84NaHCO3ЗжБ№гызуСПбЮЫсЗДгІЃЌЗХГіЖўбѕЛЏЬМЕФжЪСП ЃЈ ЃЉ
AЃЎаЁгк BЃЎДѓгк CЃЎЕШгк DЃЎВЛФмПЯЖЈ
15ЃЎЙигкяЈМАЦфЛЏКЯЮяЕФаджЪЕФЭЦВте§ШЗЕФЪЧ ЃЈ ЃЉ
AЃЎяЈИњРфЫЎЗДгІБШМиИќОчСв
BЃЎяЈЕФШлЕуБШФЦИп
CЃЎRb2CO3ЪмШШвзЗжНтЃЌЩњГЩRb2OКЭCO2
DЃЎяЈдкбѕЦјжаШМЩеЩњГЩRb2O
16ЃЎЯТСаЗДгІжаЃЌNa2O2жЛБэЯжЧПбѕЛЏадЕФЪЧ ЃЈ ЃЉ
AЃЎ2Na2O2 2CO2 2Na2CO3 O2
BЃЎNa2O2 MnO2= Na2MnO4
CЃЎ5 Na2O2 2M2nO  16H =10Na 2Mn2 5O2Ёќ 8H2O 16H =10Na 2Mn2 5O2Ёќ 8H2O
DЃЎ2Na2O2 2H2SO4=2Na2SO4 2H2O O2Ёќ
17ЃЎЯТСаЖдНјаабцЩЋЗДгІЕФЪЕбщВйзїзЂвтЪТЯюЕФЫЕУїе§ШЗЕФЪЧ ЃЈ ЃЉ
ЂйМиЕФЛ№бцЕФбеЩЋвЊЭИЙ§РЖЩЋюмВЃСЇЙлВь ЂкЯШзЦЩеВЌЫПЕНЛ№бцЮоЩЋЪБЃЌдйеКБЛМьЮяжЪ
ЂлУПДЮЪЕбщКѓвЊНЋВЌЫПеКбЮЫсзЦЩеИЩОЛ ЂмЪЕбщЪБзюКУбЁдёБОЩэбеЩЋНЯЧПЕФЛ№бц
ЂнУЛгаВЌЫППЩгУЮоатЬњЫПДњЬц
AЃЎНіЂлВЛе§ШЗ BЃЎНіЂмВЛе§ШЗ
CЃЎНіЂйЂмВЛе§ШЗ DЃЎШЋВПе§ШЗ
18ЃЎЯТСаЙигкNaHCO3КЭNa2CO3ЕФаджЪЕФа№ЪіВЛе§ШЗЕФЪЧ ЃЈ ЃЉ
AЃЎЯђБЅКЭNa2CO3ШмвКжаЭЈШызуСПCO2ЦјЬхгаАзЩЋГСЕэЩњГЩ
BЃЎЯђШШЕФNaOHШмвКЭЈШызуСПCO2ЦјЬхПЩжЦЕУNaHCO3
CЃЎМгШыГЮЧхЪЏЛвЫЎЖМгаАзЩЋГСЕэЩњГЩ
DЃЎNa2CO3ЪЧжЮСЦЮИЫсЙ§ЖрЕФвЛжжвЉМС
19ЃЎАб6.2gNa2OШмгк93.8gЫЎжаЃЌАб4.6gН№ЪєФЦШмгк 95.6gЫЎжаЃЌАб7.8gNa2O2Шмгк93.8g
ЫЎжаЃЌАб8gNaOHШмгк92gЫЎжаЃЌЫљЕУЕНЕФШмвКЕФжЪСПЗжЪ§ЮЊ ЃЈ ЃЉ
AЃЎЖМЪЧ8% BЃЎЗжБ№ЮЊ8%ЃЌ8%ЃЌ7%ЃЌ10%
CЃЎЖМЪЧ9% DЃЎЗжБ№ЮЊ6%ЃЌ7%ЃЌ8%ЃЌ9%
20ЃЎгаШ§ИібѕЛЏЛЙдЗДгІЃК
ЃЈ1ЃЉ2FeCl3 2KI 2FeCl2 2KCl I2
ЃЈ2ЃЉ2FeCl2 Cl2 2FeCl3
ЃЈ3ЃЉ2KMnO4 16HCl 2KCl 2MnCl2 5Cl2Ёќ 8H2O
ФГШмвКжагаFe2 ЁЂIЃКЭClЃЙВДцЃЌвЊбѕЛЏГ§ШЅIЃЃЌЖјВЛгАЯьFe2 КЭClЃЃЌПЩМгШыЕФЪдМСЪЧ
ЃЈ ЃЉ
AЃЎCl2 BЃЎKMnO4 CЃЎFeCl3 DЃЎHCl
ЖўЁЂЗЧбЁдёЬтЃК
21ЃЎдкБъГі2KMnO4 16HCl 2KCl 2MnCl2 5Cl2Ёќ 8H2OЗДгІжаЕчзгЕУЪЇЕФЗНЯђЪ§ФПЃЌ
ИУЗДгІбѕЛЏМСЪЧ ЃЌбѕЛЏВњЮяЪЧ ЃЌбѕЛЏВњЮягыЛЙдВњЮяЕФжЪСПжЎБШ
ЮЊ ЃЌЕчзгзЊвЦЕФзмЪ§ЮЊ ЃЌШєга7.3gHClБЛбѕЛЏЃЌВњЩњCl2ЕФ
жЪСПЮЊ gЁЃ
22ЃЎЃЈ1ЃЉаДГіЯТСаЗДгІЕФРызгЗНГЬЪНЁЃ
ЃЈaЃЉСђЫсЭШмвККЭЧтбѕЛЏБЕШмвКЕФЗДгІ ЁЃ
ЃЈbЃЉбѕЛЏУОгыЯЁСђЫсЗДгІ ЁЃ
ЃЈcЃЉЬМЫсЧтФЦШмвКгыЯЁСђЫсЗДгІ ЁЃ
ЃЈ2ЃЉаДГівЛР§ЗћКЯЯТСаРызгЗНГЬЪНЕФЛЏбЇЗДгІЗНГЬЪНЁЃ
ЃЈaЃЉCa2 CO 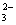 =CaCO3Ё§ ЁЃ =CaCO3Ё§ ЁЃ
ЃЈbЃЉNH 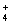 OHЃ=NH3Ёќ H2O ЁЃ OHЃ=NH3Ёќ H2O ЁЃ
23ЃЎФГгаЩЋЕчНтжЪШмвКжаЃЌПЩФмДѓСПДцдкгаAg ЁЂH ЁЂCu2 ЁЂCO 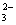 ЁЂOHЃЁЂClЃЕШРызгЃЌФу ЁЂOHЃЁЂClЃЕШРызгЃЌФу
ШЯЮЊЃКвЛЖЈгаЕФРызгЪЧ ЃЌвЛЖЈУЛгаЕФРызгЪЧ ЃЌЛЙашНјвЛВНШЗШЯЕФРызгЪЧ
ЁЃ
24ЃЎвбжЊSO2ФмБЛCl2бѕЛЏГЩ 6МлЕФSO3ЃЌЖјТШдЊЫиБОЩэБЛЛЙдГЩЃ1МлЕФТШЁЃЪдаДГіCl2
НЋSO2ЕФЫЎШмвКбѕЛЏГЩСђЫсЕФЛЏбЇЗНГЬЪНКЭРызгЗНГЬЪН
ЁЃ
25ЃЎЛЏЪЏШМСЯжївЊАќРЈ ЕШЃЌЪєгкЗЧдйЩњФмдДЁЃ
ШМСЯГфЗжШМЩеЕФЬѕМўЃКЃЈ1ЃЉвЊгазуЙЛЖрЕФ ЃЌЃЈ2ЃЉШМСЯКЭПеЦјвЊгазуЙЛДѓЕФ ЁЃ
ШМСЯШМЩеВЛГфЗжЪБЃЌВЛЕЋВњЩњЕФШШСП ЃЌЖјЧвЛЙЛсВњЩњДѓСПЕФ ЕШгаКІЦјЬхЃЌЮЊЬсИпШМСЯЕФРћгУТЪЃЌЪЙжЎШМЩеЭъШЋЃЌЙЄвЕЩЯГЃашвЊЙЬЬхШМСЯ ЃЌЛђНЋвКЬхШМСЯ ЃЌвддіДѓШМЩегыПеЦјЕФНгДЅУцЛ§ЃЌЬсИпШМЩеаЇТЪЁЃ
УКЬПжБНгШМЩеВЛНіВњЩњДѓСПбЬГОЃЌЖјЧвУК жаКЌгаЕФСђдЊЫидкШМЩеЪБЛсЩњГЩ ЃЌетЪЧЕМжТаЮГЩЫсгъЕФжївЊдвђжЎвЛЁЃ
26ЃЎAЁЂBЁЂCШ§жжЙЬЬхЮяжЪЕФбцЩЋЗДгІЮЊЛЦЩЋЃЌЗжБ№ИњЫЎЗЂЩњЛЏбЇЗДгІОљЕУЮяжЪDЕФШмвКЃЛ
AИњЫЎЗДгІЛЙгаO2ЩњГЩЃЌBИњЫЎЗДгІЛЙгаH2ЩњГЩЃЌCИњЫЎЗДгІЪЧЛЏКЯЗДгІЁЃ
ЃЈ1ЃЉAЮЊ ЃЌBЮЊ ЃЌCЮЊ ЃЌDЮЊ ЁЃ
ЃЈ2ЃЉгЩBЩњГЩAЕФЛЏбЇЗНГЬЪН ЁЃ
ЃЈ3ЃЉгЩAЩњГЩDЕФРызгЗНГЬЪН ЁЃ
ЃЈ4ЃЉгЩBЩњГЩDЕФРызгЗНГЬЪН ЁЃ
27ЃЎгавЛПщТѓУцБЛбѕЛЏЮЊбѕЛЏФЦЕФН№ЪєФЦЃЌЦфжЪСПЪЧ16.2gЃЌНЋЫќЭЖШыЕН150gЫЎжаЃЌЭъШЋЗД
гІКѓЪеМЏЕН0.3gЧтЦјЁЃЪдМЦЫуЃК
ЃЈ1ЃЉЮДБЛбѕЛЏЕФН№ЪєФЦЕФжЪСПЁЃ
ЃЈ2ЃЉБЛбѕЛЏЮЊбѕЛЏФЦЕФН№ЪєФЦЕФжЪСПЁЃ
ЃЈ3ЃЉЗДгІКѓЫљЕУШмвКЕФШмжЪСПЗжЪ§ЁЃ
28ЃЎМгШШ432gNa2CO3 КЭNaHCO3ЕФЛьКЯЮяжСжЪСПВЛдйБфЛЏЃЌЪЃгрЙЬЬхЕФжЪСПЮЊ339g ЁЃЮЪ
дЛьКЯЮяжаNa2CO3ЕФжЪСПЗжЪ§ЪЧЖрЩйЃП
ИНМгЬтЃК
29ЃЎЯжгавЛЖЈСПКЌгаNa2OдгжЪЕФNa2O2ЪдбљЁЃЧыДгЯТЭМжабЁгУЪЪЕБЕФЪЕбщзАжУЃЌЩшМЦвЛИізюМђЕЅЕФЪЕбщЃЌВтЖЈNa2O2ЪдбљЕФДПЖШЃЈПЩЙЉбЁгУЕФЗДгІЮяжЛгаNa2CO3ЙЬЬхЃЌ6ФІ/Щ§бЮЫсКЭеєСѓЫЎЃЉЁЃ
ЧыЬюаДЯТСаПеАзЃК
ЃЈ1ЃЉаДГідкЪЕбщжаNa2O2КЭNa2OЗжБ№ЗЂЩњЗДгІЕФЛЏбЇЗНГЬЪН
ЁЃ
ЃЈ2ЃЉгІбЁгУЕФзАжУЪЧЃЈжЛвЊЧѓаДГіЭМжазАжУЕФБъКХЃЉ ЁЃ
ЃЈ3ЃЉЫљбЁгУзАжУЕФСЌНгЫГађгІЪЧЃЈЬюИїНгПкЕФзжФИЃЛСЌНгНКЙмЪЁТдЃЉ
ЁЃ
30ЃЎвЛЖЈжЪСПЕФаЁЫеДђЗлФЉОГфЗжМгШШКѓЃЌжЪСПБШдРДМѕЩй3.1gЃЌЪЃгрЮяжЪСПЮЊa gЃЌЯрЭЌжЪ
СПЕФаЁЫеДђКЭвЛЖЈжЪСПЕФНсОЇЫеДђЃЈNa2CO3ЁЄXH2OЃЉЕФЛьКЯЮяОГфЗжМгШШКѓЃЌжЪСПБШ
дРДМѕЩй10.3gЃЌЪЃгрЕФжЪСПЮЊb gЃЌгжжЊa:b=1:2ЃЌЪдЧѓЃК
ЃЈ1ЃЉдРДаЁЫеДђКЭНсОЇЫеДђЕФжЪСПЁЃ
ЃЈ2ЃЉНсОЇЫеДђжаXЕФжЕЁЃ
ИпвЛЛЏбЇЩЯбЇЦкЦкжаВЮПМД№АИ
вЛЁЂбЁдёЬт |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 | |
C |
C |
C |
A |
C |
C |
A |
D |
A |
C | |
11 |
12 |
13 |
14 |
15 |
16 |
17 |
18 |
19 |
20 | |
D |
C |
B |
C |
A |
B |
B |
D |
A |
C | |