一、选择题(每题6分,共180分)
1.分析发现,某陨石中含有半衰期极短的镁的一种放射性同位素28Mg,该同位素的原子核内的中子数是 ( )
A.12 B.14 C.16 D.18
2.下列说法正确的是 ( )
A.常温常压下,只有一种元素的单质呈液态
B.周期表中所有元素都有从自然界中发现的
C.过渡元素不全是金属元素
D.常温常压下,气态单质的分子都是由非金属元素的原子形成的
3.下列单质中,最容易跟氢气发生反应的是 ( )
A.O2 B.N2 C.F2 D.Cl2
4.NA代表阿伏加德常数,下列说法正确的是 ( )
A.在同温同压时,相同体积的任何气体单质所含的原子数目相同
B.2g氢气所含原子数目为NA
C.在常温常压下,11.2L氮气所含的原子数目为NA
D.17g氨气所含电子数目为10NA
5.近期,北京大学的两位教授率先发现人体心肺血管中存在微量硫化氢,它对调节心血管功能具有重要作用。下列叙述正确的是( )
A.硫化氢分子很稳定,受热难分解
B.硫化氢分子中所有原子的最外电子层都达到8电子结构
C.将硫化氢通人溴水,溴水褪色
D.硫化氢是电解质,其电离方程式是H2S =2H ++ S 2-
6.某校学生用化学知识解决生活中的问题,下列家庭小实验不合理的是( )
A.用食醋除去暖水瓶中的薄层水垢
B.用米汤检验含碘盐中的碘酸钾(KIO3)
C.用食用碱(Na2CO3)溶液洗涤餐具上的油污
D.用灼烧并闻气味的方法区别纯棉织物和纯毛织物
7.下列叙述中指定粒子的数目大于6.02×1023的是( )
A.2 g重水(D20,D为21 H)中含有的中子数
B.0.1 mol F-中含有的电子数
C.标准状况下,11.2 L N2和NO混合气体中的原子数
D.1 L 1mol·L - 1Na2SO4溶液中的Na+离子数
8.下列各组试剂在溶液中反应,当两种试剂的量发生改变时,不能用同一离子方程式表示的是( )
A.氯化镁、氢氧化钠 B.硫酸钠、氢氧化钡
C.氯化铝、氨水 D.溴化亚铁、氯水
9.甲、乙两元素原子的L层电子数都是其它层电子总数的2倍。下列推断正确的是( )
A.甲与乙处于同一周期
B.甲与乙处于同一主族
C.甲与乙的单质都是原子晶体
D.甲与乙的原子序数之和为偶数
10.相等物质的量的KClO3分别发生下述反应:( )
①有MnO2催化剂存在时,受热分解得到氧气;
②若不使用催化剂,加热至470℃左右,得到KClO4 (高氯酸钾)和KCl。
下列关于①和②的说法不正确的是
A.都属于氧化还原反应
B.发生还原反应的元素相同
C.发生氧化反应的元素不同
D.生成KCl的物质的量相同
11.现有以下几种措施:①对燃烧煤时产生的尾气进行除硫处理,②少用原煤做燃料,③燃煤时鼓入足量空气、,④开发清洁能源。其中能减少酸雨产生的措施的( )
A.①②③ B.②③④ C.①②④ D.①③④
12.同一主族的两种元素的原子序数之差不可能是( )
A.16 B.26 C.36 D.46
13.向0.1mol·L-1NaOH溶液中通入过量CO2后,溶液中存在的主要离子是( )
A.Na+、CO B.Na+、HCO3- C.HCO3-、CO D.Na+、OH-
14.已知KH和H2O反应生成H2和KOH,反应中1molKH( )
A.失去1mol电子 B.得到1mol电子 C.失去2mol电子 D.没有电子得失
15.在273K和100kPa的条件下,将2.00g氦气、1.40g氮气和1.60g氧气混合,该混合气体的体积( )
A.6.72L B.7.84L C.10.08L D.13.44L
16.下列分子中所有原子都满足最外层为8电子结构的是( )
A.BF3 B.H2O C.SiCl4 D.PCl5
17.等物质的量的主族金属A、B、C分别与足量的稀盐酸反应,所得氢气的体积依次为VA、VB、VC,已知VB=2VC,且VA=VB+VC,则在C的生成物中,该金属元素的化合价为( )
A.+1 B.+2 C.+3 D.+4
18.已知Q与R的摩尔质量之比为9:22,在反应X+2Y=2Q+R中,当1.6g X与Y完全反应后,生成4.4g R,则参与反应的Y和生成物Q的质量之比为( )
A.46 : 9 B.32 : 9 C.23 : 9 D.16 : 9
19.下列说法中正确的是( )
A.非金属元素呈现的最高化合价不超过该元素原子的最外层电子数
B.非金属元素呈现的最低化合价,其绝对值等于该元素原子的最外层电子数
C.最外层有2个电子的原子都是金属原子
D.最外层有5个电子的原子都是非金属原子
20.在pH=1的溶液中,可以大量共存的离子是( )
A.K+、Na+、SO42—、S2O32— B.NH4+、Mg2+、SO42—、Cl—
C.Na+、K+、HCO3—、Cl— D.K+、Na+、AlO2—、NO3—
21、据报道,科学家已成功合成了少量N4,有关N4的说法正确的是( )
A、N4是N2的同素异形体 B、N4是N2的同分异构体
C、相同质量的N4和N2所含原子个数比为1:2 D、N4的摩尔质量是56g
22、设阿伏加德常数为NA。则下列说法正确的是( )
A、 常温常压下,11.2L甲烷中含有的氢原子数为2NA
B、 标准状况下,0.3mol二氧化硫中含有氧原子数为0.3NA
C、 常温下,2.7g铝与足量的盐酸反应,失去的电子数为0.3NA
D、常温下,1L 0.1mol/L MgCl2溶液中含Mg2+数为0.2NA
23、浓硫酸和2mol/L的稀硫酸,在实验室中敞口放置。它们的质量和放置天数的关系如右图,分析a、b曲线变化的原因是( )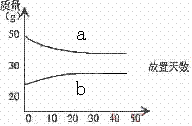

A、a升华、b冷凝 B、a挥发、b吸水
C、a蒸发、b潮解 D、a冷凝、b吸水
24、欲使0.1mol/L的NaHCO3溶液中c(H+)、c(CO32¯)、c(HCO3¯)都减少,其方法是( )
A、通入二氧化碳气体 B、加入氢氧化钠固体
C、通入氯化氢气体 D、加入饱和石灰水溶液
25、下列离子中,电子数大于质子数且质子数大于中子数的是( )
A、D3O+ B、Li+ C、OD¯ D、OH¯
26、含8.0g NaOH的溶液中通入一定量H2S后,将得到的溶液小心蒸干,称得无水物7.9g,则该无水物中一定含有的物质是( )
A、Na2S B、NaHS
C、Na2S和NaHS D、NaOH和NaHS
27、在下列元素中,不属于主族元素的是( )
A 磷 B 铁 C 钙 D 碘
28、在下列生成二氧化硫的反应中,反应物中的含硫物质被氧化的是( )
A 硫在空气中燃烧 B 铜片与浓硫酸共热
C 红热的木炭与浓硫酸反应 D 亚硫酸钠与稀硫酸反应
29、下列有关钠的叙述中,错误的是( )
A 钠的还原性很强,可以用来冶炼金属钛、锆、铌等
B 钠的化学性质非常活泼,钠元素只能以化合态存在于自然界
C 钠是一种灰黑色的固体
D 钠的质地软,可用小刀切割
30、能用离子方程式H++OH-=H2O表示的反应是( )
A 稀醋酸和稀氨水反应 B 稀硫酸和烧碱溶液反应
C 稀盐酸和氢氧化铜反应 D 稀硫酸和氢氧化钡溶液反应
二、非选择题(共120分)
31、(15分)A、B、C、D、E 5瓶透明溶液,分别是HCl、BaCl2、NaHSO4、Na2CO3、AgNO3中的一种。
①A与B反应有气体生成 ②B与C反应有沉淀生成
③C与D反应有沉淀生成 ④D与E反应有沉淀生成
⑤A与E反应有气体生成 ⑥在②和③的反应中生成的沉淀是同一种物质
请填空:
(1)在②和③的反应中,生成的沉淀物质的化学式(分子式)是 。
(2)A是 ,B是 ,C是 ,
D是 ,E是 。
(3)A与E反应的离子方程式是 。
32、(21分)化学活动课上,三组学生分别用图示甲、乙两装置,探究“NaHCO3,和Na2CO3,与稀盐酸的反应”,按表中的试剂用量,在相同条件下,将两个气球中的固体粉末同时倒入试管中(装置的气密性已检查)。 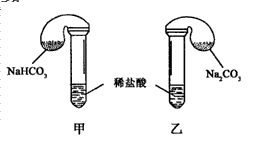

 (1)各取适量固体试剂分别加入6支试管中,加入适量蒸馏水,振荡试管,观察到的现象是
(1)各取适量固体试剂分别加入6支试管中,加入适量蒸馏水,振荡试管,观察到的现象是 被检出的物质的化学式(分子式)是
(2)分别取未检出的溶液,往其中加入上述已检出的溶液,观察到的现象和相应的离子方程式是1支试管中有白色沉淀生成 ,2支试管中有蓝色沉生成
被检出的物质的化学式(分子式)是
(3)鉴别余下未检出物质的方法和观察到的现象是(i)
(ii)
34、(15分)
已知某纯碱试样中含有NaCl杂质,为测定试样中纯碱的质量分数,可用下图中的装置进行实验。 
主要步骤如下:
①按图组装仪器,并检查装置的气密性
②将ag试样放入锥形瓶中,加适量蒸馏水溶解,得到试样溶液
③称量盛有碱石灰的U型管的质量,得到bg
④从分液漏斗滴入6mol·L-1的硫酸,直到不再产生气体时为止
⑤从导管A处缓缓鼓入一定量的空气
⑥再次称量盛有碱石灰的U型管的质量,得到cg
⑦重复步骤⑤和⑥的操作,直到U型管的质量基本不变,为dg
请填空和回答问题:
(1)在用托盘天平称量样品时,如果天平的指针向左偏转,说明
(2)装置中干燥管B的作用是
(3)如果将分液漏斗中的疏酸接成浓度相同的盐酸,测试的结果 (填偏高、偏低可不变)
(4)步骤⑤的目的是
(5)步骤⑦的目的是
(6)该试样中纯碱的质量分数的计算式为
(7)还可以用其他实验方法测定试样中纯碱的质量分数。请简述一种不同的实验方法。
35、(本题共8分)某一反应体系有反应物和生成物共五种物质:
O2、H2CrO4、Cr(OH)3、H2O、H2O2
已知该反应中H2O2只发生如下过程:H2O2→ O2
(1)该反应中的还原剂是 。
(2)该反应中,发生还原反应的过程是 → 。
(3)写出该反应的化学方程式,并标出电子转移的方向和数目
。
(4)如反应转移了0.3mol电子,则产生的气体在标准状况下体积为 。
36、(本题共7分)过氧化钙是一种安全无毒的物质,带有数量不等的结晶水,通常还含有部分CaO。
(1)称取0.542g过氧化钙样品,灼热时发生如下反应:
2CaO2·XH2O 2CaO + O2↑ + 2XH2O,得到的O2在标准状况下体积为67.2mL,该样品中CaO2的物质的量为 。
(2)另取同一样品0.542g,溶于适量的稀盐酸中,然后加入足量的Na2CO3溶液,将溶液中Ca2+全部转化为CaCO3沉淀,得到干燥的CaCO3 0.70g。
① 试计算样品中CaO的质量。
② 试计算样品中CaO2·XH2O的X值。
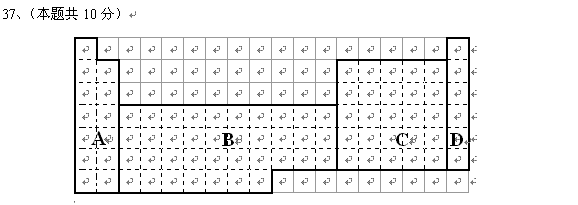
(1)在上面元素周期表中全部是金属元素的区域为
(a) A (b) B
(c) C (d) D
(2)有人认为形成化合物最多的元素不是IVA族的碳元素,而是另一种短周期元素,请你根据学过的化学知识判断这一元素是 。
(3)现有甲、乙两种短周期元素,室温下,甲元素单质在冷的浓硫酸或空气中,表面都生成致密的氧化膜,乙元素原子核外M电子层与K电子层上的电子数相等。① 用元素符号将甲、乙两元素填写在上面元素周期表中对应的位置。② 甲、乙两元素相比较,金属性较强的是 (填名称),可以验证该结论的实验是 。(a)将在空气中放置已久的这两种元素的块状单质分别放入热水中(b)将这两种元素的单质粉末分别和同浓度的盐酸反应(c)将这两种元素的单质粉末分别和热水作用,并滴入酚酞溶液(d)比较这两种元素的气态氢化物的稳定性38、(8分)某同学拟用氯化钙固体、碳酸钠溶液和稀硝酸等试剂,先制得碳酸钙,最终制得纯净的硝酸钙晶体。(1)写出制取过程中反应的离子方程式:、(2)请帮助该同学完成下列实验操作步骤(不要求回答使用的仪器)①用蒸馏水完全溶解CaCl2后,加入 。②将反应后的混合物过滤,并用适量蒸馏水洗涤沉淀至无Cl-。③加入 ,使沉淀完全溶解。④ ,得到纯净的硝酸钙晶体。39、(16分)下图所涉及的物质均为中学化学中的常见物质,其中C为O2、D为C12、E为Fe单质,其余为化合物。它们存在如下转化关系,反应中生成的水及次要产物均已略去。(1)写出有关物质的名称或化学式:B ,F ,H 。(2)指出MnO2在相关反应中的作用:反应①中是 剂,反应②中是 剂。(3)若反应①是在加热条件下进行,则A是 ;若反应①是在常温条件下进行,则A是 。(4)写出B与MnO2共热获得D的化学方程式 。高一部分化学试题答案一、选择题(每小题只有一个选项符合题意,每小题6分,共180分)
BaSO4↓; Cu2++2OH-Cu(OH)2↓;Cu2++COCuCO3↓;BaCl2;(3)(i)分别取(2)中能产生蓝色沉淀的两种溶液,向其中加入BaCl2溶液,有白色沉淀生成的是Na2CO3溶液,无沉淀生成的是NaOH溶液。 (ii)分别取少量未检出的溶液,往其中加入NaOH溶液,无明显现象的是Na2SO4溶液,有刺激性气味气体产生的是(NH4)2SO4溶液34.(15分)(1)样品重,砝码轻(2)防止空气中的CO2和水气进入U型管中(3)偏高(4)把反应产生的CO2全部导入U型管中(5)判断反应产生的CO2是否全部排出,并被U型管中的碱石灰吸收(6)(7)答案略。35、(本题共8分)(1)H2O2(2)H2CrO4 Cr(OH)3(3)(4)3.36L36、(本题共7分)(1)0.006mol(2)① n(CaO2) = 0.006mol n(Ca2+) = 0.007mol m(CaO) = 0.056g② n(H2O) = 0.003mol X = 1/237、(B)(本题共10分)
(4)MnO2+4HCl(浓) MnCl2+C12↑+2H2O