|
…η±Ψ“≥ΈΣ Ή“≥ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ
ΓΓ ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΦ”»κ ’≤Ί |
|
| ÷–ΈΡ”ρΟϊ: Ι≈Ϋώ÷–Άβ.comΓΓΓΓΓΓΓΓΓΓΓΓ
”ΔΈΡ”ρΟϊΘΚwww.1-123.comΓΓΓΓΓΓΓΓΓΓΖαΗΜ Β”ΟΒΡΫΧ”ΐΫΧ―ßΉ Νœ |
| |
| |
| |
|
|
ΔΌ Ά®Ιΐ…œ ω–≈œΔΚΆ±μ÷–ΒΡ ΐΨίΖ÷ΈωΘΚΈΣ ≤Ο¥ο°‘≠Ή” ß»ΞΚΥΆβΒΎΕΰΗωΒγΉ” ±Υυ–ηΒΡ ΡήΝΩ“Σ‘Ε‘Ε¥σ”Ύ ß»ΞΒΎ“ΜΗωΒγΉ”Υυ–ηΒΡΡήΝΩΘΚ ΓΓΓΓ ΘΜ ΔΎ‘Ύ“ΜΕ®ΧθΦΰœ¬Θ§±μ÷–XΩ…Ρή”κ«βΤχΖ¥”ΠΒΡΜ·―ßΖΫ≥Χ Ϋ « ΓΓ ΘΜ ΔέY‘ΣΥΊ≥ΘΦϊΒΡΜ·ΚœΦέΩ…Ρή «ΓΓΓΓ ΓΓΓΓΓΓΓΓΓΘ 30Θ°ΧζΥαΡΤ(Na2FeO4) «Υ°¥ΠάμΙΐ≥Χ÷– Ι”ΟΒΡ“Μ÷÷–¬–ΆΨΜΥ°ΦΝΘ§Υϋ―θΜ·–‘±»ΗΏΟΧΥαΦΊΗϋ«ΩΘ§±Ψ…μ‘ΎΖ¥”Π÷–±ΜΜΙ‘≠ΈΣFe3 άκΉ”ΓΘ÷Τ»ΓΧζΥαΡΤΒΡ≥Χ ΫΈΣΘΚ Fe(NO3) NaOH Cl2©ΛNa2FeO4 NaNO3 NaCl H2O Θ§‘ρΖ¥”Π÷– ‘ΣΥΊ±Μ―θΜ·ΓΘ
ΈεΓΔΆΤΕœΧβ(±ΨΧβΙ≤1–ΓΧβΘ§Ι≤8Ζ÷) 31Θ°Ρ≥ΜλΚœΈοAΘ§Κ§”–KAl(SO4)2ΓΔAl2O3ΚΆFe2O3Θ§‘Ύ“ΜΕ®ΧθΦΰœ¬Ω… Βœ÷ΆΦΥυ ΨΒΡΈο÷ ÷°ΦδΒΡ±δΜ·ΘΚ Ψί¥Υ≈–ΕœΘΚ
(1)ΙΧΧεBΥυΚ§Έο÷ ΒΡΜ·―ß ΫΈΣ______________ΘΜ (2)ΙΧΧεEΥυΚ§Έο÷ ΒΡΜ·―ß ΫΈΣ______________ΘΜ (3)Ζ¥”ΠΔΌΒΡάκΉ”ΖΫ≥Χ ΫΈΣ____________ ΓΘ ΝυΓΔΦΤΥψΧβ(±ΨΧβΙ≤2–ΓΧβΘ§Ι≤16Ζ÷) 32Θ°ΫΪ50mL 0.1mol/LBaCl2»ή“Κ”κ100mL0.75mol/L H2SO4»ή“ΚΜλΚœΘ§«σΘΚ Θ®1Θ©Ζ¥”Π≤ζ…ζ≥ΝΒμΒΡ÷ ΝΩ «ΓΓΓΓΓΓΓΓΓΓΓΓ gΘΜ(±ΘΝτ2ΈΜ”––ß ΐΉ÷) Θ®2Θ©»τ≤ΜΩΦ¬«»ή“ΚΧεΜΐΒΡ±δΜ·Θ§‘ρΖ¥”ΠΚσ»ή“ΚΒΡCΘ®HΘΪΘ©ΈΣ ΓΓ ΓΘ
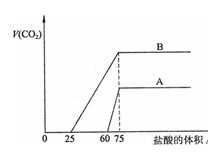 33Θ°»ΓΒ»Έο÷ ΒΡΝΩ≈®Ε»ΒΡNaOH»ή“ΚΝΫΖίA 33Θ°»ΓΒ»Έο÷ ΒΡΝΩ≈®Ε»ΒΡNaOH»ή“ΚΝΫΖίA
ΚΆBΘ§ΟΩΖί50mLΘ§œρΤδ÷–ΗςΆ®»κ“ΜΕ®ΝΩΒΡCO2Θ§ »ΜΚσΗς»Γ»ή“Κ10mLΘ§Ζ÷±πΫΪΤδœΓ ΆΈΣ100mLΘ§ Ζ÷±πœρœΓ ΆΚσΒΡ»ή“Κ÷–÷πΒΈΦ”»κ0.1mol/LΒΡ ―ΈΥαΘ§±ξΉΦΉ¥Ωωœ¬≤ζ…ζCO2ΤχΧεΧεΜΐ”κΥυΦ”―Έ ΥαΧεΜΐ÷°ΦδΒΡΙΊœΒ»γœ¬ΆΦΥυ ΨΘ§ ‘ΜΊ¥πœ¬Ν–Έ ΧβΘΚ Θ®1Θ©«ζœΏA±μΟςΘ§‘≠»ή“Κ÷–Ά®»κCO2ΚσΘ§ΥυΒΟ»ή“Κ÷–ΒΡ»ή÷ ΈΣΘ© Θ§ Θ§ΝΫ÷÷»ή÷ ΒΡΈο÷ ΒΡΝΩ÷°±»ΈΣ ΘΜΦ”―ΈΥαΚσ≤ζ…ζCO2ΧεΜΐΒΡΉν¥σ÷ΒΈΣ mLΓΘ Θ®2Θ©«ζœΏB±μΟςΘ§‘≠»ή“Κ÷–Ά®»κCO2ΚσΘ§ΥυΒΟ»ή“Κ÷–ΒΡ»ή÷ ΈΣ Θ§ Θ§ΝΫ÷÷»ή÷ Έο÷ ΒΡΝΩ÷°±»ΈΣ ΘΜΦ”―ΈΥαΚσ≤ζ…ζCO2ΧεΜΐΉν¥σ÷Β mLΓΘ Θ®3Θ©Ά®ΙΐΦΤΥψ«σNaOH»ή“ΚΒΡΈο÷ ΒΡΝΩ≈®Ε»ΓΘ
¥πΑΗΦΑΤάΖ÷±ξΉΦ “ΜΓΔΕΰΓΔ―Γ‘ώΧβΘ®50Ζ÷Θ©
ΒΎΔρΨμΘ®Ι≤50Ζ÷Θ© »ΐΓΔ Β―ιΧβ(±ΨΧβΑϋά®2–ΓΧβΘ§Ι≤14Ζ÷) 26Θ°Θ®1Θ©œ¬Ν– Β―ι≤ΌΉς’ΐ»ΖΒΡ « AΓΔB ΓΘ AΓΔ”ΟΥα ΫΒΈΕ®ΙήΝΩ»Γ25.12mLΒΡKMnO4»ή“Κ BΓΔ”Ο10mLΝΩΆ≤ΝΩ»Γ8.5mL’τΝσΥ° CΓΔ”ΟpH ‘÷Ϋ≤βΕ®¬»Υ°ΒΡpH÷ΒΈΣ3.3 DΓΔΫΪ“Μ’≈ Σ»σΒΡάΕ…Ϊ ·»ο ‘÷ΫΆΕ»κ Δ”–Cl2ΒΡΦ·ΤχΤΩ÷–, ‘÷ΫΉν÷’ΫΪ±δΚλ EΓΔ”ΟέαέωΦ”»»ΝρΥαΆ≠»ή“Κ÷Τ»ΓΒ®Ζ·ΨßΧε Θ®2Θ©œ¬ΟφaΓΣf «÷–―ß…ζ Β―ι÷–≥ΘΦϊΒΡΦΗ÷÷“«ΤςΘ®Χν–¥±ύΚ≈Θ§Εύ―ΓΒΙΩέΖ÷Θ©ΘΚ Θ®aΘ©ΝΩΆ≤ Θ®bΘ©»ίΝΩΤΩ Θ®cΘ©Τ’Ά® ‘Ιή Θ®dΘ©‘≤ΒΉ…’ΤΩ Θ®eΘ©Έ¬Ε»ΦΤ Θ®fΘ©ΧλΤΫ (1)Τδ÷–“Σ±ξ Ψ“«ΤςΨΏΧε Ι”ΟΈ¬Ε»ΒΡ «Θ®≤ΜΩΦ¬«Έ¬Ε»ΦΤΘ© aΓΔb ΘΜ (2)Ω…”ΟΉςΖ¥”ΠΤς≤ΔΡήΫχ––Φ”»»ΒΡ « cΓΔd ΓΓΓΓ ΓΘ 27.œ÷”–“ΜΕ®ΝΩΚ§”–Na2O‘”÷ ΒΡNa2O2 ‘―υΓΘ«κ¥”œ¬ΆΦ÷–―Γ”Ο Β±ΒΡ Β―ιΉΑ÷ΟΘ§«κ…ηΦΤ“ΜΗωΉνΦρΒΞΒΡ Β―ιΘ§≤βΕ®Na2O2 ‘―υΒΡ¥ΩΕ»ΓΘ Θ®Ω…Ι©―Γ‘ώΒΡΖ¥”ΠΈο÷Μ”–CaCO3ΙΧΧεΘ§6mol/L―ΈΥαΚΆ’τΝσΥ°Θ©ΓΘ
«κΧν–¥œ¬Ν–Ω’ΑΉΘΚ Θ®1Θ©–¥≥ω Β―ι÷–Na2OΚΆNa2O2Ζ÷±πΖΔ…ζΖ¥”ΠΒΡΜ·―ßΖΫ≥Χ ΫΓΘ Na2OΘΪH2OΘΫ2NaOH ΓΔΓΓ2Na2O2ΘΪ2H2OΘΫ4NaOHΘΪO2ΓϋΓΓΓΓΓΓΘΜ Θ®2Θ©”Π―Γ”ΟΒΡΉΑ÷Ο «(÷Μ“Σ«σ–¥≥ωΆΦ÷–ΉΑ÷ΟΒΡ±ξΚ≈) ΔίΔΌΔή ΘΜ Θ®3Θ©Υυ―ÔϹΑ÷ΟΒΡΝ§Ϋ”Υ≥–ρ”Π «(ΧνΗςΫ”ΩΎΒΡΉ÷ΡΗ;Ν§Ϋ”ΫΚΙή Γ¬‘). GABF ΓΓΓΘ ΥΡΓΔΦρ¥πΧβ(±ΨΧβΑϋά®4–ΓΧβΘ§Ι≤12Ζ÷) 28Θ°Κ§”–“ΜΕ®ΝΩCH3COONaΚΆCH3COOHΒΡΥ°»ή“Κ≥ΤΉςΓΑΜΚ≥ε»ή“ΚΓ±Θ§‘ΎΗΟ»ή“Κ÷–Φ”»κ…ΌΝΩΒΡ«ΩΥαΜρ«ΩΦν ±Θ§»ή“ΚΒΡpHΦΗΚθ≤Μ±δΘ§’βΩ…”…œ¬Ν–άκΉ”ΖΫ≥Χ Ϋά¥ΥΒΟςΘΚ Φ”»κΥα ±CH3COOΘ≠ H =CH3COOHΘΜΦ”»κΦν ±CH3COOH OHΘ≠= CH3COOΘ≠ H2OΘ§ ”…”ΎCH3COOHΚΆCH3COOΘ≠ΒΡ¥σΝΩ¥φ‘ΎΘ§»ή“Κ÷–ΒΡc(H )”κc(OHΘ≠)Μυ±Ψ±Θ≥÷≤Μ±δΓΘ “ΜΕ®ΝΩΒΡH2SΚΆNaHSΒΡ»ή“Κ“≤ΨΏ”–ΜΚ≥εΉς”ΟΘ§–¥≥ω‘Ύ¥Υ»ή“Κ÷–Φ”»κ…ΌΝΩ«ΩΥαΜρ«ΩΦν ±ΖΔ…ζΒΡάκΉ”Ζ¥”ΠΖΫ≥Χ ΫΘΚ Φ”»κΥα ± HSΘ≠ HΘΪ=H2S ΓΓΓΓΓΓ ΓΓ ΘΜ Φ”»κΦν ± H2S OHΘ≠=HSΘ≠ΘΪH2O ΓΓΓΓ ΓΓ ΓΘ 29Θ°Μ·―ßΖ¥”Π÷–Θ§»γΙϊΗχ‘≠Ή”ΚΥΆβΒγΉ”ΉψΙΜΒΡΡήΝΩΘ§’β–©ΒγΉ”±ψΜαΑΎΆ―‘≠Ή”ΚΥΒΡ χΗΩΕχάκ»ΞΓΘΚΥΆβΒγΉ”άκΩΣΗΟ‘≠Ή”ΜράκΉ”Υυ–η“ΣΒΡΡήΝΩ÷ς“Σ ήΝΫ¥σ“ρΥΊΒΡ”ΑœλΘΚ‘≠Ή”ΚΥΕ‘ΚΥΆβΒγΉ”ΒΡΈϋ“ΐΝΠΘΜ–Έ≥…Έ»Ε®ΫαΙΙΒΡ«ψœρΓΘœ¬±μ «“Μ–©÷ήΤΎ±μ÷–1Θ≠18Κ≈‘ΣΥΊΒΡΤχΧ§‘≠Ή” ß»ΞΚΥΆβ≤ΜΆ§ΒγΉ”Υυ–ηΒΡΡήΝΩΘ®kJΓΛmolΘ≠1Θ©ΘΚ
|
| ο°
| X
| Y
| ß»ΞΒΎ“ΜΗωΒγΉ”
| 519
| 502
| 580
| ß»ΞΒΎΕΰΗωΒγΉ”
| 7296
| 4570
| 1820
| ß»ΞΒΎ»ΐΗωΒγΉ”
| 11799
| 6920
| 2750
| ß»ΞΒΎΥΡΗωΒγΉ”
|
| 9550
| 11600 |
ΔΎ Ά®Ιΐ…œ ω–≈œΔΚΆ±μ÷–ΒΡ ΐΨίΖ÷ΈωΘΚΈΣ ≤Ο¥ο°‘≠Ή” ß»ΞΚΥΆβΒΎΕΰΗωΒγΉ” ±Υυ–ηΒΡ
ΡήΝΩ“Σ‘Ε‘Ε¥σ”Ύ ß»ΞΒΎ“ΜΗωΒγΉ”Υυ–ηΒΡΡήΝΩΘΚο° ß»ΞΒΎ“ΜΗωΒγΉ”Κσ¥οΈ»Ε®ΫαΙΙΘΜ
ΔΎ‘Ύ“ΜΕ®ΧθΦΰœ¬Θ§±μ÷–XΩ…Ρή”κ«βΤχΖ¥”ΠΒΡΜ·―ßΖΫ≥Χ Ϋ « 2XΘΪH2ΘΫ2XH ΘΜ
ΔέY‘ΣΥΊ≥ΘΦϊΒΡΜ·ΚœΦέΩ…Ρή «ΓΓΘΪ3ΓΓΓΓΓΓΓΓΓΘ
30Θ°ΧζΥαΡΤ(Na2FeO4) «Υ°¥ΠάμΙΐ≥Χ÷– Ι”ΟΒΡ“Μ÷÷–¬–ΆΨΜΥ°ΦΝΘ§Υϋ―θΜ·–‘±»ΗΏΟΧΥαΦΊΗϋ«ΩΘ§±Ψ…μ‘ΎΖ¥”Π÷–±ΜΜΙ‘≠ΈΣFe3 άκΉ”ΓΘ÷Τ»ΓΧζΥαΡΤΒΡ≥Χ ΫΈΣΘΚ
Fe(NO3)3 NaOH Cl2©ΛNa2FeO4 NaNO3 NaCl H2O Θ§‘ρΖ¥”Π÷– Fe ‘ΣΥΊ±Μ―θΜ·ΓΘ
ΈεΓΔΆΤΕœΧβ(±ΨΧβΙ≤1–ΓΧβΘ§Ι≤8Ζ÷)
31Θ°Ρ≥ΜλΚœΈοAΘ§Κ§”–KAl(SO4)2ΓΔAl2O3ΚΆFe2O3Θ§‘Ύ“ΜΕ®ΧθΦΰœ¬Ω… Βœ÷ΆΦΥυ ΨΒΡΈο÷ ÷°ΦδΒΡ±δΜ·ΘΚ
Ψί¥Υ≈–ΕœΘΚ
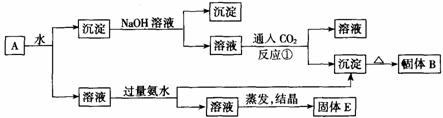
(1)ΙΧΧεBΥυΚ§Έο÷ ΒΡΜ·―ß ΫΈΣ__Al2O3_____ΘΜ
(2)ΙΧΧεEΥυΚ§Έο÷ ΒΡΜ·―ß ΫΈΣ_K2SO4”κΘ®NH4Θ©2SO4___________ΘΜ
(3)Ζ¥”ΠΔΌΒΡάκΉ”ΖΫ≥Χ ΫΈΣ__ Al O2Θ≠ΘΪCO2ΘΪ2H2OΘΫAlΘ®OHΘ©3ΓΐΘΪHCO3Θ≠ ΓΘ
ΝυΓΔΦΤΥψΧβ(±ΨΧβΙ≤2–ΓΧβΘ§Ι≤16Ζ÷)
32Θ°ΫΪ50mL 0.1mol/LBaCl2»ή“Κ”κ100mL0.75mol/L H2SO4»ή“ΚΜλΚœΘ§«σΘΚ
Θ®1Θ©Ζ¥”Π≤ζ…ζ≥ΝΒμΒΡ÷ ΝΩ «ΓΓ1.2ΓΓΓΓ gΘΜ(±ΘΝτ2ΈΜ”––ß ΐΉ÷)
Θ®2Θ©»τ≤ΜΩΦ¬«»ή“ΚΧεΜΐΒΡ±δΜ·Θ§‘ρΖ¥”ΠΚσ»ή“ΚΒΡCΘ®HΘΪΘ©ΈΣ 1. 0mol/L ΓΘ
 33Θ°»ΓΒ»Έο÷ ΒΡΝΩ≈®Ε»ΒΡNaOH»ή“ΚΝΫΖίA
33Θ°»ΓΒ»Έο÷ ΒΡΝΩ≈®Ε»ΒΡNaOH»ή“ΚΝΫΖίA
ΚΆBΘ§ΟΩΖί50mLΘ§œρΤδ÷–ΗςΆ®»κ“ΜΕ®ΝΩΒΡCO2Θ§
»ΜΚσΗς»Γ»ή“Κ10mLΘ§Ζ÷±πΫΪΤδœΓ ΆΈΣ100mLΘ§
Ζ÷±πœρœΓ ΆΚσΒΡ»ή“Κ÷–÷πΒΈΦ”»κ0.1mol/LΒΡ
―ΈΥαΘ§±ξΉΦΉ¥Ωωœ¬≤ζ…ζCO2ΤχΧεΧεΜΐ”κΥυΦ”―Έ
ΥαΧεΜΐ÷°ΦδΒΡΙΊœΒ»γœ¬ΆΦΥυ ΨΘ§ ‘ΜΊ¥πœ¬Ν–Έ ΧβΘΚ
Θ®1Θ©«ζœΏA±μΟςΘ§‘≠»ή“Κ÷–Ά®»κCO2ΚσΘ§ΥυΒΟ»ή“Κ÷–ΒΡ»ή÷ ΈΣNaOH Θ§Na2CO3 Θ§ΝΫ÷÷»ή÷ ΒΡΈο÷ ΒΡΝΩ÷°±»ΈΣ3:1ΘΜΦ”―ΈΥαΚσ≤ζ…ζCO2ΧεΜΐΒΡΉν¥σ÷ΒΈΣ 33.6 mLΓΘ
Θ®2Θ©«ζœΏB±μΟςΘ§‘≠»ή“Κ÷–Ά®»κCO2ΚσΘ§ΥυΒΟ»ή“Κ÷–ΒΡ»ή÷ ΈΣ Na2CO3 Θ§NaHCO3 Θ§ΝΫ÷÷»ή÷ Έο÷ ΒΡΝΩ÷°±»ΈΣ 1:1 ΘΜΦ”―ΈΥαΚσ≤ζ…ζCO2ΧεΜΐΉν¥σ÷Β 112 mLΓΘ
Θ®3Θ©Ά®ΙΐΦΤΥψ«σNaOH»ή“ΚΒΡΈο÷ ΒΡΝΩ≈®Ε»ΓΘ
ΫβΈωΘΚ…ζ≥…Εΰ―θΜ·ΧΦΉνΕύ ±Θ§»ή“Κ÷–÷Μ”–NaCl
Ι 0.05C(NaOH)ΓΝ1/5=0.075ΓΝ0.1
C(NaOH)=0.75mol/L
| |