|
ΗΏ“ΜΜ·―ß…œ≤αΤΎ÷– ‘Ψμ
ΑύΦΕ___________ –’Οϊ____________ ―ßΚ≈________________ ≥…Φ®______________
“ΜΓΔΜυ¥ΓΧβΘ®ΉήΖ÷85Ζ÷Θ©
ΒΎІΨμΘ®―Γ‘ώΧβΘ§Ι≤42Ζ÷Θ©
œ¬Ν–1ΓΪ14–ΓΧβΈΣ―Γ‘ώΧβΘ§ΟΩ“Μ–ΓΧβ÷Μ”–“ΜΗω’ΐ»Ζ―ΓœνΖϊΚœΧβ“βΓΘΟΩ–ΓΧβ3Ζ÷Θ§Ι≤42Ζ÷ΓΘ
1ΓΔ»ή“ΚΓΔΫΚΧεΓΔΉ«“Κ»ΐ÷÷Ζ÷…ΔœΒΉν±Ψ÷ ΒΡ«χ±π «Θ®ΓΓΓΓΘ©
AΘ°Έ»Ε®–‘ΓΓΓΓBΘ°ΆΗΟςΕ»ΓΓΓΓCΘ°Ζ÷…Δ÷ ΈΔΝΘ¥σ–ΓΓΓΓΓDΘ°ΡήΖώΖΔ…ζΕΓ¥οΕϊœ÷œσ
2ΓΔœ¬Ν–ΜλΚœΈοΡή”Ο»ήΫβΓΔΙΐ¬ΥΓΔ’τΖΔ»ΐ≤Ϋ≤ΌΉςΖ÷άκΒΡ «Θ®ΓΓΓΓΘ©
AΘ°Υ°ΚΆΨΤΨΪΒΡΜλΚœΈοΓΓΓΓΓΓ ΓΓΓΓBΘ° ≥―ΈΚΆ’αΧ«ΒΡΜλΚœΈο
CΘ°¬»Μ·ΦΊΚΆ¬»Μ·“χΒΡΜλΚœΈοΓΓ ΓΓDΘ°ΝρΥα±ΒΚΆΥ°ΒΡΜλΚœΈο
3ΓΔœ¬Ν–ΗςΉιΈο÷ ÷–Θ§ΨυΈΣ¥ΩΨΜΈοΒΡ“ΜΉι «
A ΒβΨΤΓΔΗ…±υ B ¥÷―ΈΓΔ“Κ¬» CΓΔNa2CO3•10H2O Na2CO3 D Φν ·Μ“ΓΔ¬»Υ°
4ΓΔΨί±®ΒάΘ§‘¬«ρ…œ”–¥σΝΩ  ¥φ‘ΎΘ§ΡήΙΜΧαΙ©Ψό¥σΒΡΡήΝΩΓΘ“‘œ¬ΙΊ”Ύ ¥φ‘ΎΘ§ΡήΙΜΧαΙ©Ψό¥σΒΡΡήΝΩΓΘ“‘œ¬ΙΊ”Ύ  ΒΡΥΒΖ®÷–Θ§’ΐ»ΖΒΡ «Θ®ΓΓΓΓΘ© ΒΡΥΒΖ®÷–Θ§’ΐ»ΖΒΡ «Θ®ΓΓΓΓΘ©
AΘ°  ”κ ”κ 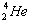 τ”Ύ≤ΜΆ§ΒΡ‘ΣΥΊΓΓΓΓΓΓBΘ° τ”Ύ≤ΜΆ§ΒΡ‘ΣΥΊΓΓΓΓΓΓBΘ°  ±» ±» 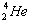 Εύ“ΜΗω÷–Ή” Εύ“ΜΗω÷–Ή”
CΘ°  « « 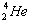 ΒΡΆ§ΈΜΥΊΓΓΓΓΓΓΓΓΓΓΓΓDΘ° ΒΡΆ§ΈΜΥΊΓΓΓΓΓΓΓΓΓΓΓΓDΘ°  ±» ±» 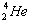 …Ό“ΜΗω÷ Ή” …Ό“ΜΗω÷ Ή”
5ΓΔœ¬Ν–ΥΒΖ®÷–’ΐ»ΖΒΡ «Θ®NA±μ ΨΑΔΖϋΦ”Β¬≥Θ ΐΒΡ ΐ÷ΒΘ©
A 71g¬»ΤχΥυΚ§”–ΒΡ‘≠Ή” ΐΡΩΈΣNA
B Μ·―ßΖ¥”Π÷–1molΫπ τΟΨ±δ≥…ΟΨάκΉ”Θ®Mg2 Θ© ± ß»ΞΒΡΒγΉ” ΐΡΩΈΣ2NA
C ±ξΉΦΉ¥Ωωœ¬Θ§22.4LΥΡ¬»Μ·ΧΦΘ®CCl4Θ©÷–Κ§”–NAΗωCCl4Ζ÷Ή”
DΆ®≥ΘΉ¥Ωωœ¬Θ§22.4L¬»Μ·«βΥυΚ§ΒΡΖ÷Ή” ΐΈΣNA
6ΓΔ≈δ÷Τ“ΜΕ®ΧεΜΐΓΔ“ΜΕ®Έο÷ ΒΡΝΩ≈®Ε»ΒΡ»ή“Κ ±Θ§œ¬Ν–«ιΩω÷–Θ§ Ι»ή“Κ≈®Ε»ΤΪ–Γ
A »ίΝΩΤΩ÷–‘≠”–…ΌΝΩΒΡΥ°
B»ή“Κ¥”…’±≠÷–ΉΣ“ΤΒΫ»ίΝΩΤΩ÷–ΚσΟΜ”–œ¥Β”…’±≠
CΕ®»ί ±Η© ”ΩΧΕ»œΏ
D ΒΈΙήΦ”Υ° ±Θ§≤Μ–Γ–ΡΑ―…ΌΝΩΥ°ΒΈΒΫ»ίΝΩΤΩΆβ
7ΓΔΫΪδεΥ°÷–ΒΡδείΆ»Γ≥ωά¥ΒΡ Β―ι÷–Θ§œ¬Ν–ΥΒΖ®¥μΈσΒΡ «
AΘ°Ζ÷“Κ¬©ΕΖ Ι”Ο«Α“ΣΦλ―ιΥϋ «Ζώ¬©Υ° BΘ°ίΆ»ΓΦΝ“Σ«σ≤Μ»ή”ΎΥ°Θ§«“±»Υ°Ηϋ»ί“Ή Ιδε»ήΫβ
C. ΉΔ»κδεΥ°ΚΆίΆ»ΓΦΝΘ§ΒΙΉΣΖ÷“Κ¬©ΕΖΖ¥Η¥”ΟΝΠ’πΒ¥ΚσΝΔΦ¥Ζ÷“Κ
D. Ζ÷“Κ ±Θ§¥ρΩΣ–ΐ»ϊΘ§ Ιœ¬≤ψ“ΚΧεΝς≥ωΘ§…œ≤ψ“ΚΧε¥”…œΩΎΒΙ≥ω
8ΓΔœ¬Ν– ΫΉ”÷–,≤ΜΡή±μ ΨΈο÷ ΒΡΝΩΈΣΕύ…ΌΡΠΒΡ «:
A. eq \o(\s\up 8(Έο÷ ΒΡΖ÷Ή” ΐ),\s\up 1(©Λ©Λ©Λ©Λ©Λ©Λ©Λ©Λ),\s\do 8(ΑΔΖϋΦ”Β¬¬ό≥Θ ΐ))Έο÷ ΒΡΖ÷Ή” ΐ©Λ©Λ©Λ©Λ©Λ©Λ©Λ©Λ B. eq \o(\s\up 8(Έο÷ ΒΡ÷ ΝΩ),\s\up 1(©Λ©Λ©Λ©Λ©Λ©Λ),\s\do 8(Έο÷ ΒΡ ΫΝΩ))Έο÷ ΒΡ÷ ΝΩ©Λ©Λ©Λ©Λ©Λ©Λ C. eq \o(\s\up 8(ΤχΧεΒΡΧεΜΐ(±ξΉΦΉ¥Ωω)),\s\up 1(©Λ©Λ©Λ©Λ©Λ©Λ©Λ©Λ©Λ©Λ),\s\do 8(ΤχΧεΡΠΕϊΧεΜΐ))ΤχΧεΒΡΧεΜΐ(±ξΉΦΉ¥Ωω©Λ©Λ©Λ©Λ©Λ©Λ©Λ©Λ©Λ©Λ
D. Έο÷ ΒΡΝΩΒΡ≈®Ε»ΓΝ»ή“ΚΧεΜΐ
9ΓΔ”Ο20g NaOH≈δ≥…250mL»ή“ΚΘ§¥”÷–»Γ≥ω5mLΘ§»ή“ΚΈο÷ ΒΡΝΩ≈®Ε»ΈΣΘΚ
A. 0.02mol/L B. 0.01mol C. 1mol/L D. 2mol/L
10ΓΔœ¬Ν–Μ·―ßΖ¥”Π÷–Θ§ τ”Ύ÷ΟΜΜΖ¥”ΠΒΡ «
A Cl2 2NaOH=NaCl NaClO 2H2O B 2Fe 3Cl2=2FeCl3
C Cl2 2KI=I2 2KCl D (NH4)2SO4 2NaOH= Na2SO4 2NH3Γϋ 2H2O
11ΓΔœ¬Ν–”–ΙΊ Β―ι≤ΌΉςΒΡ–π ω÷–Θ§¥μΈσΒΡ «
A Β―ι “”Ο≈≈±ΞΚΆ ≥―ΈΥ°Φ·ΤχΖ® ’Φ·¬»ΤχΆξ±œΚσΘ§Α―ΒΦΙή¥”Υ°÷–»Γ≥ωΘ§»ΜΚσ“Τ»ΞΨΤΨΪΒΤ
B «βΤχΜΙ‘≠―θΜ·Ά≠ΒΡ Β―ιΫα χ ±Θ§œ»“Τ»ΞΨΤΨΪΒΤΘ§¥ΐ ‘Ιήά以Κσ‘ΌΆΘ÷ΙΆ®»κ«βΤχ
C «ψΒΙ“ΚΧεΫχ––Ιΐ¬Υ ±Θ§”Π Ι“ΚΧε―ΊΉ≈≤ΘΝßΑτΝςœ¬Θ§«“ΒΆ”Ύ¬Υ÷Ϋ±Ώ‘Β
D “ρNaOH”–Η· ¥–‘Θ§Ω…‘ΎΧλΤΫΝΫΆ–≈Χ…œΖ≈Ά§―υΒΡ¬Υ÷ΫΚσ‘ΌΖ≈NaOHΘ§»ΜΚσΫχ––≥ΤΝΩ
12ΓΔ‘Ύœ¬Ν–Έο÷ ΒΡΥ°»ή“Κ÷–Ζ÷±πΦ”»κΈό…ΪΒΡ«β―θΜ·±Β»ή“ΚΚσΘ§‘≠»ή“Κ÷–ΒΡ“θάκΉ”ΚΆ―τάκΉ”ΕΦΦθ…ΌΒΡ «Θ® Θ©
AΘ°CuSO4 BΘ°CaΘ®NO3Θ©2ΓΓΓΓCΘ°Na2CO3ΓΓΓΓ DΘ°FeCl3
13ΓΔΙΐ¬ΥΚσΒΡ ≥―ΈΥ°»‘Κ§”–Ω…»ή–‘ΒΡCaCl2ΓΔMgCl2ΓΔNa2SO4 Β»‘”÷ Θ§Ά®Ιΐ»γœ¬ΦΗΗω Β―ι≤Ϋ÷ηΘ§Ω…÷ΤΒΟ¥ΩΨΜΒΡ ≥―ΈΥ°ΘΚΔΌ Φ”»κ…‘ΙΐΝΩΒΡNa2CO3»ή“ΚΘΜΔΎ Φ”»κ…‘ΙΐΝΩΒΡNaOH»ή“ΚΘΜΔέ Φ”»κ…‘ΙΐΝΩΒΡBaCl2 »ή“ΚΘΜΔήΒΈ»κœΓ―ΈΥα÷ΝΈόΤχ≈ί≤ζ…ζΘΜΔί Ιΐ¬ΥΘΜ’ΐ»ΖΒΡ≤ΌΉςΥ≥–ρ «
AΘ°ΔέΔΎΔΌΔίΔή BΘ°ΔΌΔΎΔέΔίΔή CΘ°ΔΎΔέΔΌΔήΔί DΘ°ΔέΔίΔΎΔΌΔή
14ΓΔ“ΜΕ®÷ ΝΩΒΡΝρΥαοß÷–Θ§οßΗυάκΉ”ΚΆΝρΥαΗυάκΉ”ΒΡΈο÷ ΒΡΝΩ÷°±» «Θ® Θ©
A 3ΘΚ8 B 2ΘΚ1 C 1ΘΚ2 D 1ΘΚ1
ΒΎΔρΨμΘ®Ζ«―Γ‘ώΧβΘ§Ι≤43Ζ÷Θ©
15ΓΔΘ®3Ζ÷Θ©œ÷”–“‘œ¬Έο÷ ΘΚΔΌΩ’ΤχΓΔΔΎ«β―θΜ·ΡΤΓΔΔέΝρΥαΓΔΔή―ΈΥαΓΔΔί“χΓΔΔό’αΧ«ΓΔΔΏCCl4ΓΘΤδ÷– τ”ΎΜλΚœΈοΒΡ”– Θ§ τ”ΎΒΞ÷ ΒΡ”– Θ§ τ”ΎΒγΫβ÷ ΒΡ”– ΓΘ
16ΓΔΘ®9Ζ÷Θ©”–XΓΔYΓΔZ»ΐ÷÷‘ΣΥΊΘ§XΒΡ‘≠Ή”ΚΥΡΎΈό÷–Ή”Θ§Y‘≠Ή”ΒΡΒΎ»ΐΒγΉ”≤ψ…œ”–1ΗωΒγΉ”Θ§Z‘≠Ή”ΉνΆβ≤ψΒγΉ” ΐ «ΤδΒγΉ”≤ψ ΐΒΡ3±ΕΓΘ ‘≈–ΕœXΓΔYΓΔZΗς « ≤Ο¥‘ΣΥΊΘΩ
Θ®1Θ©“ά¥Έ–¥≥ω’β»ΐ÷÷‘ΣΥΊΒΡΖϊΚ≈____ ____ΓΔ___ _____ΓΔ________ ΘΜ
Θ®2Θ©Μ≠≥ωX‘≠Ή”ΫαΙΙ Ψ“βΆΦΘΚ____ ____ΘΜYάκΉ”ΫαΙΙ Ψ“βΆΦΘΚ_ _____ΘΜ
ZάκΉ”ΫαΙΙ Ψ“βΆΦΘΚ_ _____ΓΘ
17ΓΔΘ®6Ζ÷Θ©19gΡ≥ΕΰΦέΫπ τΒΡ¬»Μ·ΈοACl2÷–Κ§”–0.4mol ClΘ≠άκΉ”Θ§ΫΪΗΟΕΰΦέΫπ τΒΡ¬»Μ·Έο»Ϊ≤Ω»ή”ΎΥ°≈δ≥…100ml»ή“ΚΓΘ‘ρΗΟACl2ΒΡΡΠΕϊ÷ ΝΩ « Θ§Έο÷ ΒΡ≈®Ε» « Θ§Τδ÷–A2 ΒΡΈο÷ ΒΡ≈®Ε» « ΓΘ
18ΓΔΘ®1Θ©(5Ζ÷)1mol ΝρΥαοßΒΡ÷ ΝΩ « gΘ§Κ§ Ηω―θ‘≠Ή”ΘΜΆξ»ΪΒγάκ ±Ω…“‘…ζ≥… mol NH4 άκΉ”, mol SO42-άκΉ”ΘΜΦ”»κ ml0.5mol/LBaCl2»ή“ΚΘ§ΡήΫΪSO42-άκΉ”«ΓΚΟΆξ»Ϊ≥ΝΒμΓΘ
Θ®2Θ©(3Ζ÷)0.1molΒΡ 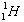 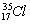 Ζ÷Ή”÷–ΥυΚ§÷–Ή” ΐ‘ΦΈΣ Θ§÷ Ή” ΐ‘ΦΈΣ Θ§÷ ΝΩ‘ΦΈΣ ΓΘ Ζ÷Ή”÷–ΥυΚ§÷–Ή” ΐ‘ΦΈΣ Θ§÷ Ή” ΐ‘ΦΈΣ Θ§÷ ΝΩ‘ΦΈΣ ΓΘ
19ΓΔΘ®4Ζ÷Θ©–ΓΚλΕ‘Ρ≥÷÷ΤχΧε―υΤΖΫχ––»γœ¬ΒΡ Β―ιΘΚΔΌΖΔœ÷Τδ÷ς“Σ≥…Ζ÷ΤχΧεA“Ή»ή”ΎΥ°ΘΜΔΎΫΪAΒΡ≈®»ή“Κ”κMnO2Ι≤»»…ζ≥…“Μ÷÷ΜΤ¬Χ…ΪΤχΧεΒΞ÷ BΘ§ΔέBΆ®»κ ·Μ“Υ°÷–Ω…“‘ΒΟΒΫΤ·ΑΉΖέΓΘ«κΜΊ¥πΘΚ
Θ®1Θ©–¥≥ωAΒΡ≈®»ή“Κ”κMnO2Ι≤»»ΒΡΜ·―ßΖΫ≥Χ ΫΘΚ ΘΜ
Θ®2Θ©–¥≥ωBΆ®»κ ·Μ“Υ°÷–÷ΤΤ·ΑΉΖέΒΡΜ·―ßΖΫ≥Χ ΫΘΚ ΓΘ
20ΓΔ Β―ι “”–ΝΫΤΩ»ή“ΚΘ§ΕΦ“― ß»Ξ±ξ«©Θ§“―÷ΣΤδ÷–“ΜΤΩ «ΝρΥα»ή“ΚΘ§Νμ“ΜΤΩ «’αΧ«»ή“ΚΓΘΆ§―ßΟ«…ηΦΤΝΥœ¬Ν–ΖΫΑΗΕ‘»ή“ΚΫχ––Φχ±πΘΚ
A”ΟPH ‘÷ΫΖ÷±π≤βΕ®ΝΫ»ή“ΚΒΡPHΓΘPH<7ΒΡ «ΝρΥα»ή“ΚΘ§PH=7ΒΡ «’αΧ«»ή“ΚΓΘ
B»Γ―υΘ§Ζ÷±πœρΝΫ»ή“Κ÷–ΒΈΦ”―ΈΥαΥαΜ·ΒΡ¬»Μ·±Β»ή“ΚΘ§…ζ≥…ΑΉ…Ϊ≥ΝΒμΒΡ «ΝρΥα»ή“ΚΘ§≤Μ≤ζ…ζ≥ΝΒμΒΡ «’αΧ«»ή“ΚΓΘ
C»Γ―υΘ§Ζ÷±πœρΝΫ»ή“Κ÷–Φ”»κ“Μ–ΓΤ§Ά≠Τ§Θ§≤ζ…ζΤχΧεΒΡ «ΝρΥα»ή“ΚΘ§≤Μ≤ζ…ζΤχΧεΒΡ «’αΧ«»ή“ΚΓΘ
D»Γ―υΘ§Ζ÷±πΫχ––ΒΦΒγ–‘ Β―ιΘ§ΡήΒΦΒγΒΡ «ΝρΥα»ή“ΚΘ§≤ΜΡήΒΦΒγΒΡ «’αΧ«»ή“ΚΓΘ
EΖ÷±π»ΓΦΪ…ΌΝΩ»ή“Κ≥Δ“Μ≥ΔΘ§”–ΧπΈΕΒΡ «’αΧ«»ή“ΚΘ§”–ΥαΈΕΒΡ «ΝρΥα»ή“ΚΓΘ
Θ®1Θ©…œ ω Β―ιΖΫΑΗΦΑΫα¬έ’ΐ»ΖΒΡ « Θ®Χν–ρΚ≈Θ©ΓΘΘ®3Ζ÷Θ©
Θ®2Θ©«κΡψ…ηΦΤΝμ“ΜΗω Β―ιΖΫΑΗΦχ±πΝρΥα»ή“ΚΚΆ’αΧ«»ή“ΚΓΘΘ®2Ζ÷Θ©
Β―ιΖΫΑΗΘΚ
21ΓΔΘ®8Ζ÷Θ© Β―ι “–η“Σ0.1mol /L«β―θΜ·ΡΤ»ή“Κ100mLΘ§œ÷”–2mol /L«β―θΜ·ΡΤ»ή“ΚΓΘ
Θ®1Θ©ΦΤΥψΥυ–η2mol /L«β―θΜ·ΡΤ»ή“ΚΒΡΧεΜΐΘΜΘ®2Ζ÷Θ©
Θ®2Θ©Άξ»Ϊ÷–ΚΆ50 mL“―≈δ÷Τ»ή“ΚΘ§–η“Σ1mol/LΒΡΝρΥα»ή“ΚΕύ…ΌΧεΜΐΘΩΘ®6Ζ÷Θ©
ΕΰΓΔΡήΝΠΧβΘΚΘ®ΉήΖ÷15Ζ÷Θ©
œ¬Ν–22ΓΪ24–ΓΧβΈΣ―Γ‘ώΧβΘ§ΟΩ“Μ–ΓΧβ÷Μ”–“ΜΗωΜρΝΫΗω’ΐ»Ζ―ΓœνΖϊΚœΧβ“βΓΘΟΩ–ΓΧβ3Ζ÷Θ§Ι≤9Ζ÷ΓΘ
22ΓΔΨΏ”–œύΆ§ΒΡ‘≠Ή”ΚΥΗω ΐΚΆœύΆ§ΒΡΒγΉ”Ηω ΐΒΡΝΫ÷÷ΈΔΝΘΫ–Β»ΒγΉ”ΧεΘ§œ¬Ν–ΗςΉιΈΔΝΘ τΒ»ΒγΉ”ΧεΒΡ «Θ®ΓΓΓΓΘ©
AΘ°Na ΚΆOH- BΘ°H3O ΚΆNH3 CΘ°NH2-ΚΆOH- DΘ°CH4ΚΆNHΘΪ4
23ΓΔΈο÷ ΒΡΝΩ≈®Ε»œύΆ§ΒΡMgCl2ΓΔKClΓΔAlCl3»ή“ΚΘ§Ζ÷±π”κΆ§ΧεΜΐΆ§≈®Ε»ΒΡAgNO3»ή“Κ«ΓΚΟΆξ»ΪΖ¥”ΠΘ§œϊΚΡ»ΐ÷÷―Έ»ή“ΚΒΡΧεΜΐ÷°±»ΈΣΘ®ΓΓΓΓΘ©
AΘ°1ΘΚ2ΘΚ3ΓΓΓΓ BΘ°3ΘΚ2ΘΚ1ΓΓ ΓΓC. 3ΘΚ6ΘΚ2ΓΓ ΓΓDΘ°6ΘΚ3ΘΚ2
24ΓΔ”–ΥΡΤΩ≥Θ”Ο»ή“ΚΘΚΔΌBaCl2»ή“Κ,ΔΎNaCl»ή“Κ,ΔέNa2SO4»ή“Κ,ΔήCuSO4»ή“ΚΓΘ≤Μ”ΟΤδΥϊ ‘ΦΝΘ§Ω…Ά®Ιΐ Β―ιΖΫΖ®ΫΪΥϋΟ«“Μ“ΜΦχ±πΩΣά¥Θ§Φχ±π≥ωά¥ΒΡœ»ΚσΥ≥–ρΩ…Ρή «Θ®ΓΓΓΓΘ©
A ΔΌΔήΔέΔΎ B ΔΌΔέΔήΔΎ C ΔήΔΌΔέΔΎ D ΔήΔΌΔΎΔέ
25ΓΔΘ®1Θ©Θ®2Ζ÷Θ©‘ΎΆ§Έ¬Ά§―Ιœ¬Θ§œύΆ§ΧεΜΐΒΡ»ΈΚΈΤχΧεΚ§”–œύΆ§ΒΡΖ÷Ή”Θ§’βΨΆ «÷χΟϊΒΡΑΔΖϋΦ”Β¬Ε®¬…ΓΘ‘ΎœύΆ§Έ¬Ε»ΚΆœύΆ§―Ι«Ωœ¬œ÷‘Ύ“―÷Σ”–œύΆ§÷ ΝΩΒΡΕΰ―θΜ·¬»Θ®ClO2Θ©ΚΆ¬»ΤχΒΡΧεΜΐ÷°±» « ΓΘ
Θ®2Θ©Θ®4Ζ÷Θ©ΓΑ»Υ‘λΩ’ΤχΓ±Θ®―θΤχ”κΚΛΤχΒΡΜλΚœΤχΧεΘ©Ω…”Ο”ΎΦθ«αΡ≥–©≤ΓΆ¥ΜρΙ©…νΥ°«±Υ°‘± Ι”ΟΓΘ‘Ύ±ξΉΦΉ¥Ωωœ¬Θ§5.6LΓΑ»Υ‘λΩ’ΤχΓ±ΒΡ÷ ΝΩ «2.4gΘ§Τδ÷–―θΤχ”κΚΛΤχΒΡΧεΜΐ±» « Θ§―θΤχΒΡ÷ ΝΩ « ΓΘ
|