|
[试题]:高一化学试题 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
命题人 张朝利 可能用到的相对原子质量:H:1 C:12 N:14 O:16 Na:23 Mg:24 S:32 K:39 Cu:64 Ba:137 (第I卷) 一、选择题(每小题仅有一个正确答案,共20小题,1-10小题每题2分,11-20小题每题3分,共50分) 1、既能使石蕊试液变红,又能使品红试液变为无色,还能使溴水褪色的是( ) A.Cl2 B.H2S C.SO2 D.CO 2、由于易被氧化而不宜长期存放的溶液是( ) A.氢硫酸 B.硫酸钠溶液 C.漂白粉 D.浓硫酸 3、现有以下几种措施:①对燃烧煤时产生的尾气进行除硫处理,②少用原煤做燃料,③燃煤时鼓入足量空气、,④开发清洁能源。其中能减少酸雨产生的措施的( ) A.①②③ B.②③④ C.①②④ D.①③④ 4、在下列生成二氧化硫的反应中,反应物中的含硫物质被氧化的是( ) A . 硫在空气中燃烧 B. 铜片与浓硫酸共热 C . 红热的木炭与浓硫酸反应 D . 亚硫酸钠与稀硫酸反应 5、氯化碘(ICl)的化学性质跟氯气相似,预计它跟水反应的最初生成物是 ( ) A.HCl和HIO B.HI和HClO C.HClO3和HIO D.HClO和HIO 6、含碘食盐中的碘是以碘酸钾(KIO3)形式存在的。已知在酸性溶液中IO3-和I-发生下列反应IO3-+5I-+6H+=3I2+3H2O。现有下列物质①稀硫酸;②pH试纸;③淀粉碘化钾溶液;④淀粉溶液。利用上述反应,可用来检验含碘食盐中含有IO3-的是 ( ) 7、下列各组离子,在溶液中能大量共存,且溶液为无色透明的离子组是( ) A.K+、MnO4-、Cl-、SO42- B.Na+、NO3-、CO32-、Cl- C.Na+、H+、SO32-、SO42- D.Na+、NO3-、Fe2+、H+ 8、下列物质中含有非极性共价键的是 ( ) A.NaOH B . Na2O C.Na2O2 D.CaCl2 9、已知反应2H2S+O2=2S↓+2H2O,4NaI+O2+2H2O=4NaOH+2I2和Na2S+I2=2NaI+S↓,下列氧化性大小关系正确的是( ) A.O2>I2>S B.I2>O2>S C.O2>S>I2 D.S>I2>O2 10、设阿伏加德常数为NA。则下列说法正确的是( ) A、 常温常压下,11.2 L甲烷中含有的氢原子数为2NA B、标准状况下,0.3 mol二氧化硫中含有氧原子数为0.3NA C、常温下,2.7 g铝与足量的盐酸反应,失去的电子数为0.3NA D、常温下,1L 0.1mol/L MgCl2溶液中含Mg2+数为0.2NA 11、使用胆矾(CuSO4?5H2O)配制0.1 mol/L 的硫酸铜溶液,正确的操作是………….( ) A、将胆矾加热除去结晶水后,称取16 g溶解在1 L水中。 B、称取25 g胆矾溶于水,然后将此溶液稀释至1 L。 C、称取25 g胆矾溶解在1 L水里。 D、将16 g胆矾溶于水,然后将此溶液稀释至1 L。 12、下列说法正确的是 ( ) A.原子及其离子的核外电子层数等于该元素所在的周期数 B.元素周期表中从ⅢB到ⅡB族10个纵行的元素都是金属元素 C.稀有气体原子的最外层电子数都是8 13、X+、Y+、Z2-是3种主族元素的离子,X+和Z2-具有相同的电子层结构,Y和Z处于同一周期,关于元素X、Y、Z的下列叙述中不正确的是 ( ) A、原子序数:X>Z>Y B、原子半径:Y>Z>X C、离子半径:Z2->X+>Y+ D、一定能形成化合物X2Z 14、已知下列分子或离子在酸性条件下都能氧化KI,自身发生如下变化 H2O2 → H2O IO3- → I MnO4- → Mn2+ HNO3 → NO 如果用等物质的量的这些物质氧化足量的KI,得到I2最多的是( ) A、H2O2 B、IO3- C、MnO4- D、HNO3 15、下列离子方程式书写正确的是( ) A、向漂白粉溶液中通入SO2气体:Ca2++2ClO-+SO2+H2O=CaSO3↓+2HClO B.、氢氧化钠溶液中通入过量的二氧化硫: C、 碳酸氢钙溶液中加足量的氢氧化钠溶液:Ca2++OH-+HCO3-==CaCO3↓+H2O D、稀硫酸和氢氧化钡溶液:Ba2++SO42-==BaSO4↓ 16 、某温度时 A.18 g≤m≤128g B.36 g<m<180g C.18 g<m<128g D.36 g≤m≤180g
17、 由10 g含有杂质的CaCO3和足量盐酸反应,产生了0.1 mol CO2,推断杂质的组成可能是( ) A.KHCO3和MgCO3 B.K2CO3和Na2CO3 C.MgCO3和Na2CO3 D.Na2CO3和BaCO3 18、 67 g过氧化钠吸收二氧化碳后,其质量增加到72.6 g,则被吸收的二氧化碳的 质量是( ) A.4.4 g B.8.8 g C.11.0 g D.16.4 g 19、下列说法正确的是( ) A、因为CO2通入水玻璃中可制取H2SiO3,说明H2CO3的酸性比H2SiO3强 B、因为SiO2和CaCO3固体混合加强热时,产生CO2气体,说明H2CO3的酸性比H2SiO3弱 C、SiO2既能溶于强碱溶液,又能和HF反应,故它是两性氧化物 D、因为玻璃中含SiO2,故玻璃试剂瓶不能盛装碱液
A.向饱和H2S溶液中通入过量的Cl2 B.向饱和H2S溶液中通入过量的SO2 C. 向饱和SO2溶液中通入过量的H2S D.向NaOH溶液中通入过量的Cl2 (第II卷)
(选择题答题拦)
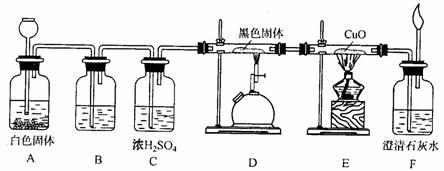
二、填空(共30分) 21、(4分)已知反应 8NH3 + 3Cl2 == 6NH4Cl + N2 ,若有42 g N2 生成,则: (1)有 克NH3参加反应 (2)被氧化的NH3 是 克。 22.(4分)实验室里盛放碱液的试剂瓶瓶塞不能用玻璃塞,是因为 (用离子反应方程式表示),检验生石灰里含有石英和石灰 石的方法是 23.(4分)已知氧和硫、氧化物和硫化物在化学性质上具有相似性,用化学方程式分别表示下列变化。 ⑴CS2与Na2S溶液一起振荡,溶液由无色变成有色:______________________________________________________ (2)Na2S2溶于足量稀盐酸中,产生浅黄色沉淀,并放出气体。 24.写出两个符合以下两个条件的置换反应①所涉及到的元素均为短周期元素②4种单质属于4个不同主族。______________________________________、 ______________________________________ 25、(9分)已知X、Y、Z都是短周期元素,它们的原子序数依次递增,X原子的电子层数与它的核外电子总数相同,而Z原子的最外层电子数是次外层的三倍,Y和Z可以形成两种以上的气态化合物。则: (1)、X是_______Y是_______Z是_______(填元素符号) (2)、由Y和Z组成,且Y和Z的质量比为7:20的化合物的化学式是_______。 (3)、由X、Y、Z中的两种元素组成,且与X2Z分子具有相同电子总数的两种离子是_______和_______。 (4)、X、Y、Z可以形成一种盐,此盐中X、Y、Z元素原子的个数比为4:2:3,该盐的化学式为_______。 26、(5分)用合适的试剂除去括号内的杂质。 (1)CO2(SO2)____________ (2)NaHCO3(Na2CO3) _____________ (3)FeCl3(FeCl2)_____________ (4)Fe2O3(Al2O3)_____________ (5)CO(CO2)_____________ 三、实验题(11分) 27、用下图组装实验可以研究CO的还原性:
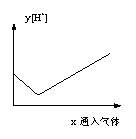
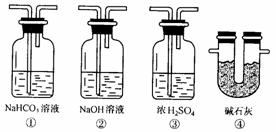
填写下列空白: (1)从A的长颈漏斗应加入的试剂是______________(填编号) A.稀硫酸 B.浓硫酸 C.稀盐酸 D.浓硝酸 (2)装置B中最适宜的试剂是_______ __。作用是_______ __。 (3)(2分)装置D中发生反应的化学方程式是____________________________________。 (4)装置E中发生的现象是___________________________ __________ (5)(2分)必须用装置C吸收除去气体中水蒸气的理由主要是_________________________。 (6)若根据F中石灰水变浑浊的现象也能确认CO具有还原性,应在图中装置______________与______________之间连接下图的哪一种装置______________(填编号)。
四、计算题(9分) 28、 3.2 g Cu与50 ml浓硫酸H2SO4 (足量)在加热的条件下充分反应。 (1)(2分)被还原的H2SO4物质的量为__________。 (2)(2分)若向50 ml浓度为a mol/L 浓硫酸中投入足量的铜片加热,充分加热后,被 还原的硫酸的物质的量n(H2SO4 )__________0.025a moL(填“<”、“>”或“=”) (3)(5分)把题干中反应后的溶液稀释至500 ml,取出50 ml,并向取出的溶液中加入足量的BaCl2 溶液中,得沉淀20.27 g,求原浓H2SO4的物质的量浓度? |
教育最重要的是使人变得更聪明。教育就是要开启人的心智,使人身体好,更主动、积极,行动能力强,更能干。
中文域名: 古今中外.com
英文域名: www.1-123.com
丰富实用的教育教学资料