高一化学三月月考
化学测试题
一 选择题[(每小题只有一个选项符合题意,每小题3分共54分)
1据报道,月球上有大量3He存在,以下关于3He的说法正确的是( )
A. 和4He的同原子 B. 比4He多一个中子
C. 是4He的同位素 D. 比4He少一个质子
2 下列关于原子的几种描述中,不正确的是( )
A. 18O与19F具有相同的中子数 B. 16O与17O具有相同的电子数
C. 12C与13C具有相同的质量数 D. 15N与14N具有相同的质子数
3 若用x代表一个中性原子中核外的电子数,y代表此原子的原子核内的质子数,z代表原子的原子核内的中子数,则对 ![]() 的原子来说 ( )
的原子来说 ( )
A. x=90 y=90 z=234 B. x=90 y=90 z=144
C. x=144 y=144 z=90 D. x=234 y=234 z=324
4 X,Y是元素周期表ⅦA族中的两种元素,下列叙述中能说明X的非金属性比Y强的是( )
A. X原子的电子层数比Y原子的电子层数多
B. X的氢化物的沸点比Y的氢化物的沸点低
C. X的气态氢化物比Y的气态氢化物稳定
D. Y的单质能将X从NaX的溶液中置换出来
5 2003年,IUPAC(国际纯粹与应用化学联合会)推荐原子序数为110的元素的符号为Ds,以纪念该元素的发现地(Darmstadt,德国)。下列关于Ds的说法不正确的是
A.Ds原子的电子层数为7 B.Ds是超铀元素
C.Ds原子的质量数为110 D.Ds为金属元素
6.A、B、C、D、E是同一周期的五种主族元素,A和B的最高价氧化物对应的水化物均呈碱性,且碱性B>A,C和D的气态氢化物的稳定性C>D;E是这五种元素中原子半径最小的元素,则它们的原子序数由小到大的顺序是( )
A.A、B、C、D、E B.E、C、D、B、A
C.B、A、D、C、E D.C、D、A、B、E
7、铊是超导材料的组成元素之一,铊在周期表中位于第六周期,与铝同主族元素,元素符号是TL,以下对铊的性质的推析不正确的是
A、铊是易导电的银白色金属 B、能生成 3价离子
C、氢氧化铊是两性氢氧化物 D、TL3 的氧化能力比Al3 强
8 X、Y、Z为短周期元素,这些元素原子的最外层电子数分别是1、4、6,则由这三种元素组成的化合物的化学式不可能是 ( )
A. XYZ B. X4YZ C. X4Y2Z2 D. X2YZ3
9下列物质中,既能与强酸又能与强碱反应的是 ( )
①Na2CO3 ②NaHCO3 ③Al2O3 ④Al(OH)3
A.①②③④ B.①②③ C.①②④ D.②③④
10已知X、Y均为1—18号之间的元素,X、Y可形成化合物X2Y和X2Y2,又知Y的原子序数小于X的原子序数,则这两种元素的原子序数之和为( )
A.19 B.18 C.16 D.9
11质量数为32,有16个中子的原子R,允许存在的粒子组是 ( )
A.R2 、RO2、RO3 B.R2-、RO2、RO3
C.R-、RO ![]() 、R2O
、R2O ![]() D.R 、RO、RO
D.R 、RO、RO ![]()
12下列叙述中,肯定a金属比b金属活泼性强的是 ( )
A.a原子的最外层电子数比B原子的最外层电子数少
B.a原子电子层数比b原子的电子层数多
C.1mol a 从酸中置换H 生成的H2比1 mol b从酸中置换H 生成的H2多
D.常温时,A能从水中置换出氢,而B不能
13.某元素原子的质量数为A,它的阴离子Xn-核外有x个电子,w克这种元素的原子核内中子数为( )
A. ![]() B.
B. ![]()
C. ![]() D.
D. ![]()
14.已知A的原子序数是x,B2-与A3 具有相同的电子层结构,则B元素的原子序数为( )
A. x 5 B. x-5 C. x 1 D. x-1
15已知反应KClO3 6HCl===KCl 3C12↑ 3H2O,若用K35ClO3和H37C1作用,则下列说法正确的是( )
A.该反应中转移电子数为6 B.KCl中只含有35C1
C.KCl中既有35Cl,又含37C1 D.生成的氯气式量约为73.3
16已知X、Y、Z、T四种非金属元素,X、Y在反应时各结合一个电子形成稳定结构所放出的能量是Y>X; 氢化物稳定性是HX>HT; 原子序数T>Z, 其稳定结构的离子核外电子数相等,而其离子半径是Z>T。四种元素的非金属性从强到弱排列顺序正确的是 ( )
A. X、Y、Z、T B. Y、X、Z、T
C. X、Y、T、Z D. Y、X、T、Z
17.X元素原子的L层比Y元素的L层少3个电子,X元素原子核外电子总数比Y元素原子核外电子 总数少5个,则X和Y可能形成的化合物是 ( )
A.离子化合物Y(XO4)2 B.离子化合物Y2X3
C.离子化合物Y3X2 D.共价化合物XY2
18.A元素的阳离子与B元素的阴离子具有相同的电子层结构,有关两元素有以下叙述:①原子半径A<B;②离子半径A>B;③原子序数A>B;④原子最外层电子数A≤B;⑤A的正价与B的负价绝对值一定相等。其中正确的是 ( )
A.①② B.③④ C.③⑤ D.③④⑤
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
二 填空题[本题共46分]
19、(9分)A、B两种离子具有相同的电子层结构,A、B两元素的单质都能与水剧烈反应,在反应中A单质为氧化剂,B单质为还原剂,则:
(1)A离子的结构示意图为______________,B原子的结构示意图为___________。
(2)A元素位于________周期___________族,新发现A的一种含氧酸的化学式为HAO,其中A的化合价为__________。
(3)A单质与水反应的化学方程式为
________________________________________。
(4)B单质与水反应的离子方程式为
________________________________________。
20、(11分)A、B、C、D四种元素都是短周期元素,A元素的离子具有黄色的焰色反应。B元素的离子结构和Ne具有相同的电子层排布;5.8 g B的氢氧化物恰好能与100 mL 2 mol·L—1盐酸完全反应;B原子核中质子数和中子数相等。H2在C单质中燃烧产生苍白色火焰。D元素原子的电子层结构中,最外层电子数是次外层电子数的3倍。根据上述条件回答:
(1)元素C位于第__________周期第__________族,它的最高价氧化物的化学式为____________。
(2)A元素是___________,B元素是___________,D元素是__________。
(3)A与D形成稳定化合物的化学式是_____________,判断该化合物在空气中是否变质的简单方法是
___________________________________________________。
(4)C元素的单质有毒,可用A的最高价氧化物对应的水化物的溶液吸收,其离子方程式为
21、(11分)已知五种元素的原子序数的大小顺序为C>A>B>D>E,A、C同周期,B、C同主族。A与B形成离子化合物A2B,A2B中所有离子的电子数相同,其电子总数为30;D和E可形成4核10个电子分子。试回答下列问题:
(1)、写出五种元素的元素符号:A__________、B_________、C____________、D__________、E________________。
(2)、用电子式表示离子化合物A2B的形成过程:
_____________________________。
(3)、写出下列物质的电子式:
1) D 形成分子________________________________-______
2)C、E形成的化合物:____________________________________
3)A、B、E形成的化合物______________________________
4)D、E形成的化合物__________________________。
22[15分]有A、B、C、D、E五种元素, 它们的原子序数由A至E逐渐增大。
D 的氢化物的分子式为H2D;D的最高氧化物中D的质量分数为40%,且D原子
的原子核中质子数和中子数相等。A原子最外电子层有4个电子。B的阴离子与
C的阳离子和氖原子的电子层结构相同。 E原子的M电子层上共有6个电子。常
温常压下,B单质是气体,已知0.1 mol的B 单质与H2完全反应需2.408×1023 个
氢原子。C单质在加热条件下与B单质反应生成淡黄色固体。根据上述情况,试
回答下列各问题:
(1)、A—E的元素符号为:______、______、______、______、______。
(2) C位于元素周期表中第_____周期、第______族,其阳离子的结构示意图为______。
(3) D原子的电子式为____________;E离子的符号为________。
(4) A元素与其余4种元素形成化合物的化学式为(仅限于由两种元素组成)_______、______、_______、_______。
(5) C单质和B单质在加热条件下生成A2B2反应的化学方程式_________________反应中________为氧化剂;________为还原剂。
(6) 1.15 g的C单质溶于50 mL水中,所得溶液中溶质的质量分数为_____________。
12. (1)C O Na S Cl (2)第三周期 ⅠA ![]() (3)
(3) ![]() Fe2 (4)CO CO2 CS2 CCl4 (5)2Na+O2=Na2O2 O2 Na (6)3.91%
Fe2 (4)CO CO2 CS2 CCl4 (5)2Na+O2=Na2O2 O2 Na (6)3.91%
1C,2C,3B,4C,5C,6D,7C,8A,9D,10A,11B,12D,13D,14D,15D,16,D [每小题3分,共48分]
17, (1)H、Cl、Mg、S
 (2)Cl、S、
(2)Cl、S、

(3)H、Cl、6种 11H3517Cl
(4)H2O、Cl2O7、MgO、SO3 [每空1分共14分]
18(1)HCl 弱 (2)N; ![]() (3)H、O、S (注:带结晶水的硫酸盐)
(3)H、O、S (注:带结晶水的硫酸盐)
(4)Be(OH)2+2NaOH → Na2BeO2+2H2O;Li [方程式2分,其余1分一空,共8分]
19, SO42- [2分]
20(1)① H2 ② NH3+HCl=NH4Cl
(2)① SO2 ② H2S+OH-=HS-+H2O ③ S+3Cl2+4H2O=H2SO4+6HCl [1分一空,共5分]
21 Si;第三周期,IVA 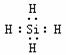 [每空一分共4分]
[每空一分共4分]
22 (1)C O Na S Cl
(2)第三周期 ⅠA ![]()
(3) ![]() Cl-
Cl-
(4)CO CO2 CS2 CCl4
(5)2Na+O2=Na2O2 O2 Na (6)3.91% [最后计算2分,其余一分一空,共19分]
