高一化学上册第一次月考试题
化学试题
说明:
1. 本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分,共100分。考试时间90分钟。
2. 请将全部答案填到答题卷中。
可能用到的相对原子质量:
H 1 C 12 O 16 Ne 20 Na 23 Cl 35.5 Mn 55
第Ⅰ卷 (选择题 共40分)
在下列各题的四个选项中只有一个符合题目要求的。
1. 容量瓶是用来配制物质的量浓度的溶液的定量仪器,其上标有:①温度、②浓度、③容量、④压强、⑤刻度线、⑥酸式或碱式 这六项中的
A.①③⑤ B.②④⑥
C.①②④ D.③⑤⑥
2. 下列物质中属于纯净物、化合物、无机化合物、盐、钙盐的是
A.石灰石 B.Ca(OH)2
C.CaCO3 D.CH4
3. 下列各组物质中都属于纯净物的一组是
A.液态氧 汽水
B.洁净的空气 纯净的盐酸
C.冰水混合物 干冰
D.铁矿石 金刚石
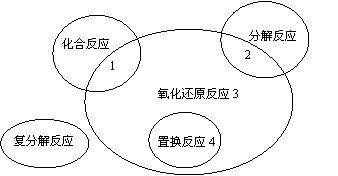
4.
|
复分解反应 |
|
化合反应 |
|
1 |
|
2 |
|
置换反应4 |
|
氧化还原反应3 |
|
分解反应 |
 将下列各组物质按酸、碱、盐分类顺次排列。正确的
将下列各组物质按酸、碱、盐分类顺次排列。正确的A.H2SO4,Cu2(OH)2CO3,CuSO4
B.H2S,Ba(OH)2,NH4NO3
C.HNO3,C2H5OH,Na2CO3
D.NaHSO4,Fe(OH)3,NaCl
5. 想一想: HCl(气态)、CH3COOH(液态)、Ba(OH)2(固态)、CuSO4(固态)这些物质为什么归为一类,下列哪些物质还可以和它们归为一类
A.C2H5OH溶液 B.Na2CO3·10H2O
C.水煤气 D.豆浆
6. 下列有关氧化—还原反应的叙述错误的是
A.在反应中不一定所有元素的化合价都发生变化
B.化合反应和分解反应不可能有氧化—还原反应
C.置换反应一定属于氧化—还原反应
D.复分解反应不可能有氧化—还原反应
7. 下列各组分散系,按分散质粒子由大到小顺序排列的是
A.溶液、胶体、浊液 B.胶体、浊液、溶液
C.浊液、胶体、溶液 D.浊液、溶液、胶体
8. 下列各组分散系,需用丁达尔效应区分的是
A.溶液与浊液 B.胶体与胶体
C.溶液与胶体 D.溶液与溶液
9. 将饱和FeCl3溶液分别滴入下述溶液或水中,能形成胶体的是
A.冷水 B.煮沸的蒸馏水
C.NaOH浓溶液 D.NaCl浓溶液
10. 下列各组分散系的分散质粒子一定能通过半透膜的是:
①过滤后的天然水 ②变浑浊的石灰水 ③石蕊试液 ④牛奶 ⑤盐酸 ⑥碘酒 ⑦淀粉溶液 ⑧墨水
A.①③⑦ B.除②④外
C.③⑤⑥ D.①③⑤⑥
11.
|
A.Cl2+2KBr
B.2NaHCO3
C.4Fe(OH)2 O2 2H2O
D.2Na2O2 2CO2
12. 下列物质按照化合物、混合物、电解质和非电解质顺序排列的是
A.纯盐酸、水煤气、硫酸、五氧化二磷
B.冰醋酸(CH3COOH)、浓硫酸、碳酸钡、乙醇
C.臭氧(O3)、天然气、氧化钾、蔗糖
D.胆矾(CuSO4•5H2O)、石灰水、苛性钠、氯气
13. 有关电解质的说法正确的是
A.液态氯化氢不能导电,所以氯化氢是非电解质
B.SO3水溶液的导电性很好,所以SO3是电解质
C.液态的铜导电性很好,所以铜是电解质
D.Na2O液态时能导电,所以Na2O是电解质
14. 在NaCl、MgCl2、MgSO4形成的混合溶液中:
c(Na )=0.1 mol·L—1,c(Mg2 )=0.25 mol·L—1,c(Cl-)=0.2 mol·L—1,则c(SO42-)为
A.0.10 mol·L—1 B.0.15 mol·L—1
C.0.20 mol·L—1 D.0.25 mol·L—1
15. 下列说法正确的是
A.摩尔是7个基本物理量之—
B.阿伏加德罗常数是12g碳中所含的碳原子数
C.1 mol OH-的质量是17 g·mol—1
D.非标况下1 mol某气体的体积也有可能为22.4L
16. 下列数量的物质:①0.45 mol 氧气 ②4℃时7.2mL水③10 g 氖气④标准状况下4.48L CH4 所含原子数由大到小顺序排列的是
A.②④①③ B.④①③②
C.④③②① D.③①②④
17. 科学家已发现一种新型分子,其分子式是H3,在相同条件下,等质量的H2和H3具有相同的
A.原子数 B.分子数
C.体积 D.物质的量
18. 下列溶液中物质的量浓度为l.00 mol·L—1的是
A.将40 g NaOH溶解于1 L水中
B.将22.4 L氯化氢气体溶于水配成1 L溶液
C.将1 L l0 mol·L—1的浓盐酸与9 L水混合
D.将10g NaOH溶解在水中配成250 mL溶液
19. 配制一定物质的量浓度的氯化钠溶液时,出现下列情况,肯定不必重新配制的是
A.转移溶液时不慎溅出数滴
B.加蒸馏水时不慎溅出数滴
C.加蒸馏水时不慎超过了刻度线
D.摇匀时有少量液体流出
20. 配制一定物质的量浓度的NaOH溶液时,造成最终浓度偏低的原因可能是
①称量时已观察到NaOH吸水
②容量瓶事先未烘干
③移液时有少量液体流出
④未洗净烧杯或玻璃棒
⑤未恢复到室温即转移定容
⑥定容时观察刻度线俯视
⑦定容摇匀后液面恰好与刻度线相切
⑧转移溶液时玻璃棒靠在刻度线上方
A.①②③④ B.①③④⑦⑧
C.①③⑤⑦ D.①②④⑥⑧
第Ⅱ卷 (非选择题 共60分)
21. (4分)下列各组物质中均有一种物质的类别与其它3种不同
A.CaO、Na2O、CO2、CuO
B.H2、C、P、Cu
C.O2、Fe、Cu、Zn
D.HCl、H2O、H2SO4、HNO3
则这4种物质依次是(填化学式):
A ;B ;C ;D 。
22. 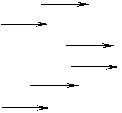 (9分)有A、B、C、D四种物质,它们可能是四氧化三铁、稀硫酸、硫酸铜溶液和水等物质中的一种。另有甲、乙、丙、丁四种气体,它们可能是二氧化碳、氧气、氢气和一氧化碳等四种气体中的一种,其中丁气体能使澄清的石灰水变浑浊。各气体与物质间有如下所示的反应和变化关系:
(9分)有A、B、C、D四种物质,它们可能是四氧化三铁、稀硫酸、硫酸铜溶液和水等物质中的一种。另有甲、乙、丙、丁四种气体,它们可能是二氧化碳、氧气、氢气和一氧化碳等四种气体中的一种,其中丁气体能使澄清的石灰水变浑浊。各气体与物质间有如下所示的反应和变化关系:
①铁 甲(气) B(黑色固体)
②铁 C 硫酸亚铁 乙(气)
③乙(气) 甲(气) A
④丙(气) 甲(气) 丁(气)
⑤B 丙(气) 铁 丁(气)
⑥铁 D 硫酸亚铁 铜
(1)试推断A、B、C、D和甲、乙、丙、丁各是何物质,写出指定物质的化学式。A:
C: D: ;甲: 乙: 。
(2)写出反应⑤的化学方程式:
。
(3)上述反应中属于置换反应的是 。
23. (6分)写出下列物质的电离方程式:
(1)HNO3 。
(2)Ba(OH)2 。
(3)NaHSO4 。
(4)(NH4)3PO4 。
(5)K2CO3 。
(6)Fe2(SO4)3 。
24. 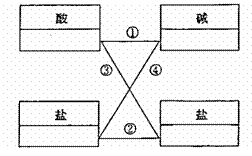 (8分)从稀盐酸、稀硫酸、石灰水、烧碱溶液、氢氧化钡溶液、氯化钠溶液、纯碱溶液、氯化钡溶液八种物质中,选出四种物质,使得图示中各线条相连的物质均能反应生成沉淀。将选出物质的化学式填写在图示相应的方框里,并写出③、④两步反应的化学方程式。
(8分)从稀盐酸、稀硫酸、石灰水、烧碱溶液、氢氧化钡溶液、氯化钠溶液、纯碱溶液、氯化钡溶液八种物质中,选出四种物质,使得图示中各线条相连的物质均能反应生成沉淀。将选出物质的化学式填写在图示相应的方框里,并写出③、④两步反应的化学方程式。
③ ;
④ 。
25. ![]() (5分)
(5分) ![]() 下列反应中,不是氧化还原反应的是 ;属于氧化还原反应的,请找出在反应中化合价发生变化的元素,并将其反应前后的化合价标在元素符号的正上方
下列反应中,不是氧化还原反应的是 ;属于氧化还原反应的,请找出在反应中化合价发生变化的元素,并将其反应前后的化合价标在元素符号的正上方
7 -2 6 4 0
例:2KMnO4 K2MnO4 MnO2 O2↑
①2FeCl2 Cl2 2FeCl3
②Na2CO3 2HCl 2NaCl H2O CO2↑
③C H2O ![]() CO H2
CO H2
④CuO 2HNO3 Cu(NO3)2 H2O
⑤MnO2 4HCl(浓) MnCl2 Cl2↑ 2H2O
26. (8分)某学生用溶质质量分数为98%、密度为1.84 g·cm—3的浓硫酸,配制0.3mol/L的硫酸溶液500mL。试回答下列问题:
(1)计算所需浓硫酸的体积 (计算结果保留到小数点后1位)。
(2)从下列用品中选出该实验一定要用的仪器
(填序号)。
A.1000mL烧杯 B.250mL烧杯 C.漏斗
D.10mL量筒 E.100mL量筒 F.500mL容量瓶
G.1000mL容量瓶 H.500mL烧瓶 I.托盘天平
除选用上述仪器外,尚缺少的必要仪器或用品是 。
(3)该学生根据计算结果,进行如下实验操作:
①用量筒量取计算所需体积的浓硫酸;
②向量筒中加入少量蒸馏水,并用玻璃棒搅拌;
③立即将稀释后的溶液转入容量瓶中;
④然后将蒸馏水注入容量瓶直至刻度线;
⑤把容量瓶盖盖紧,再振荡摇匀;
⑥定容摇匀后液面下降又补加水。
你认为上述实验操作中正确的是 (用编号表示)。
27. (10分)(1)含有9 NA个电子的 ![]() 质量为
质量为
kg,其中含有 mol质子; 个中子。
(2)标准状况下448mL某气体的质量为1.28g,该气体的摩尔质量约为 。
(3)1.0L含9.03×1023个Cl—的AlCl3溶液的物质的量浓度为 。
(4)同温、同压下,某瓶充满O2时质量为116g,充满CO2时质量为122g,充满A时为114g,则A的相对分子质量为 。
28. (10分,要求写出规范的解题过程)
(1)36.5%的浓盐酸,密度为1.19 g·cm—3,求其物质的量浓度?(列出计算式)
(2)实验室里常用浓盐酸与二氧化锰反应来制取少量的氯气,反应的化学方程式为:
MnO2 4HCl(浓) ![]() MnCl2 Cl2 2H2O。
MnCl2 Cl2 2H2O。
若产生的氯气在标况下的体积为11.2L,试计算:
①参加反应的MnO2的质量。
②参加反应的HCl的物质的量。
高一第一次月考
化学试题参考答案
第Ⅰ卷 (选择题 共40分)
1.A 2.C 3.C 4.B 5.B 6.B 7.A
8.C 9.B 10.C 11.D 12.B 13.D 14.C
15.D 16.A 17.A 18.D 19.B 20.B
第Ⅱ卷 (非选择题 共60分)
21.(4分)
A.CO2;B.Cu;C.O2 ;D.H2O
|
(1)A: H2O B: Fe3O4 C: H2SO4 D: CuSO4
甲: O2 乙: H2 丙: CO 丁: CO2
(2) Fe3O4 4CO
(3)②⑥
23.(6分)略
24.(8分)
H2SO4、Ba(OH)2、Na2CO3、BaCl2、
③H2SO4 BaCl2 BaSO4↓ 2HCl
④H2SO4 Na2CO3 Na2SO4 H2O CO2↑
25.(5分)②③ 其余略
26.(8分)
(1)8.1ml
(2)BDF; 胶头滴管 玻璃棒
(3)①⑤
27.(9分)
(1)0.018 kg 9mol 9 NA
(2)64g ·mol—1、
(3)0.5 mol·L—1
(4)28
28.(10分)
(1)11.9mol·L—1
(2)①43.5g ②2 mol
