|
ΗΏ“ΜΜ·―ß…œ≤αΒΎ“Μ¥Έ‘¬ΩΦ ‘Ψμ
2008.10.7
Ω…Ρή”ΟΒΫΒΡœύΕ‘‘≠Ή”÷ ΝΩΘΚHΓΣ1 OΓΣ16 NΓΣ14 SΓΣ32 ClΓΣ35.5 CΓΣ12 NaΓΣ23
ΒΎΔώΨμΘ®―Γ‘ώΧβΘ§Ι≤52Ζ÷Θ©
 “ΜΓΔ―Γ‘ώΧβΘ®÷Μ”–1Ηω’ΐ»Ζ¥πΑΗΘΜΙ≤10–ΓΧβΘ§ΟΩ–ΓΧβ2Ζ÷Θ§Ι≤20Ζ÷ΓΘΘ© “ΜΓΔ―Γ‘ώΧβΘ®÷Μ”–1Ηω’ΐ»Ζ¥πΑΗΘΜΙ≤10–ΓΧβΘ§ΟΩ–ΓΧβ2Ζ÷Θ§Ι≤20Ζ÷ΓΘΘ©
1.”Ο»γΆΦΥυ ΨΒΡΖΫΖ®―–ΨΩΡ≥ΤχΧεΒΡ–‘÷ Θ§’β÷÷ΖΫΖ® τ”Ύ
A. Β―ιΖ® B.Ιέ≤λΖ® C.Ζ÷άύΖ® D.±»ΫœΖ®
2Θ°“‘œ¬ «“Μ–©≥Θ”ΟΒΡΈΘœ’ΤΖ±ξ÷ΨΘ§ΉΑ‘Υ““¥ΦΒΡΑϋΉΑœδ”ΠΧυΒΡΆΦ±ξ «
A B C D
3. Β―ι ““Σ”ΟΙΧΧ嬻̷ΡΤ ‘ΦΝΉΦ»Ζ≈δ÷Τ0.5 L 0.2 molΓΛL-1ΒΡNaCl»ή“ΚΘ§œ¬Ν–ΡΡ÷÷“«Τς≤Μ «±Ί–κ Ι”ΟΒΡ
A.500 mL»ίΝΩΤΩ B.ΫΚΆΖΒΈΙή C. ‘Ιή D.Ά–≈ΧΧλΤΫ
4Θ° Β―ι÷–ΒΡœ¬Ν–≤ΌΉς’ΐ»ΖΒΡ «
AΘ°”Ο ‘Ιή»Γ≥ω ‘ΦΝΤΩ÷–ΒΡNa2CO3»ή“ΚΘ§ΖΔœ÷»ΓΝΩΙΐΕύΘ§ΈΣΝΥ≤ΜάΥΖ―Θ§”÷Α―ΙΐΝΩΒΡ ‘ΦΝΒΙ»κ ‘ΦΝΤΩ÷–
BΘ°Ba(NO3)2 »ή”ΎΥ°Θ§Ω…ΫΪΚ§”–Ba(NO3)2 ΒΡΖœ“ΚΒΙ»κΥ°≤έ÷–Θ§‘Ό”ΟΥ°≥ε»κœ¬Υ°Βά
CΘ°”Ο’τΖΔΖΫΖ® ΙNaCl ¥”»ή“Κ÷–Έω≥ω ±Θ§”ΠΫΪ’τΖΔΟσ÷–NaCl »ή“Κ»Ϊ≤ΩΦ”»»’τΗ…
DΘ°”Ο≈®ΝρΥα≈δ÷Τ“ΜΕ®Έο÷ ΒΡΝΩ≈®Ε»ΒΡœΓΝρΥα ±Θ§≈®ΝρΥα»ή”ΎΥ°ΚσΘ§”Πά以÷Ν “Έ¬≤≈ΡήΉΣ“ΤΒΫ»ίΝΩΤΩ÷–
5Θ°œ¬Ν––π ω’ΐ»ΖΒΡ «
AΘ°1 mol H2OΒΡ÷ ΝΩΈΣ18g/mol BΘ°CH4ΒΡΡΠΕϊ÷ ΝΩΈΣ16g
CΘ°3.01ΓΝ1023ΗωSO2Ζ÷Ή”ΒΡ÷ ΝΩΈΣ32g DΘ°±ξΉΦΉ¥Ωωœ¬,1 mol»ΈΚΈΈο÷ ΧεΜΐΨυΈΣ22.4L
6.‘Ύ≈δ÷ΤΈο÷ ΒΡΝΩ≈®Ε»»ή“ΚΒΡ Β―ι÷–Θ§ΉνΚσ”ΟΫΚΆΖΒΈΙήΕ®»ίΚσΘ§“ΚΟφ’ΐ»ΖΒΡ «
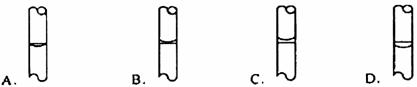
7Θ°ΩΤ―ßΦ““―ΖΔœ÷“Μ÷÷–¬–Ά«βΖ÷Ή”Θ§ΤδΜ·―ß ΫΈΣH3Θ§‘ΎœύΆ§ΧθΦΰœ¬Θ§Β»÷ ΝΩΒΡH3ΚΆH2œύΆ§ΒΡ «
AΘ°‘≠Ή” ΐ BΘ°Ζ÷Ή” ΐ CΘ°ΧεΜΐ DΘ°Έο÷ ΒΡΝΩ
8Θ°Ά§Έ¬Ά§―Ιœ¬Θ§Β»÷ ΝΩΒΡœ¬Ν–ΤχΧεΥυ’Φ”–ΒΡΧεΜΐΉν¥σΒΡ «
AΘ°O2 BΘ°CH4 CΘ°CO2 DΘ°SO2
9Θ°÷Μ”Ο“Μ÷÷ ‘ΦΝΨΆΡήΫΪBaCl2ΓΔNaClΓΔKOH»ΐ÷÷Έό…Ϊ»ή“Κ«χ±πΩΣΘ§¥Υ ‘ΦΝ «
A.Na2CO3 B. ―ΈΥα C. ΝρΥα D.Fe2(SO4)3»ή“Κ
10Θ°Ά§Έ¬Ά§―Ιœ¬Θ§1ΧεΜΐX2ΤχΧε”κ3ΧεΜΐY2ΤχΧεΜ·Κœ…ζ≥…2ΧεΜΐΤχΧεΜ·ΚœΈοΘ§‘ρΗΟΜ·ΚœΈοΒΡΜ·―ß ΫΈΣ
A.XY3 B.XY C.X3Y D.X2Y3
ΕΰΓΔ―Γ‘ώΧβΘ®”–1-2Ηω¥πΑΗΘ§÷Μ”–“ΜΗω’ΐ»Ζ―ΓœνΒΡΘ§Εύ―Γ≤ΜΗχΖ÷ΘΜ”–ΝΫΗω’ΐ»Ζ―ΓœνΒΡΘ§―ΓΕ‘“ΜΗωΗχ2Ζ÷Θ§―Γ¥μ“ΜΗωΗΟ–ΓΧβ≤ΜΗχΖ÷ΓΘΙ≤8–ΓΧβΘ§ΟΩ–ΓΧβ4Ζ÷Θ§ΦΤ32Ζ÷ΓΘΘ©
11Θ°œ¬Ν––π ω’ΐ»ΖΒΡ «
AΘ°Ά§Έ¬Ά§―Ιœ¬Θ§œύΆ§ΧεΜΐΒΡΈο÷ Θ§ΤδΈο÷ ΒΡΝΩ“ΜΕ®œύΒ»
BΘ°»ΈΚΈΧθΦΰœ¬Θ§Β»Έο÷ ΒΡΝΩΒΡΦΉΆιΚΆ“Μ―θΜ·ΧΦΥυΚ§ΒΡΖ÷Ή” ΐ“ΜΕ®œύΒ»
CΘ°1L“Μ―θΜ·ΧΦΤχΧε“ΜΕ®±»1L―θΤχΒΡ÷ ΝΩ–Γ
DΘ°œύΆ§ΧθΦΰœ¬ΒΡ“Μ―θΜ·ΧΦΤχΧεΚΆΒΣΤχΘ§»τΧεΜΐœύΒ»Θ§‘ρ÷ ΝΩ“ΜΕ®œύΒ»
12.…ηNA±μ ΨΑΔΖϋΦ”Β¬¬ό≥Θ ΐΘ§œ¬Ν––π ω÷–’ΐ»ΖΒΡ «
A.≥ΘΈ¬≥Θ―Ιœ¬Θ§11.2 L―θΤχΥυΚ§ΒΡ‘≠Ή” ΐΈΣNA
B.1.8 gΒΡNH 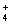 άκΉ”÷–Κ§”–ΒΡΒγΉ” ΐΈΣ10NA άκΉ”÷–Κ§”–ΒΡΒγΉ” ΐΈΣ10NA
C.≥ΘΈ¬≥Θ―Ιœ¬Θ§48 g O3Κ§”–ΒΡ―θ‘≠Ή” ΐΈΣ3NA
D.2.4 gΫπ τΟΨ±δΈΣΟΨάκΉ” ± ß»ΞΒΡΒγΉ” ΐΈΣ0.1NA
13œ¬Ν–Ε‘”ΎΓΑΡΠΕϊΓ±ΒΡάμΫβ’ΐ»ΖΒΡ «
AΘ°ΡΠΕϊ «ΙζΦ ΩΤ―ßΫγΫ®“ι≤…”ΟΒΡ“Μ÷÷ΈοάμΝΩ
BΘ°ΡΠΕϊ «Έο÷ ΒΡΝΩΒΡΒΞΈΜΘ§Φρ≥ΤΡΠΘ§ΖϊΚ≈ΈΣmol
CΘ°ΡΠΕϊΩ…“‘Α―Έο÷ ΒΡΚξΙέ ΐΝΩ”κΈΔΙέΝΘΉ”ΒΡ ΐΝΩΝΣœΒΤπά¥
DΘ°ΙζΦ …œΙφΕ®Θ§0.012kgΧΦ‘≠Ή”ΥυΚ§”–ΒΡΧΦ‘≠Ή” ΐΡΩΈΣ1ΡΠ
14Θ°PH ‘÷Ϋ≤βΕ®»ή“ΚpHΒΡ’ΐ»Ζ≤ΌΉς «ΘΚ
AΘ°ΫΪ“Μ–ΓΩι ‘÷ΫΖ≈‘Ύ±μΟφΟσ…œΘ§”Ο≤ΘΝßΑτ’Κ»Γ…ΌΝΩ¥ΐ≤β“ΚΒψ‘Ύ ‘÷Ϋ…œΘ§‘Ό”κ±ξΉΦ±»
…ΪΩ®Ε‘’’
BΘ°ΫΪ“Μ–ΓΩι ‘÷Ϋ”Ο’τΝσΥ°»σ ΣΚσΖ≈‘Ύ±μΟφΟσ…œΘ§”Ο≤ΘΝßΑτ’Κ»Γ…ΌΝΩ¥ΐ≤β“ΚΒψ‘Ύ ‘÷Ϋ
…œΘ§‘Ό”κ±ξΉΦ±»…ΪΩ®Ε‘’’
CΘ°ΫΪ“Μ–ΓΧθ ‘÷Ϋ‘Ύ¥ΐ≤β“Κ÷–’Κ“Μœ¬Θ§»Γ≥ωΚσΖ≈‘Ύ±μΟφΟσ…œΘ§”κ±ξΉΦ±»…ΪΩ®Ε‘’’
DΘ°ΫΪ“Μ–ΓΧθ ‘÷Ϋœ»”Ο’τΝσΥ°»σ ΣΚσΘ§‘Ύ¥ΐ≤β“Κ÷–’Κ“Μœ¬Θ§»Γ≥ωΚσ”κ±ξΉΦ±»…ΪΩ®Ε‘’’
15.…ηNA¥ζ±μΑΔΖϋΦ”Β¬¬ό≥Θ ΐΘ§œ¬Ν–ΥΒΖ®’ΐ»ΖΒΡ «
A.22.4 L COΚΆCO2ΒΡΜλΚœΤχΧε÷–ΥυΚ§ΒΡΧΦ‘≠Ή” ΐ“ΜΕ® «NA
B.Κ§1 mol HClΒΡ―ΈΥα»ή“Κ”κΉψΝΩFeΖ¥”ΠΘ§FeΥυ ß»ΞΒΡΒγΉ”Ήή ΐΈΣ2NA
|
―ß–Θ ΑύΦΕΘΚ_________ ―ßΚ≈ΘΚ_______________ –’ΟϊΘΚ_____________________ |
   C.≥ΘΈ¬≥Θ―Ιœ¬Θ§32 g O2ΚΆ32 g O3ΥυΚ§―θ‘≠Ή” ΐΕΦ «2NA C.≥ΘΈ¬≥Θ―Ιœ¬Θ§32 g O2ΚΆ32 g O3ΥυΚ§―θ‘≠Ή” ΐΕΦ «2NA
D.±ξΉΦΉ¥Ωωœ¬Θ§11.2 L H2OΚ§”–0.5NAΖ÷Ή”
16.»γΙϊa gΡ≥ΤχΧε÷–Κ§”–ΒΡΖ÷Ή” ΐΈΣbΘ§‘ρc gΗΟΤχΧε‘Ύ±ξΉΦΉ¥Ωωœ¬ΒΡΧεΜΐ «
A. 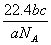 L B. L B. 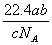 C. C. 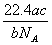 L D. L D.  L L
17.‘Ύ0.5 LΡ≥≈®Ε»ΒΡNaCl»ή“Κ÷–Κ§”–0.5 mol Na Θ§œ¬Ν–Ε‘ΗΟ»ή“ΚΒΡΥΒΖ®÷–Θ§≤Μ’ΐ»ΖΒΡ «
A.ΗΟ»ή“ΚΒΡΈο÷ ΒΡΝΩ≈®Ε»ΈΣ1 molΓΛL-1 B.ΗΟ»ή“Κ÷–Κ§”–58.5 g NaCl
C.≈δ÷Τ100 mLΗΟ»ή“Κ–η”Ο5.85 g NaCl
D.ΝΩ»Γ100 mLΗΟ»ή“ΚΒΙ»κ…’±≠÷–Θ§…’±≠÷–Na ΒΡΈο÷ ΒΡΝΩΈΣ0.1 mol
18.AΓΔBΓΔCΓΔDΥΡ÷÷Έο÷ Ψυ“Ή»ή”ΎΥ°Θ§Ζ÷±πΑ¥œ¬Ν–ΧθΦΰ≈δ≥…»ή“ΚΘ§Τδ÷–Έο÷ ΒΡΝΩ≈®Ε»Ήν¥σΒΡ «
A.10 mL 5molΓΛL-1ΒΡA»ή“ΚΦ”Υ°≈δ÷Τ≥…100 mL»ή“Κ
B.9.2 g BΈο÷ Θ® ΫΝΩΈΣ46Θ©»ή”ΎΥ°≈δ≥…100 mL»ή“Κ
C.1.806ΓΝ1023ΗωCΒΡΖ÷Ή”»ή”ΎΥ°≈δ≥…100 mL»ή“Κ
D.0.1 moL DΈο÷ »ή”Ύ100 mL 2.5 molΓΛL-1ΒΡD»ή“Κ÷–
ΒΎΔρΨμΘ®Ζ«―Γ‘ώΧβΘ§Ι≤48Ζ÷Θ©
»ΐΓΔ Β―ιΧβΘ®±ΨΧβΑϋά®2–ΓΧβΘ§Ι≤29Ζ÷Θ©
19.(15Ζ÷) ‘ΜΊ¥πœ¬Ν–÷–―ßΜ·―ß Β―ι “÷–≥ΘΦϊ“«ΤςΒΡ”–ΙΊΈ ΧβΘΚ
Θ®1Θ©‘Ύ“«ΤςΔΌΖ÷“Κ¬©ΕΖΓΔΔΎ ‘ΦΝΤΩΓΔΔέΦ·ΤχΤΩΓΔΔήΒΈΤΩΓΔΔίΆ–≈ΧΧλΤΫΓΔΔό»ίΝΩΤΩΓΔΔΏΝΩΆ≤ΓΔ÷–Θ§±ξ”–ΓΑ0Γ±ΩΧΕ»ΒΡ «Θ®Χν–ρΚ≈Θ§œ¬Ά§Θ©_________ _________ΘΜ
±ξ”– Ι”ΟΈ¬Ε»ΒΡ“«Τς «___________ ______________ΓΘ
Θ®2Θ©ΓΑΡΞ…ΑΓ± «‘ωΦ”≤ΘΝß“«ΤςΟήΖβ–‘ΒΡ“Μ÷÷¥ΠάμΙΛ“’ΓΘ‘Ύ“«Τς ΔΌ ‘ΙήΓΔΔΎΖ÷“Κ¬©ΕΖΓΔΔέœΗΩΎ ‘ΦΝΤΩΓΔΔήΙψΩΎ ‘ΦΝΤΩΓΔΔίΦ·ΤχΤΩΓΔΔόΒΈΤΩ÷–Θ§”ΟΒΫΓΑΡΞ…ΑΓ±ΒΡ”–________________ΓΘ
Θ®3Θ©‘Ύ“«ΤςΔΌ¬©ΕΖΓΔΔΎ»ίΝΩΤΩΓΔΔέ’τΝσ…’ΤΩΓΔΔήΖ÷“Κ¬©ΕΖΓΔΔί…’±≠ΓΔΔό’τΖΔΟσ ÷–Θ§Ω…”Ο”Ύ¥÷―ΈΧα¥Ω Β―ιΒΡ”– ΘΜΩ…”Ο”ΎΖ÷άκΝΫ÷÷Ζ–ΒψΫ”Ϋϋ«“ΜΞ≤Μœύ»ήΒΡ“ΚΧ§ΜλΚœΈο Β―ιΒΡ”– ΓΘ
20Θ°(14Ζ÷)≈δ÷Τ0.25molΓΛLΘ≠1ΒΡNaOH»ή“Κ100mLΘ§Ρ≥―ß…ζ≤ΌΉς»γœ¬ΘΚΔΌ”ΟΆ–≈ΧΧλΤΫ≥Τ≥ω1.00g«β―θΜ·ΡΤΘΚΫΪΧλΤΫΒςΚΟΝψΒψΘ§‘Ό‘ΎΝΫ≈Χ…œΗς»Γ“Μ’≈Ά§―υ÷ ΝΩΒΡ÷ΫΘ§Α―”Έ¬κΒςΒΫ1.00gΒΡΈΜ÷Ο…œΘ§”ΎΉσ≈ΧΖ≈ΝΘΉ¥«β―θΜ·ΡΤ÷ΝΧλΤΫΤΫΚβΘ§»Γœ¬≥ΤΚΟΒΡ«β―θΜ·ΡΤΘ§≤Δ≥ΖΒτΝΫ≈Χ…œΒΡ÷ΫΓΘΔΎΑ―≥ΤΚΟΒΡ«β―θΜ·ΡΤΖ≈»κ“Μ÷Μ100mLΒΡ…’±≠÷–Θ§Φ”»κ‘Φ10mLΥ°Θ§ΫΝΑη Ι÷°»ήΫβΘ§»ήΫβΚσΝΔΦ¥”Ο≤ΘΝßΑτ“ΐΝςΫΪ»ή“Κ“Τ÷Ν“Μ÷Μ100mLΒΡ»ίΝΩΤΩΡΎΘ§Φ”Υ°÷ΝάκΩΧΕ»œΏ‘Φ2cm¥ΠΘ§”ΟΒΈΙήΦ”Υ°÷ΝΩΧΕ»œΏΓΘΔέ–¥≥ω“ΜΗω±ξ”–≈δ÷Τ»’ΤΎΒΡΓΑ0.25molΓΛLΘ≠1NaOH»ή“ΚΓ±ΒΡ±ξ«©Θ§Χυ‘Ύ»ίΝΩΤΩ…œΟή±’±Θ¥φΓΘ÷Η≥ω…œ ω≤ΌΉς÷–ΒΡ7¥Π¥μΈσΘΚ
Θ®1Θ©___________ _____________ΘΜ
Θ®2Θ©____________ _____________ΘΜ
Θ®3Θ©_____________ ____________ΘΜ
Θ®4Θ©__________________ _______ΘΜ
Θ®5Θ©______________ ___________ΘΜ
Θ®6Θ©_________ ________________ΘΜ
ΓΓΓΓΘ®7Θ©__________ ________________ΓΘ
ΥΡΓΔΦΤΥψΧβΘ®±ΨΧβΑϋά®2–ΓΧβΘ§Ι≤19Ζ÷Θ©
21Θ°Θ®10Ζ÷Θ©œ÷”–mgΡ≥ΤχΧεΘ§Υϋ”…ΥΪ‘≠Ή”Ζ÷Ή”ΙΙ≥…Θ§ΥϋΒΡΡΠΕϊ÷ ΝΩΈΣMgΓΛmol-1ΓΘ»τΑΔΖϋΦ”Β¬¬ό≥Θ ΐ”ΟNA±μ ΨΘ§‘ρΘΚ
Θ®1Θ©ΗΟΤχΧεΒΡΈο÷ ΒΡΝΩΈΣ___ _____molΓΘ
Θ®2Θ©ΗΟΤχΧεΥυΚ§‘≠Ή”Ήή ΐΈΣ______ _ _ΗωΓΘ
Θ®3Θ©ΗΟΤχΧε‘Ύ±ξΉΦΉ¥Ωωœ¬ΒΡΧεΜΐΈΣ______ ______LΓΘ
Θ®4Θ©ΗΟΤχΧε»ή”Ύ1LΥ°÷–Θ®≤ΜΩΦ¬«Ζ¥”ΠΘ©Θ§Τδ»ή“Κ÷–»ή÷ ΒΡ÷ ΝΩΖ÷ ΐΈΣ______ _ΓΘ
Θ®5Θ©ΗΟΤχΧε»ή”ΎΥ°Κσ–Έ≥…VL»ή“ΚΘ§Τδ»ή“ΚΒΡΈο÷ ΒΡΝΩ≈®Ε»ΈΣ_____ molΓΛL -1ΓΘ
22Θ°Θ®9Ζ÷Θ©‘Ύ±ξΉΦΉ¥Ωωœ¬Θ§ΫΪ224LΒΡHClΤχΧε»ή”Ύ635mLΒΡΥ°÷–Θ®…ηΥ°ΒΡΟήΕ»ΈΣ1.00g/cm3Θ©Θ§«σΥυΒΟ―ΈΥαΒΡ÷ ΝΩΖ÷ ΐΓΘ»τ»Γ≥ω’β÷÷―ΈΥαΘ®ΟήΕ»ΈΣ1.19g/cm3Θ©10.0mLœΓ Ά÷Ν1190mLΘ§‘ρœΓ ΆΚσ―ΈΥαΒΡΈο÷ ΒΡΝΩ≈®Ε»ΈΣΕύ…ΌΘΩ
ΡœΡΣ÷–―ßΗΏ“ΜΡξΦΕΜ·―ß‘¬ΩΦ¥πΨμ
“ΜΓΔ―Γ‘ώΧβΘ®ΟΩ–ΓΧβ2Ζ÷Θ§Ι≤20Ζ÷ΓΘΘ©
1.B 2.D 3.C 4.D 5.C 6.B 7.A 8.B 9.D 10.A
ΕΰΓΔ―Γ‘ώΧβΘ®Ι≤10–ΓΧβΘ§ΟΩ–ΓΧβ4Ζ÷Θ§ΦΤ32Ζ÷ΓΘΘ©
11.BD 12.C 13.B 14.A 15.C 16.A 17.B 18.D
»ΐΓΔ Β―ιΧβΘ®±ΨΧβΑϋά®2–ΓΧβΘ§Ι≤29Ζ÷Θ©
19Θ°Δ≈ΔίΘΜ ΔόΔΏ ΔΤ ΔΎΔέΔήΔίΔόΘΜ Δ« ΔΌΔίΔό ΘΜ ΔήΔί
Θ®ΟΩΩ’3Ζ÷Θ©
20Θ°Θ®1Θ©NaOH”ΠΖ≈‘ΎΗ…‘οΒΡ…’±≠÷–≥ΤΝΩ
Θ®2Θ©”ΟΙΐΒΡ”Έ¬κΈ¥≤ΠΜΊ‘≠¥Π
Θ®3Θ©Ά–≈ΧΧλΤΫ÷ΜΡή≥Τ≥ω0.1ΓΪ0.2gΘ§≥Τ≤Μ≥ω1.00g
Θ®4Θ©…’±≠ΚΆ≤ΘΝßΑτΈ¥œ¥Β”Θ§œ¥Β”“Κ“ύ”ΠΉΣ»κ»ίΝΩΤΩ
ΓΓ Θ®5Θ©»ήΫβNaOH”Πά以Κσ‘ΌΉΣ“Τ÷Ν»ίΝΩΤΩ÷–
ΓΓ Θ®6Θ©»ίΝΩΤΩ÷–ΒΡ»ή“ΚΈ¥“Γ‘»
Θ®7Θ©≈δΚΟΒΡ»ή“Κ”ΠΦΑ ±ΉΣ“ΤΒΫ”–ΫΚ»ϊΒΡ ‘ΦΝΤΩΡΎ
Θ®ΟΩΩ’2Ζ÷Θ©
ΥΡΓΔΦΤΥψΧβΘ®±ΨΧβΑϋά®2–ΓΧβΘ§Ι≤19Ζ÷Θ©
21Θ°Θ®1Θ©m/M Θ®2Θ©2mNA/M Θ®3Θ©22.4m/MΘ®4Θ©m/(m 1000)
Θ®5Θ©m/MV Θ®ΟΩΩ’2Ζ÷Θ©
22. 36.5% Θ® 4Ζ÷Θ© 0.10mol/L Θ®5Ζ÷Θ©
|