高一化学上册期中试卷
总分100分 考试时间100分钟
质子量:H—1 C—12 N—14 O—16 Na—23 Mg—24 Al—27
S—32 Cl—35.5 K—39 Ca—40
一、单选题(本题包括20小题,共40分。)
1. 钠加热后能在空气中着火燃烧的现象是( )
A. 黄色火焰,生成白色固体Na2O
B. 黄色火焰,生成淡黄色固体Na2O2
C. 紫色火焰,生成淡黄色固体Na2O2
D. 红色火焰,生成黄色固体Na2O
2. 氧化还原反应的实质是( )
A. 氧元素的得失 B. 氢元素的得失
C. 电子的得失或偏移 D. 元素化合价的升降
3. Na2O和Na2O2在下列哪一点性质上是相似的( )
A. 颜色 B. 氧化性 C. 水溶液呈碱性 D. 漂白作用
4. 与水反应最剧烈的碱金属是( )
A. 锂 B. 钠 C. 钾 D. 铷
5. 下列物质与水反应后溶液为碱性并有气体逸出的是( )
A. Cl2 B. Na2O C. Na2O2 D. Na2CO3
6. 下列物质:①NaCl ②HNO3 ③CO2 ④KOH ⑤AgNO3 ⑥H2O ⑦CH4 ⑧H2CO3 ⑨蔗糖 ⑩酒精 其中属于弱电解质的是( )
A. ②③⑥ B. ③⑤⑧ C. ③⑥⑧ D. ⑥⑧
7. 金属钠在空气中长期放置,最终生成的物质是( )
A. NaOH B. Na2O C. NaCl D. Na2CO3
8. 下列钠、钾的对比中,叙述不正确的是( )
A. 失电子能力:K>Na
B. 还原性:K>Na
C. 质量相等的Na和K与水反应,产生的氢气一样多
D. 钾跟水反应比钠更剧烈
9. 下列有关金属钠的说法,正确的是( )
A. 钠是活泼金属,将钠投入FeSO4溶液中,可将铁置换出来
B. 钠在化学反应中,失电子,表现氧化性
C. 钠是一种比水轻的金属
D. 钠着火时,应用泡沫灭火器灭火
10. 下列各组离子在酸性溶液里能大量共存,并且溶液是无色的是( )
A. ![]()
B. ![]()
C. ![]()
D. ![]()
11. 金属钠分别与下列溶液反应时,即有沉淀产生又有气体生成的是( )
A. BaCl2 B. K2SO4 C. FeCl3 D. NH4NO3
12. 钠不能用于( )
A. 高压钠灯 B. 原子反应堆导热剂
C. 制普通电线 D. 提炼某些稀有金属
13. 根据以下几个反应:
① ![]()
② ![]()
③ ![]()
④ ![]() 判断氧化性
判断氧化性
由强到弱的顺序是( )
A. ![]()
B. ![]()
C. ![]()
D. ![]()
14. 下列反应需加入氧化剂才能发生的是( )
A. ![]() B.
B. ![]()
C. ![]() D.
D. ![]()
15. 下列物质间发生反应的离子方程式正确的是( )
A. NaOH和NaHCO3溶液混合: ![]()
B. Na2O2投入水中: ![]()
C. Ba(OH)2和硫酸溶液: ![]()
D. 氧化铜与硫酸混合: ![]()
二、多选题(每小题有1—2个选项符合题意,共10分。)
16. 以下反应中,属于氧化还原反应的是( )
A. ![]()
B. ![]()
C. ![]()
D. ![]()
17. 下列各组微粒中,在一定条件下均可以做氧化剂的是( )
A. ![]() B.
B. ![]()
C. ![]() D.
D. ![]()
18. 下列各反应,能用同一离子方程式表示的是( )
A. 氢氧化铜与盐酸 氢氧化铜与醋酸
B. 氯化钡溶液与硫酸铜溶液 氢氧化钡溶液与硫酸铜溶液
C. 碳酸氢钠溶液与稀硫酸 碳酸钠溶液与稀硫酸
D. 石灰石与稀硝酸 石灰石与稀盐酸
19. 有关钠原子和钠离子的叙述正确的是( )
A. 钠原子与钠离子的化学性质相似
B. 钠原子比钠离子多一个质子
C. 钠原子具有还原性,钠离子具有氧化性
D. 钠原子不稳定,而钠离子稳定
20. 氢化钠(NaH)是一种白色的离子晶体,其中钠是 1价。NaH与水反应放出氢气。下列叙述,正确的是( )
A. NaH在水中显酸性
B. NaH中氢离子的电子层排布与氦原子的相同
C. NaH中氢离子具有还原性
D. NaH中氢离子可被还原成氢气
三、填空题(本题包括4题,共30分)
1. 碱金属包括__________、__________、__________、__________、__________(写元素符号)等,它们原子核外的最外电子层上均有__________个电子。在化学反应中,碱金属的原子都__________电子,具有__________性。它们之所以被称为碱金属是因为它的氧化物的水化物是可溶于水的__________。
2. 取一小块钠,刚切开时,断面呈__________色,在空气中放置片刻,断面变__________,这是因为主要生成了__________。
另取一小块钠,将其投入滴有酚酞的一烧杯水中,观察到的现象及结论为:(填写下表)
现象(至少四个)
结论
其反应的离子方程式为(标出电子转移的方向与数目):
3. 可用于鉴别NaCl和KCl的方法是____________________,现象是______________________________。
可用于鉴别Na2CO3和NaHCO3的方法是__________,现象是____________________。
除去Na2CO3固体中少量的NaHCO3固体的方法是__________,方程式为__________
____________________________________________________________。
4. 4.6g钠在空气中充分燃烧,得到淡黄色粉末,将该粉末与足量水反应,生成气体的质量为__________。
四、简答题(共10分)
写出下列反应方程式:是离子反应的写出离子反应方程式;是氧化还原反应的标出电子转移的方向与数目,并指出氧化剂、被氧化元素,氧化产物
1. 小苏打溶液中加入盐酸
2. 过量CO2通入碳酸钠溶液
3. 硫酸铜溶液与氢氧化钡溶液混合
4. 过氧化钠和水反应
5. 将金属钠投入硫酸铜溶液中
五、实验题(本题共6分。)
1. 按以下装置图进行实验,填写有关现象及化学方程式
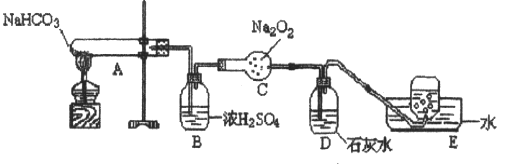
①A中现象是____________________
②B中浓硫酸的作用是____________________
③C中发生反应的化学方程式为____________________
④D中现象是____________________,反应的化学方程式是____________________
⑤E中收集的气体是____________________
六、计算题(本题包括2小题,共10分。)
1. 将7.8克过氧化钠投入100克水中,求所得溶液的质量分数
2. 将一定量的NaHCO3和Cu的混合粉末在空气中加热到质量不再变化时,发现加热前后固体的质量相等,求原混合物中NaHCO3的质量分数(提示:Cu在空气中加热可生成CuO固体)
【试题答案】
一、单选题
1. B 2. C 3. C 4. D 5. C 6. D 7. D 8. C 9. C 10. C
11. C 12. C 13.B 14. A 15. A
二、多选题
16. AD 17. BD 18. D 19. CD 20. BC
三、填空题
1. Li Na K Rb Cs 1 失 还原 强碱
2. 银白 暗 Na2O
现象(至少四个)
结论
1. 金属钠浮在水面上。
2. 熔成小球。
3. 小球四处游动,发出嘶嘶声。
4. 溶液变成红色
5. Na消失
1. ![]()
2. Na的熔点低,反应放热
3. 生成H2
4. 生成NaOH
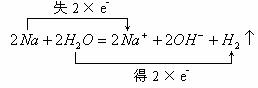
3. 焰色反应 火焰里黄色为NaCl 紫色为KCl
用加热固体或加CaCl2溶液,放出CO2的是NaHCO3,无现象的是Na2CO3或 出白色沉淀的是Na2CO3,无现象的是NaHCO3
加热 ![]()
或 ![]()
4. 1.6g 提示:
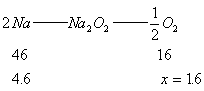
四、简答题
1. ![]()
![]()
2. ![]()
![]()
3. ![]()
![]()
4.
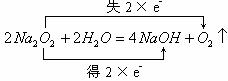
氧化剂Na2O2 还原剂Na2O2 被氧化的元素是O 氧化产物是O2
![]()
5.
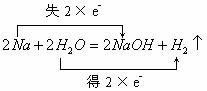
氧化剂H2O 被氧化的元素Na 氧化产物NaOH
![]()
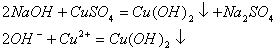
五、实验题
1.①试管内壁有无色液滴 ②干燥气体、(吸收H2O)
③ ![]()
④石灰水变浑浊 ![]()
⑤O2
六、计算题
1. 解:设生成NaOH的质量为x
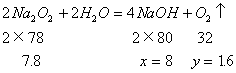
![]()
答:所得溶液的质量分数为7.5%。
2. 解:设NaHCO3的质量为x,Cu的质量为y
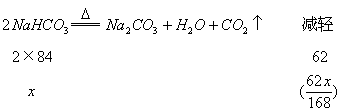

![]()
![]()
或用质量守恒关系,反应物总质量=生成物(剩余,固体)总质量
![]()
答:原混合物中NaHCO3的质量分数是40.4%。
