一、选择题(每小题只有一个选项符合题意。每小题3分,共30分。)
1.20世纪90年代初,国际上提出了“预防污染”这一新概念。绿色化学是“预防污染”的根本手段。下列各项中不属于绿色化学的是( )。
(A)处理废弃物 (B)治理污染点
(C)减少有毒物 (D)杜绝污染源
2.下列说法中正确的是( )。
(A)难失电子的原子,获得电子的能力一定强
(B)易得电子的原子所形成的简单阴离子,其还原性一定强
(C)分子中键能越大,键长越长、则分子越稳定
(D)电子层结构相同的不同离子,核电荷数越多,半径越小
3.物质的量浓度相同的下列等体积溶液中,吸收 ![]() 气体的量最多的是( )。
气体的量最多的是( )。
(A) ![]() (B)
(B) ![]() (C)
(C) ![]() (D)
(D) ![]()
4.将盛有某种金属卤化物和浓硫酸的烧瓶加热后,可制取无色卤化氢气体,则该金属卤化物是( )。
(A)氟化物 (B)氯化物 (C)溴化物 (D)碘化物
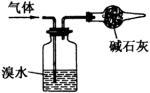
5.下列四种气体(括号内是混有的少量杂质),可用下图所示仪器装置进行净化和干燥的气体是( )。
(A) ![]() (
( ![]() ) (B)
) (B) ![]() (
( ![]() )
)
(C) ![]() (
( ![]() ) (D)
) (D) ![]() (
( ![]() )
)
6.造纸工业常用 ![]() 漂白纸浆。漂白后的纸浆要用
漂白纸浆。漂白后的纸浆要用 ![]() 除去残留的
除去残留的 ![]() ,其反应为:
,其反应为:
![]() ,在这个反应中,氧化产物与还原产物的物质的量之比是( )。
,在这个反应中,氧化产物与还原产物的物质的量之比是( )。
(A)1:1 (B)2:1 (C)1:2 (D)2:3
7.下列材料中,最不宜用于制造储存浓硫酸容器的是( )。
(A)铁 (B)铝 (C)铜 (D)陶瓷
8.下列各组物质在一定条件下能发生反应的是( )。
① ![]() ②
② ![]() ③
③ ![]()
④ ![]() ⑤
⑤ ![]() ⑥
⑥ ![]()
(A)②③④⑤⑥ (B)只有③④⑤
(C)只有④⑤⑥ (D)只有①②③
9.下列各组稀溶液不用其他试剂和试纸,就可以将它们区别开的是( )。
(A)硝酸钾 硫酸铜 硫酸氢钠 氯化钡
(B)硫酸 硫酸铝 氯化钠 硝酸钠
(C)盐酸 硫酸钠 硝酸钠 氢氧化钠
(D)硫酸镁 碳酸钠 氢氧化钠 氯化钾
10.质量分数不同的2种硫酸溶液,以相同质量混合时,所得混合溶液密度为 ![]() ;以相同体积混合时,所得混合溶液密度为
;以相同体积混合时,所得混合溶液密度为 ![]() 。2种浓度不同的乙醇溶液,以相同质量混合时,所得混合溶液密度为
。2种浓度不同的乙醇溶液,以相同质量混合时,所得混合溶液密度为 ![]() ;以相同体积混合时,所得混合溶液密度为
;以相同体积混合时,所得混合溶液密度为 ![]() 。则
。则 ![]() 之间大小关系正确的是( )。
之间大小关系正确的是( )。
(A) ![]() (B)
(B) ![]()
(C) ![]() (D)
(D) ![]()
二、选择题(每小题有一个或两个选项符合题意。每小题4分,共20分。)
11.下列各组离子在pH=1的溶液中,因发生氧化还原反应而不能大量共存的是( )。
(A) ![]() (B)
(B) ![]()
(C) ![]() (D)
(D) ![]()
12.硫代硫酸钠可作为脱氯剂,已知25.0mL 0.100mol/L ![]() 溶液恰好把标准状况下的224mL
溶液恰好把标准状况下的224mL ![]() 完全转化为
完全转化为 ![]() 离子,则
离子,则 ![]() 将转化成( )。
将转化成( )。
(A) ![]() (B)
(B) ![]() (C)
(C) ![]() (D)
(D) ![]()
13.对于复分解反应:X+Y=Z+W,下列叙述中正确的是( )。
(A)若Z是强酸,则X和Y必有一种是酸
(B)若Y是强碱,X是盐,则Z或W必有一种是弱碱
(C)若X是强酸,Y是盐,反应后可能有强酸或弱酸生成
(D)若W是弱碱,Z是盐,则X和Y必有一种是强碱
14.下列反应的离子方程式中,错误的是( )。
(A)将 ![]() 通入
通入 ![]() 溶液:
溶液:
![]()
(B)用氨水吸收少量的二氧化硫气体:
![]()
(C) ![]() 通入
通入 ![]() 溶液中:
溶液中:
![]()
(D)硫酸氢钠溶液与氢氧化钡溶液以等物质的量混合:
![]()
15.已知:A、B、C、D、E是核电荷数依次增大的五种短周期元素;原子半径按D、E、B、C、A的顺序依次减小;B和E同主族。下列推断中不正确的是( )。
(A)A、B、E一定在不同周期
(B)C的最高价氧化物对应的水化物可能显碱性
(C)A、D可能位于同一主族
(D)C和D的单质可能化合形成离子化合物
第Ⅱ卷(非选择题,共50分。)
三、(本题包括2小题,共12分。)
16.(4分)回答下列问题:
(1)在进行沉淀反应的实验中,如何认定沉淀已经完全?
(2)中学化学实验中,在过滤器上洗涤沉淀的操作是 。
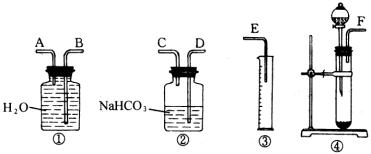
17.(8分)有一小块 ![]() 合金质量为m g,请从下图中选用适当的实验装置,设计一个简单合理的实验,测定合金中Al的质量分数。可供选用的试剂还有:浓
合金质量为m g,请从下图中选用适当的实验装置,设计一个简单合理的实验,测定合金中Al的质量分数。可供选用的试剂还有:浓 ![]() 、浓
、浓 ![]() 、6mol/L的
、6mol/L的 ![]() 、6mol/L的
、6mol/L的 ![]() 、6mol/L的
、6mol/L的 ![]() 溶液。
溶液。
请填写下列空白:
(1)写出实验中合金参与反应的化学方程式: 。
(2)若气体流向从左到右,则所选装置的玻璃管接口顺序为 (填字母代号)。
(3)简述选用或不选用装置②的理由: 。
(4)按上述(2)的方式连接仪器,还可进行下列哪些定量测定: 。
A.用一定质量的纯锌粒测定Zn的相对原子质量
B.用 ![]() 与盐酸反应,测定盐酸的浓度
与盐酸反应,测定盐酸的浓度
C.测定 ![]() 和
和 ![]() 混合物中
混合物中 ![]() 的质量分数
的质量分数
D.用加热分解的方法测定 ![]() 的纯度
的纯度
四、(本题包括4小题,共25分。)
18.(5分)在氮化硅中添加氧化铝,用氧原子替代一部分氮,用铝原子替代一部分硅,通过常压烧结即成新一代无机非金属材料,叫氧氮硅铝,即赛伦(Sialon),化学通式为 ![]() (
( ![]() 为2~4)。试回答:
为2~4)。试回答:
(1)赛伦有 等特性(至少写3种)。
(2)化学通式里的y值为 (用含 ![]() 的表达式或某一具体数值表示)。
的表达式或某一具体数值表示)。
19.(7分)(1)分别写出由氧在一定条件下生成下列物质的化学方程式(必须注明反应条件)。
① ![]() : 。②
: 。② ![]() : 。③
: 。③ ![]() : 。
: 。
(2)指出氧在下列各物质中的化合价: ![]() ;
; ![]() ;
; ![]() 。
。
(3) ![]() 能吸收
能吸收 ![]() 生成
生成 ![]() 和
和 ![]() ,故可用作特殊情况下的氧气源,试写出该反应的化学方程式: 。
,故可用作特殊情况下的氧气源,试写出该反应的化学方程式: 。
(4)人体内 ![]() 离子对健康有害,使人过早衰老,但在催化剂SOD存在下可发生如下反应,请完成该反应的离子方程式:
离子对健康有害,使人过早衰老,但在催化剂SOD存在下可发生如下反应,请完成该反应的离子方程式:
![]()
20.(7分)A、B、C、D、E、F为原子序数依次增大的同周期主族元素。已知:A、C、F三原子的最外层共有10个电子,且这三种元素的最高价氧化物对应的水化物之间两两皆能反应,均能生成盐和水;D元素原子的最外层电子数比次外层电子数少4;E元素原子次外层电子数比最外层电子数多3。
(1)写出下列元素的符号:B ,D ,E 。
(2)五种元素中,原子半径最大的是 ,常温下能与水剧烈反应的单质的元素是 ,气态氢化物最稳定的是 (用A、B、C、D、E、F回答)。
(3)A、C两种元素最高价氧化物对应的水化物反应的离子方程式是 。
21.(6分)向100mL 3mol/L硫酸铝铵[ ![]() ]溶液中逐滴加入1mol/L
]溶液中逐滴加入1mol/L ![]() 溶液。
溶液。
(1)写出当刚好出现沉淀的总物质的量为最大值时的离子方程式(用一个式子表示): 。
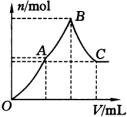
(2)随着 ![]() 溶液体积V的变化,沉淀总物质的量n的变化如下图所示。写出B点和C点所对应的
溶液体积V的变化,沉淀总物质的量n的变化如下图所示。写出B点和C点所对应的 ![]() 溶液的体积:B ,C 。
溶液的体积:B ,C 。
五、(本题包括2小题,共13分。)
22.(6分)第ⅠV主族元素R,在它的化合物 ![]() 中,其质量分数为0.778,在它的另一种化合物
中,其质量分数为0.778,在它的另一种化合物 ![]() 中,其质量分数为0.636。
中,其质量分数为0.636。
(1)试求n和m的值: ![]() ,
, ![]() 。
。
(2)试求R的相对原子质量: ![]() 。
。
23.(7分)用20mL 18.4mol/L浓 ![]() 和铜共热一段时间后,使反应混合物冷却,滤去多余的铜,将滤液加水定容到100mL,测得
和铜共热一段时间后,使反应混合物冷却,滤去多余的铜,将滤液加水定容到100mL,测得 ![]() 离子浓度为3.18mol/L。试求溶液中
离子浓度为3.18mol/L。试求溶液中 ![]() 的物质的量浓度。
的物质的量浓度。
答案:
1.C 2.D 3.C 4.B 5.B 6.C 7.C 8.A 9.A 10.B
11.BC 12.D 13.C 14.AD 15.B
16.(1)在上层清液中(或取少量上层清液置于小试管中),滴加沉淀剂,如果不再产生沉淀,说明沉淀完全。(2)向漏斗里注入蒸馏水,使水面没过沉淀物,等水流完后,重复操作数次。
17.(1) ![]() 。 (2)F→A→B→E。
。 (2)F→A→B→E。
(3)不选用;排水法水可以把 ![]() 溶解掉,若选用②,生成的
溶解掉,若选用②,生成的 ![]() 反而使测得的
反而使测得的 ![]() 的体积增大。
的体积增大。
(4)A、C。
18.(1)耐高温、高强度、超硬度、耐磨损、抗腐蚀、热稳定性好。
(2) ![]() 。
。
19.(1)① ![]()
![]()
![]() ②
② ![]()
![]()
![]()
③ ![]()
![]()
![]()
(2)0;-1;-2。
(3) ![]() 。
。
(4)2、2、1、1、2 ![]() 。
。
20.(1)Mg;Si;P。 (2)A;A;F。
(3) ![]() 。
。
21.(1) ![]()
(2)600mL;750mL。
22.(1)2;4。 (2)119。
23.0.5mol/L
