|
乐清市第三中学2006-2007学年第一次月考试卷
高一化学
可能需要的原子量: H-1 C-12 N-14 O-16 Ne-20 S-32 Cl-35.5 Na-23 Mg-24 Al-27 Fe-56 Ba-137 总分100分
一、选择题(每小题只有一个选项符合题意,每小题2分,共32分)
1.下列物质属于电解质的是( )
A 铁 B 氯化氢 C 蔗糖 D Na2SO4溶液
2.等质量的N2和CO中,有可能不同的是( )
A 物质的量 B 体积 C 分子数 D 原子数
3.下列反应属于氧化还原反应的是( )
A CaCO3+2HCl====CaCl2+H2O+CO2↑
B 2NaHCO3 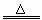 Na2CO3+H2O+CO2↑ Na2CO3+H2O+CO2↑
C Cl2+2NaOH===NaCl+NaClO+H2O
D NaBr+AgNO3===AgBr↓+NaNO3
4.容量瓶上标有的是①温度 ②浓度 ③容量 ④质量 ⑤刻度线 ⑥酸式或碱式( )
A ①③⑤ B ③⑤⑥ C ①⑤⑥ D ②③⑤
5.做焰色反应实验用的铂丝,每试验一种样品后都必须( )
A 用水洗涤2~3次后再使用
B 用盐酸洗涤后,经蒸馏水冲洗,方可使用
C 用滤纸擦干后才可使用
D 用盐酸洗涤后,再在酒精灯火焰上灼烧到没有颜色,才可使用
6.下列实验操作中错误的是( )
A 分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出
B 加热烧杯时垫石棉网
C 在烧杯中溶解一定量的某物质,然后移入量筒中配制一定物质的量浓度的溶液
D 称量时,称量物放在称量纸上,置于托盘天平的左盘,砝码放在托盘天平的右盘中
7.能区分胶体和溶液的方法是( )
A 静置,有沉淀现象的是胶体 B 有丁达尔现象的是胶体
C 能透过滤纸的是溶液 D 用肉眼观察,均匀透明的是溶液
8.下列说法正确的是 ( )
A 在常温常压下,11.2 L N2含有的分子数为0.5 NA
B 在常温常压下,1 mol Ne含有的原子数为NA
C 71 g Cl2所含原子数为NA
D 在同温同压时,相同体积的任何气体单质所含的原子数相同
9.下列溶液中Cl-物质的量浓度最大的是( )
A 100mL2mol/LMgCl2 B 1000mLl.5mol/LNaCl
C 250mLl mol/LAlCl3 D 300mL5mol/LKClO3
10.下列物质中,所指定的微粒数目最多的是( )
A 35.5g氯气所含的原子数 B 标准状况下1.8LH2O所含的氧原子数
C 标准状况下11.2LCO所含的分子数 D 200mL 2mol/LAlCl3溶液所含Cl-数目
11.下列说法中错误的是( )
A 物质的聚集状态不同主要是构成物质的基本粒子间的距离不同
B 不同分散系其对应分散质的微粒直径不同
C 1mol O2与1mol O3所含的分子数目相等
D 1mol氢气所占体积约为22.4L
12.为了检验某固体物质中是否含有NH4+,你认为下列试纸和和试剂一定用不到的是( )
①蒸馏水 ②NaOH溶液 ③红色石蕊试纸 ④蓝色石蕊试纸 ⑤稀硫酸
A ①⑤ B ④⑤ C ①③ D ①④⑤
13.除去食盐溶液中的Ca2+、Mg2+、SO42-等杂质,需加入NaOH、Na2CO3、BaCl2和盐酸,加入顺序正确的是( )
A NaOH Na2CO3 BaCl2 HCl B Na2CO3 BaCl2 HCl NaOH
C BaCl2 HCl NaOH Na2CO3 D NaOH BaCl2 Na2CO3 HCl
14.已知每个氧原子中含有8个电子,mg的氧气中含有1 mole-,则m的数值为( )
A 2 g B 4 g C 16 g D 32 g
15.2.16g X2O5中含有0.1mol 氧原子,则X的相对原子质量为( )
A 21.6 B 28 C 14 D 31
16.某同学想用实验证明硫酸铜溶液显蓝色与SO42-无关,进行下列实验无意义的是( )
A 观察硫酸钠溶液没有颜色
B 向硫酸铜溶液中滴加适量的氯化钡溶液,振荡后静置,溶液蓝色未消失
C 向硫酸铜溶液中滴加适量的氢氧化钠溶液,振荡后静置,溶液蓝色消失
D 加水稀释硫酸铜溶液,溶液蓝色变浅
二、选择题(每小题只有一个选项符合题意,每小题3分,共15分)
17.向等浓度的NaCl、MgCl2、AlCl3溶液中分别加入0.1mol/L的AgNO3溶液105ml,刚好都能使Cl―沉淀完全,则消耗这三种溶液的体积比为( )
A 3 :2 :1 B 1 :2 :3 C 2 :3 :6 D 6 :3 :2
18.在标准状况下,16g气体A和1g气体B的分子数相同,下列说法中,不正确的是( )
A 气体A和B的式量比为16:1
B 同质量气体A和B的分子个数比为1:16
C 同温同压下,A气体与B气体的密度比为1:16
D 相同状态下,同体积A气体和B气体的质量比为16:1
19.两个容积相同的容器,一个盛有一氧化氮(NO),另一个盛有氮气和氧气,在同温、同压下两容器内的气体不一定相同的是( )
A 原子总数 B 气体物质的量 C 分子总数 D 质量
20.在40g密度为dg/cm3的硫酸铁溶液中,含有1.4gFe3 离子,则此溶液中Fe3 的物质的量浓度为( )
A 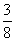 d B d B 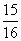 d C d C 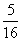 d D d D  d d
21.在NaOH溶液中,Na+和的H2O个数比为1 :20时,此溶液的质量分数为( )
A 5% B 10% C 11.1% D 20%
三、填空与实验分析题
22.(14分)(1)人们可根据物质的性质,采取适当的方式将混合物中各物质分离开来:
①不溶性固体与水的混合物,如泥沙与水,可用 方法分离;
②可溶性固体与水的混合物,如水和食盐,可用 方法分离;
③两种可溶性固体,若它们的溶解度随温度变化不同,如氯化钠和硝酸钾,可通过
方法将其分离;
④两种互相溶解但沸点不同的液体,如水与乙醇,可用 方法分离;
⑤两种互不相溶的液体,如汽油与水,可通过 方法分离;
(2)苯、四氯化碳、氯仿都是常用的无色的有机溶剂,下列实验现象分别能得出什么结论?往溴水中滴加氯仿,上层呈橙色,下层接近无色,振荡静置后,下层呈橙色,上层接近无色。结论:① ,
② ,
③ 。
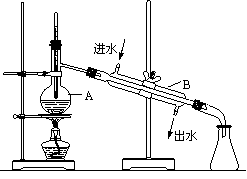
(3)如图为实验室制取蒸馏水的装置示意图,根据图示回答下列问题。
① 图中的两处明显的错误是 、 。
②A仪器的名称是 ,B仪器的名称是 。
③实验时A中除加入自来水外,还需加入少量 ,其作用是
23.(8分)有一固体粉末,其中可能含有Na2CO3、NaCl、Na2SO4、CuCl2、Ba(NO3)2、K2CO3、
K2SO4中的一种或几种,现按下列步骤进行实验。
(1)将该粉末溶于水得无色溶液和白色沉淀。
(2)在滤出的沉淀中加入稀硝酸,有部分沉淀溶解,同时产生无色气体。
(3)取滤液做焰色反应,可证明滤液中含Na ,不含K 。
由上述现象推断:
(1)该混合物中一定含有 ;一定不含有 ,可能含有 。
(2)如要检验其是否存在,将如何操作 。
24.(6分)配制500mL0.1mo1・L-1碳酸钠溶液
(1)应用托盘天平称取碳酸钠晶体(Na2CO3・10H2O) g
(2)配制碳酸钠溶液时需要用到的仪器有
(除托盘天平外,按先后顺序,写出主要四种)
(3)下列操作结果,溶液物质的量的浓度偏低的是
A 没有将洗涤液转移到容量瓶中
B 容量瓶洗净后未经干燥处理
C 转移过程中有少量的溶液溅出
D 摇匀后立即观察,发现溶液未达刻度线,再用滴管加几摘蒸馏水至刻度线
25.(4分)①氢气、②氧气、③氮气各10g,在标准状况下体积由大到小的顺序是(填序号)___________,所含分子数最多的是____________。
26.(2分)配置100mLlmol/LHCl溶液需密度为1.19g/mL、HCl的质量分数为36.5%的浓盐酸的体积是 mL。
27.(6分)在无土栽培中,配制1 L内含0.5 mol NH4Cl、0.16 mol KCl、0.24 mol K2SO4的某营养液,若用KCl、NH4Cl、(NH4)2SO4配制,则需这三种固体的物质的量分别为 、 、 。
四、计算题(13分)
28.(6分)标准状况下,1.6g氢气完全燃烧。
(1)需要的O2体积是多少升?
(2)消耗的O2分子数与多少克甲烷所具有的原子数相等?
29.(7分)HCl和H2SO4混合溶液200mL,分成两等份,往一份中滴加足量BaCl2溶液,产生4.66g白色沉淀,往另一份中投入足量铁片,放出标准状况下1.12 L气体。求该混合溶液中HCl和H2SO4的物质的量浓度。
化学参考答案
一、二 选择题 |
题号 |
1 |
2 |
3 |
4 |
5 |
6 |
7 | |
答案 |
B |
B |
C |
A |
D |
C |
B | |
题号 |
8 |
9 |
10 |
11 |
12 |
13 |
14 | |
答案 |
B |
A |
B |
D |
B |
D |
A | |
题号 |
15 |
16 |
17 |
18 |
19 |
20 |
21 | |
答案 |
C |
D |
D |
C |
D |
D |
B | |