高一化学
可能用到的相对原子质量:H:1 Mg:24 C:12 N:14 O:16 S:32 Cl:35.5 Br:80 Na:23 Al:27 K:39 Fe:56 Cu:64 Ca:40
一、选择题(本题包括20小题,每小题2分,共44分,每小题只有一个选项符合题意)
( )1.下列物质不是电解质的是
A. Na2SO4 B. NaOH C. O2 D.HCl
( )2、下列化学反应基本类型中一定不是氧化还原反就的是
A.化合反应 B.分解反应 C.复分解反应 D.置换反应
( )3、摩尔是
A.物质的质量单位 B.物质的量
C.物质的量的单位 D.就是6.02×1023个微粒
( )4、下列反应都有沉淀生成,其中属于氧化还原反应的是
A. Na2SO4 BaCl2===2NaCl BaSO4↓ B. 4Fe(OH)2 O2 2H2O== 4Fe(OH)3↓
C. FeCl3 3KOH===Fe(OH)3↓ 3KCl D.CuCl2 2NaOH===Cu(OH)2↓ 2NaCl
( )5、下列离子方程式正确的是
A.亚硫酸钠与盐酸反应:Na2SO3 2H ===2Na2 SO2↑ H2O
B.碳酸钙与盐酸反应:CO32- 2H =CO2↑ H2O
C.稀硫酸与锌反应:H2SO4 Zn=Zn2 SO42- H2↑
D. 硫酸溶液与氢氧化钠溶液反应:H OH-===H2O
( )6、实验室中,要使AlCl3溶液中的Al3 离子全部沉淀出来,适宜用的试剂是
A、NaOH溶液 B、Ba(OH)2溶液 C、盐酸 D、氨水
( )7、下列各组物质发生反应后,能生成盐和O2的是
A.Na和H2O B.Na2O和H2O C.Na2O2和H2O D.Na2O2和CO2
( )8、关于Na2CO3和NaHCO3性质的说法正确的是
A.在水中的溶解性:NaHCO3>Na2CO3
B.热稳定性:NaHCO3<Na2CO3
C.与盐酸溶液反应的速率:NaHCO3<Na2CO3
D.Na2CO3不能转化成NaHCO3,而NaHCO3能转化成Na2CO3
( )9、除去Na2CO3 固体中少量的NaHCO3最佳方法是
A.加入适量盐酸 B.加入NaOH溶液
C.加热灼烧 D. 配成溶液后通入CO2
( )10、一块钠暴露在空气中一段时间,发生的反应是
①4Na O2=2Na2O ②2Na O2=Na2O2
③Na2O H2O=2NaOH ④2NaOH CO2=Na2CO3 H2O
A.① B.② C.①③ D.①③④
( )11、16克O2的摩尔质量为
A.32 B.32g/mol C.32g D.32mol
( )12、做蒸馏实验时温度计的水银球应处在什么位置
A、液面下 B、液面上 C、支管口 D、任何位置
( )13、下列各组离子能在溶液中大量共存的是
A.Ba2 、Cu2 、Cl-、SO42- B.Na 、Fe3 、SO42-、OH-
C.H 、Na 、Cl-、CO32- D.K 、OH-、Na 、NO3-
( )14、下列试剂中能用来分别Al3 和Fe3 的是
A.KSCN B.FeCl3 C.H2SO4 D.CuSO4
( )15、下列变化需要加入还原剂才能实现的转化是:
A.浓H2SO4→SO2 B.Fe2 →Fe3 C. H2S→SO2 D. HCOeq \o(\s\up 5(- ),\s\do 2(3 ))- 3 →CO2
( )16、把铁片放入下列溶液中,铁片溶解,溶液质量增重且无气体放出的是
A、CuSO4溶液 B、FeCl3溶液 C、稀硫酸 D、盐酸
( )17、下列叙述正确的是
A、1mol任何气体的体积一定是22.4L
B、同温同压下两种气体,只要它们的分子数相同,所占体积也一定相同
C、在标准状况下,体积为22.4L的物质都是1mol
D、在非标准状况下,1mol任何气体的体积不可能是22.4L
( )18、做焰色反应实验时所用的铂丝,每次用毕后都要
A、用水多洗几次 B、先用稀盐酸洗,再用水洗
C、用稀盐酸洗 ,再在火焰上灼烧到没有什么颜色为止
D、放在火焰上灼烧,直到铂丝发红为止
( )19、在相同条件下,下列气体中所含分子数目最多的是
A、1gH2 B、10gO2 C、30gCl2 D、17gNH3
( )20、关于胶体的叙述,不正确的是:
A.有色玻璃是固溶胶 B.雾、云、烟都是气溶胶
C.利用丁达尔效应能把胶体同溶液区分开 D.布朗运动是胶体特有的性质
( )21、密度为1.84g/cm3、H2SO4的质量分数为98%的浓硫酸中H2SO4的物质的量浓度是
A、18.4mol/L B、18.8mol/L C、18.4mol D、18.8
( )22、吸入人体內的氧有2%转化为氧化性极强的“活性氧”,它能加速人体衰老,被称为“生命杀手”,服用含硒元素(Se)的化合物亚硒酸钠(Na2SeO3),能消除人体內的活性氧,由此推断Na2SeO3的作用是
A 作还原剂 B 作氧化剂
C 既作氧化剂又作还原剂 D 既不作氧化剂又不作还原剂
二、选择题(每小题有1个或2个正确答案,每小题占3分,如果2个选项,只选一个,并且正确的给1分,本大题共21分)
( )23、等质量的SO2和SO3
A、所含氧原子的个数比为2∶3 B、所含硫原子个数比为1∶1
C、所含硫元素的质量比为5∶4 D、所含原子个数比为3∶4
( )24、制印刷电路时常用氯化铁溶液作为“腐蚀液”。铜被氯化铁溶液腐蚀的方程式为B2FeCl3 Cu=2FeCl2 CuCl2;FeCl3 溶液也能与铁反应2FeCl3 Fe=3FeCl2;当向盛有氯化铁溶液的烧杯中同时加入铁粉和铜粉,反应结束后,烧杯底部不可能出现的是
A.有铜无铁 B.有铁无铜 C.有铁有铜 D.无铁无铜
( )25、在强酸性溶液中,下列离子组能大量共存且溶液为无色透明的是C
A.Na 、K 、OH-、Cl- B.Na 、Cu2 、SO42-、NO3-
C.Mg2 、Na 、SO42-、Cl- D.Ba2 、Al3+、Cl-、K
( )26、下列各组物质中,X是主体物质,Y是少量杂质,Z是要除去杂质而加入的试剂,其中正确的组别是
X Y Z
A. FeCl2溶液 FeCl3 KSCN溶液
B. Fe粉 A1粉 NaOH溶液
C. Fe2(SO4)3溶液 FeS04 C12
D. FeCl2溶液 CuCl2 Fe粉
|
沉淀质量 |
|
NaOH溶液体积 |
|
0 |
 ( )27.在某无色溶液中缓慢地滴入NaOH溶液直至过量,产生沉淀的质量与加入的NaOH溶液体积的关系如右图所示,由此确定,原溶液中含有的阳离子是:
( )27.在某无色溶液中缓慢地滴入NaOH溶液直至过量,产生沉淀的质量与加入的NaOH溶液体积的关系如右图所示,由此确定,原溶液中含有的阳离子是:
A.Mg2 、Al3 、Fe2 B.H 、Mg2 、Al3
C.H 、Ba2 、Al3 D.只有Mg2 、Al3
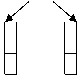 ( )28.如图所示的实验中,投入铝片后 铝
( )28.如图所示的实验中,投入铝片后 铝
A ①中产生气泡,②中不产生气泡 片
B ①和②中都不产生气泡 稀HCl NaOH溶液
C ①和②中都产生气泡,①中是H2,②中是O2
D ①和②中都产生气泡,且都是H2 ① ②
( )29、在硫酸钠和硫酸铝的混和溶液中,Al3 的物质的量浓度为0.2mol/L,SO42-为0.4mol/L,溶液中Na 的物质的量浓度为
A.0.1mol/L B.0.2mol/L C.0.3mol/L D.0.4mol/L
|
密封线内不准答题 |
|
班级: 姓名: 学号: |

 均安中学2006学年度第一学期第17周月考考试试卷
均安中学2006学年度第一学期第17周月考考试试卷
高一化学
三、填空
30、(2分)用Na2CO3固体配制1mol/L的Na2CO3溶液100mL。
(1)供选用的仪器有:①玻璃棒;②胶头滴管;③100mL量筒;④100mL容量瓶;⑤250mL量筒;⑥天平;⑦50mL烧杯;应选用的仪器(填编号) 。
(2)应称取Na2CO3的质量为 。
31、(4分)写出下列反应的化学反应方程式:
(1)钠与硫酸铜溶液反应:________________________________________
(2)氢氧化亚铁空气中被氧化
(3)铝与氢氧化钾溶液
(4)过氧化钠与水反应_____________________________________________
32.(4分)有X、Y、Z三种单质,X为金属单质,Y、Z为非金属单质,Y、Z通常情况下为气态,Y、Z一定条件下反应的产物溶于水可得无色溶液E,E能使紫色石蕊试液变红,X与E反应可生成Z和另一产物w,X、Y反应的产物F溶于水为棕黄色溶液,将Y通入w溶液也可得到F的溶液。
(1)Z的化学式是 。
A、O2 B、H2 C、Cl2 D、N2
(2)w的名称是 。
A、氯化铁 B、盐酸 C、氯化亚铁 D、铁
(3)棕黄色溶液F是 。
A、氯化铁溶液 B、氯化亚铁溶液 C、盐酸 D、氯水
(4)若往w溶液中滴入NaOH溶液,可产生沉淀,此沉淀在空气中发生变化,现象是 _______ 。
A、红色→灰绿色→红褐色 B红褐色→白色→灰绿色
C、红色→红褐色→灰绿色 D、白色→灰绿色→红褐色
33.(3分)有一包固体粉末,可能含有下列阳离子或阴离子中的若干种:K 、NH4 、Fe3 、Cu2 、Mg2 、Cl-、SO42-。现做以下实验:
(1)取少量固体,加适量蒸馏水,搅拌后固体全部溶解,得到无色透明溶液;
(2)在混合溶液中加入浓NaOH溶液并加热无现象;
(3)向混合溶液中滴入Ba(NO3)2溶液,无沉淀产生。再滴入AgNO3溶液生成白色沉淀;
(4)用铂丝蘸取少量粉末放在火焰上灼烧,透过蓝色钴玻璃观察时,火焰呈紫色。
试根据以上实验现象判断:
这包白色粉末一定含有的离子是 ;一定不含有的离子是 ;
并写出参加反应的离子方程式是:
34、(3分)用双线桥法表示下列氧化还原反应电子转移情况,并指出氧化剂。
MnO2 4HCl(浓) = MnCl2 2H2O Cl2↑ 氧化剂 。
35、(2分)为了除去下表中各物质所含的杂质(括号内的物质),请完成下面表格
|
物 质 |
除杂试剂 |
分离方法 |
有关的离子方程式为 |
|
CuO(Al2O3) |
|||
|
Na2CO3(NaHCO3) |
――――― |
36.(5分)回答问题:
(1)(3分)甲、乙两试管分别盛有5 mLFeCl3溶液和5 mLFeCl2溶液,各滴入几滴KSCN溶液。填写下表:
|
试 样 |
滴入KSCN溶液后的现象 |
两试管里产生不同的现象有何用途 |
|
甲试管(FeCl3) |
||
|
乙试管(FeCl2) |
(2)(2分)在盛有3 mLFeCl3溶液的试管中加入少量铁粉,若充分反应后没有固体物剩余。该试管的溶液中存在什么金属阳离子?如何进一步得到肯定答案?
_____________________________________________________________________
_____________________________________________________________________
_____________________________________________________________________
四、计算题(12分)
37、(2分)2.7 g Al 物质的量为_________ 。与足的盐酸反应生成H2的体积为____________ (在标准状况下)。
38. (6分)某种待测浓度的H2SO4溶液20mL,加入10mL0.5mol/LBaCl2溶液,恰好完全反应。问(1)得到BaSO4沉淀多少克?(2)待测H2SO4溶液的物质的量浓度是多少?
39.(4分)将Na2CO3、NaHCO3的混合物1.9g,强热至无气体出现为止,恢复至原来状态,称量剩余物的质量减轻了0.31g,求原混合物中NaHCO3质量分数。
均安中学2006-007学年度第一学期第17周月考考试试卷
高一化学 参考答案
选择题答案
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
11 |
12 |
13 |
14 |
15 |
|
C |
C |
C |
B |
D |
D |
D |
B |
C |
D |
B |
C |
D |
A |
A |
|
16 |
17 |
18 |
19 |
20 |
21 |
22 |
23 |
24 |
25 |
26 |
27 |
28 |
29 |
- |
|
B |
B |
C |
D |
D |
A |
A |
C |
B |
CD |
BD |
B |
D |
B |
- |
30、2分,(1)①②④⑥⑦ 1分 (2)10.6 g 1分
31、4分,略32、4分(1) B 。(2) C 。(3) A (4) D
33、3分 K 、Cl- ; NH4 、Fe3 、Cu2 、Mg2 、SO42- ;
参加反应的离子方程式是: Ag Cl-=AgCl↓
34、3分,略 35、2分,略
36、5分,
|
试 样 |
滴入KSCN溶液后的现象 |
两试管里产生不同的现象有何用途 |
|
甲试管(FeCl3) |
溶液变成红色; |
常用KSCN溶液检验Fe3 的存在 |
|
乙试管(FeCl2) |
溶液没有变色 |
(2)答:若铁粉不足,反应后溶液里存在的金属离子可能是Fe2 和Fe3 ,若铁粉恰好与Fe3 完全反应,则反应后溶液中的金属离子是Fe2 。(1分)
取少量反应后的溶液于另一试管中,滴入几滴KSCN溶液,观察溶液是否变红,若变红说明是Fe2 和Fe3 ,若不变色,则说明是Fe2 。(1分)
37、2分,0.1mol 3.36L
38、6分,1.165g 0.25mol/L
39、4分,44.2%
