| 中文域名: 古今中外.com
英文域名:www.1-123.com 丰富实用的教育教学资料 |
| |
| |
| |
|
|
A.焚烧垃圾 B.使用含磷洗衣粉 C.汽车排放的尾气 D.用煤和石油产品作燃料 2.光导纤维传输信息容量大,而且抗干扰、防窃听、不腐蚀,制光导纤维的材料是( )。 A.晶体硅 B.二氧化硅 C.硅酸盐 D.铝硅合金 3.一定量的浓硫酸跟过量的锌充分反应,产生的气体可能有( ) ① SO2 ② SO3 ③ H2S ④ H2 A.①② B.①③ C.①④ D.只有① 4.下列四个反应中水起的作用与其它不相同的是 = 1 \* GB3 ①Cl2 H2O、 = 2 \* GB3 ②NO2 H2O、 = 3 \* GB3 ③Na H2O、 = 4 \* GB3 ④ NH3 H2O、( )。 A. = 1 \* GB3 ① B.② C. = 3 \* GB3 ③ D. = 4 \* GB3 ④ 5.下列物质中,按其成分能与玻璃、水泥、陶瓷归于同一类的是( )。 A.硅石 B.碳化硅 C.硅酸钠 D.二氧化硅 6.生石灰中含有碳酸钙和二氧化硅,要检验这两种杂质是否存在,选用的试剂最好是( )。 A.稀盐酸 B.水 C.烧碱溶液 D.稀硫酸 7.下列反应制取气体合理可行的是( )。
B.CaCO3 H2SO4(稀) 、 CaSO4 H2O CO2↑
8.不能用检验新制氯水和长期放置的氯水的试剂是( )。 A.石蕊试液 B.品红溶液 C.FeCl2溶液 D.AgNO3溶液
对上述两个反应的下列叙述中,错误的是( )。 A.两个反应都是置换反应 B.两个反应中的H2均作为还原剂 C.两个反应都要在耐腐蚀的容器中进行 D.两个反应都是氧化还原反应 10.下列关于浓硝酸和浓硫酸的叙述错误的是( )。 A.都是常用的干燥剂 B.分别露置在空气中,容器内溶质的物质的量浓度都降低 C.都可以储存于铝制槽罐中 D.和铜反应中都表现出强氧化性和强酸性 11.下列的各组离子在酸性溶液中能大量共存的是 A、Na 、Fe2 、、NO3-、SCN― B、Ca2 、K 、Cl―、NO3― C、Al3 、K 、OH―、NO3― D、Na 、Ca2 、SiO32―、Cl― 12.将盛有N2和NO2 的混合气体的试管倒立于水中经过足够时间后,气体体积减少为原来的一半,则原混合气体中N2和NO2 的体积比是( ) A 1:1 B 1:2 C 1:3 D 3:1 13.在下图装置中,烧瓶中充满干燥气体a,将滴管中的液体b挤入烧瓶内,轻轻振荡烧瓶,然后打开弹簧夹f,烧杯中的液体b呈喷泉状喷出,最终几乎充满烧瓶。a和b分别是( )
|
| a(干燥气体)
| b(液体)
| ①
| N02
| 水
| ②
| CO2
| 4 mol・L―1NaOH溶液
| ③
| C12
| 饱和食盐水
| ④
| NH3
| l mol・L―1盐酸 |
|
b |
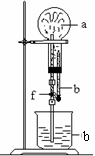
14.能正确表示下列反应的离子方程式是( )
A.将Cl2通入溴化亚铁溶液: 2Fe2 Cl2 = 2Fe3 2Cl-
B. 氯气通入水中: Cl2 H2O = 2H Cl- ClO-
C. AlCl3溶液中通入过量的氨水: Al3 3NH3 • H2O = Al(OH)3↓ 3NH4
D.碳酸氢钠和稀硫酸反应: CO32- 2H =CO2↑ H2O
二、非选择题(44分)
15.(6分)酸雨的形成与大气中二氧化硫及氮氧化物的含量有关。目前中国已是仅次于欧洲和北美的第三大酸雨区。
(1)机动车所排放的废气中主要含CO和氮氧化物。为使机动车达标排放,可在排气简中安装一个催化净化装置,使尾气中的CO和NO转化为参与大气循环的两种无毒气体,写出反应的化学方程式: 。
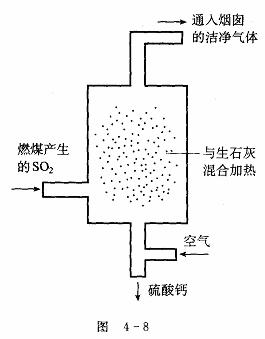
(2)某火力发电厂为除去有害气体SO2,并变废为宝,采用尾气脱硫新工艺,如图4―8所示。写出尾气脱硫工艺中反应的化学方程式:_____________________________________
。
16. (12分)已知A、B、C、D、E、F是含有同一种元素的化合物,其中F是能使红色湿润石蕊试纸变蓝的气体,它们之间能发生如下反应
|
△ |
(1)写出它们的化学式:A 、B 、C 、
D 、E 、F ;
(2)写出各步反应的离子方程式,并指反应①的氧化剂和还原剂
① 、氧化剂 、还原剂
②
③
(3)工业生产C的过程中有如下一步反应,即F经催化氧化生成B和H2O,写出该步反应的化学方程式 。
17.(8分)(1)现有废铜屑和废硫酸,请从原料的利用率和环保的角度分析,设计一个制取胆矾(CuSO4•5H2O)的合理方案,用简要的文字和化学方程式说明。
第一步:
第二步:
第三步:过滤,加热浓缩,冷却结晶
(2)有人建议用铜和稀硫酸混合在加热的条件下不断通入空气以制得硫酸溶液,请写出该反应的化学方程式 。
18.(10分)为了验证Cu和 浓H2SO4反应的产物中有SO2和H2O,选用下图所示仪器(内含物质)组装成实验装置 . B中有无水硫酸铜、C中有品红、D中有氢氧化钠溶液
|
a |
|
b |
|
c |
|
e |
|
g |
|
d |
|
f |
|
A |
|
B |
|
C |
|
D |

(1)如按气流由左向右流向,连接上述装置的正确顺序是(填各接口字母):a接 ,
接 , 接 ;
(2) 仪器B、C应有怎样的实验现象才表明已检验出SO2和H2O?
B中 ,C中 ;
若将 B、C装置前后对调,对实验有何影响
。
(3)D中氢氧化钠溶液的作用是 ;
(4)写出A中反应的化学方程式 .
19.(8分)取17.3g的NH4Cl和(NH4)2SO4固体混合物,加水完全溶解后,加入50mL的BaCl2溶液,恰好反应完得到11.65g的白色沉淀,试计算固体混合物中NH4Cl的物质的量和BaCl2溶液的物质的量浓度。
非金属及其化合物单元检测题参考答案(A)
 1.B 2.B 3.C 4.C 5.C 6.A 7.D 8.D 9.B 10.A 11.B 12.C 13.D 14.C
1.B 2.B 3.C 4.C 5.C 6.A 7.D 8.D 9.B 10.A 11.B 12.C 13.D 14.C
15.
16. (1)A NO2 B NO C HNO3 D NH4NO3 E NaNO3 F NH3
|
|
|
17.(1)第一步:将铜屑灼烧 2Cu O2 ===== 2CuO
第二步:将灼烧后的物质加入到硫酸中 CuO H2SO4 = CuSO4 H2O
第三步:CuSO4 5H2O = CuSO4•5H2O
18. (1) a接 b , c 接 e , d 接 f ;
(2) B中 白色粉末变蓝 ,C中 品红褪色 ;
如果C装置放在B之前,则不能检验出反应是否有水生成。
|
(4)写出A中反应的化学方程式 2H2SO4(浓) Cu ====== CuSO4 SO2↑ 2H2O 。
19.0.2mol,1mol/L
| |