|
第一学期期末考试
高一化学
可能用到的相对原子质量:C. 12 H.1 N. 14 O. 16 Na. 23 Mg. 24 Al. 27 S. 32 Cl. 35.5 Ca. 40
Mn. 55 Ba. 137
一、单项选择题(20小题,40分)
1、下列为强电解质的是( )
A,H2SO4 B,Fe C,CH3COOH D,酒精
2、下列关于钠的单质的说叙述中,正确的为( )
A,化学性质比较活泼,所以自然界中无游离态的钠
B,不能保存在水中是因为钠的密度比水小
C,是一种较硬的金属,导热性好
D,熔沸点较高
3、下列说法中正确的是( )
A,Na在空气中缓慢氧化生成白色的Na2O2 B,Na在空气中燃烧生成Na2O2
C,Na在空气中燃烧生成淡黄色的Na2O D,Na在空气中燃烧生成白色的Na2O2
4、关于摩尔的说法中正确的为( )
A,摩尔是表示物质数量的单位 B,摩尔是表示物质多少的单位
C,摩尔是表示物质的量的单位 D,摩尔是表示物质的质量的单位
5、Cl2的摩尔质量是( )
A,71mol B,71g C,71g・mol D,71mol・L-1
6、下列说法正确的是( )
A,液氯和氯水是同一物质
B,HCl是一种无色无味,极易溶于水的气体
C,区别Na2SO4.AgNO3两溶液客人用BaCl2溶液
D,区别NaCl. NaBr. NaI三种溶液可用AgNO3溶液
7、下列变化需要加入还原剂的为( )
A,MnO4-→Mn2+ B,CO32-→CO2 C,I- →I2 D,H2S→SO2
8、下列各组离子在溶液中能大量共存的为( )
A,H+. Ag+. Br-. K+ B,Ba2+. Cl-. OH-. Na+
C,Cl-.H+. Na+. ClO- D,NO3-. Na+. HCO3-. H+
9、下列物质中,不能使有色布条褪色的为( )
A,HClO溶液 B,Ca(ClO)2溶液 C,氯 水 D,CaCl2溶液
10、下列物质中,不能使润湿的淀粉KI试纸变蓝的是( )
A,HCl气体 B,碘水 C,氯水 D,溴水
11、下列判断碳酸氢钠粉末中混有碳酸钠的实验方法是( )
A,加热时有气体放出 B,滴加盐酸时有气体放出
C,溶于水后滴加BaCl2溶液,有白色沉淀产生
D,溶于水后滴加沉清石灰水,有白色沉淀产生
12、随着卤素核电荷数的递增,下列叙述正确的为( )
A,化合价逐渐升高 B,单质的氧化性逐渐增强
C,卤化氢的稳定性逐渐增强 D,单质的熔沸点逐渐升高
13、下列物质不能由金属单质和氯气直接化合生成的是( )
A,CuCl2 B,MgCl2 C,FeCl3 D,FeCl2
14、同温同压下,甲容器中的氢气(H2)和乙容器中的氨气(NH3)所含的分子个数相等,则这两
种容器的体积比为( )
A,1:2 B,2:3 C,1:1 D,3:1
15、下列溶液中Cl-浓度最大的是( )
A,1L0. 1mol・L-1的NaCl溶液 B,0. 5L 0. 1mol・L-1的HCl溶液
C,0. 2L0. 1mol・L-1的MgCl2溶液 D,0. 1L0. 1mol・L-1的AlCl3溶液
16、下列说法正确的为( )
A,需要加热才能发生的反应一定是吸热反应
B,放热的反应在常温下不一定能发生 C,吸热反应在一定条件下也能发生
D,反应物的总能量大于生成物的总能量的反应是吸热反应
17、1gN2含有M个N2分子,则阿伏加德罗常数可表示为( )
A,M / 28 B,M / 14mol-1 C,28M D,28mol-1
18、下列实验中有沉淀生成的是( )
A,将少量的金属钠放到水中 B,将少量的金属钠放到CuSO4溶液中
C,将少量的Na2O2放到水中 D,将少量的烧碱放到水中
19、某的的自来水利用了氯气消毒,一学生用该自来水来配制下列物质的溶液,溶质不会发生
变化的是( )
A,AgNO3 B,KI C,NaOH D,KCl
20、下列叙述中正确的为( )
A,标准状况下任何气体的体积都是22.4 L
B,两种气体的物质的量之比等于其分子数之比
C,1mol任何气体体积若是22. 4L,它必定处于标准状况
D,体积相同的任何气体都一定含有相同数目的分子
二、选择题(5小题10分。每小题有一个或两个答案。)
21、下列物质暴露在空气中,不是由于发生氧化还原反应而使质量增加的为( )
A,AgBr B,浓硫酸 C,Na2O2 D,NaOH
22、VL Al2(SO4)2溶液中含有m g Al3+,则该溶液中SO42―的物质的量浓度是( )mol・L-1
A,m / 3V B,m / 9V C,m / 18V D,m / 27V
23、下列离子方程式错误的为( )
A,大理石与盐酸反应:CaCO3 2H ==Ca2+ + CO2 + H2O
B,氢氧化钠与硝酸反应:OH-+ H+ === H2O
C,小苏打溶液与石灰水反应:CO32- + Ca2+ ===CaCO3
D、铜片与硝酸银溶液反应:Cu + Ag+ ===Cu2+ + Ag
24、能用离子方程H+ + OH-===H2O表示的化学反应是( )
A,氢氧化钠与盐酸反应 B,氢氧化钾与醋酸反应
C,氢氧化钡与硫酸反应 D,氢氧化铜与硫酸反应
25、25、将8.7gMnO2与足量的浓盐酸共热来制取氯气。有关说法正确的为( )
A,可制得14. 2g氯气 B,被氧化的HCl的质量为14. 6g
C,被氧化的HCl的质量为7. 3g D,转移的电子的物质的量为0. 1mol
三、填空题(有5小题,共25分)
26、(6分)根据卤素单质或化合物、碱金属元素单质或化合物的性质回答;
(1)可用在呼吸面具中用来作为氧气来源的物质是 。
(2)作过碘升华实验的烧杯内壁上的碘可用 洗涤。
(3)卤化物中可用做人工降雨的是 。
(4)用于消毒、制造漂白粉的是 。
(5)涂在照相感光相片上的是 。
(6)用作原子反应堆的导热剂的是 。
27、(4分)解释钠投入水中反应产生现象的原因:
(1)钠浮在水面上 。
(2)钠熔化成小球 。
(3)小球在水面上四处游动,并发出嘶嘶的声音 。
(4)滴有酚酞的溶液变红 。
28、(5分)按照要求各写出一个化学方程式;
(1)氯元素在反应被氧化未被还原的是
(2)氯元素在反应被还原未被氧化的是
(3)氯元素在反应既被氧化又被还原的是
(4)氯元素在反应既未被氧化又未被还原的是
(5)氯元素在反应前后化合价改变了6价
29、(4分)分别采用何种试剂或方法除去下列物质中的杂质(括号内为杂质)
(1)NaCl溶液(Na2CO3)
(2)Na2CO3固体(NaHCO3)
(3)炭粉(MnO2)
(4)盐酸(HClO)
30、(6分)A B C D四种化合物,其焰色反应通过蓝色钴玻璃片观察均为紫色。
A B C和盐酸反应均生成D,B和C等物质的量可反应生成A,在B的溶液中通入
一种无色无味的气体,适量时得A,气体过量得C,回答下列问题。
(1)写出下列物质的化学式;
A B C D
(2)写出下列变化的离子方程式:

四、实验题(有2小题,共15分)
31、(5分)实验室用二氧化锰和浓盐酸反应制氯气,根据如下实验装置,回答下列
问题
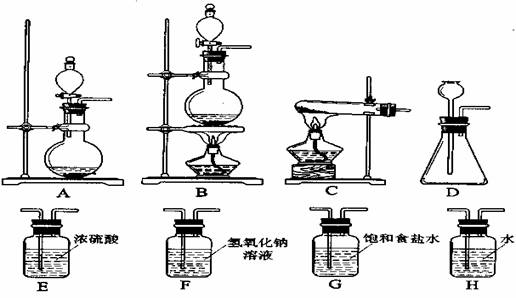
(1)写出反应的化学方程式:
(2)制取氯气时应选用的发生装置是(填装置序号)
(3)要得到纯净的氯气,应先后使用的气体净化装置是(填装置序号)
32、(10分)把98%(密度为1.84g / cm3)的浓硫酸稀释成3mol / L的稀硫酸100ml,
回答下列问题:
(1)需要量取浓硫酸 ml。
(2)配制操作可分解成以下几步;
(A)往 ml容量瓶注入蒸馏水,检查是否漏水。
(B)用少量蒸馏水洗涤烧杯及玻璃棒,将洗涤液注入容量瓶中并反复操作两次。
(C)将已 的稀硫酸注入已检不漏水的容量瓶中。
(D)根据计算,用 ml的量筒量取一定体积的浓硫酸(从规格为20ml 50ml 100ml的量筒中选取)
(E)将浓硫酸沿烧杯壁缓慢注入盛有少量蒸馏水的小烧杯中,并不断用
搅拌。
(F)盖上容量瓶塞子,振荡,摇匀。
(G)用 加蒸馏水,使溶液的凹面最低点恰好与刻度线相切
(H)继续往容量瓶中小心地加蒸馏水,使液面接近刻度线。
(3)以上正确的操作顺序为(填操作序号)
(4)若使用容量瓶之前,洗净的容量瓶存有少量的蒸馏水,对所要配制的溶液的浓
度 影响(填“有”或“无”)
五、计算题(2小题,共10分)
33、(4分)将标准状况下500L氯化氢气体溶解于1L水中,所得盐酸溶液的密度为
1. 19g / cm3。求该盐酸的物质的量浓度。
34、(6分)取50mlNa2CO3和Na2SO4的混合溶液,加过量的BaCl2溶液后得沉淀14.51g
用过量的稀硝酸处理后得沉淀4.66g,并有气体放出。试计算。
(1)原混合溶液中Na2CO3和Na2SO4的物质的量浓度。
(2)产生气体在标准状况下的体积。
参考答案;
一、选择题(40分) |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
A |
A |
B |
C |
C |
D |
A |
B |
D |
A | |
11 |
12 |
13 |
14 |
15 |
16 |
17 |
18 |
19 |
20 | |
C |
D |
D |
C |
D |
C |
D |
B |
D |
B | | ![]() MnCl2 2Cl2 ↑ 2H2O
MnCl2 2Cl2 ↑ 2H2O