(考试时间3小时,满分150分)
H
1.008
相对原子质量
He
4.003
Li
6.941
Be
9.012
B
10.81
C
12.01
N
14.01
O
16.00
F
19.00
Ne
20.18
Na
22.99
Mg
24.31
Al
26.98
Si
28.09
P
30.97
S
32.07
Cl
35.45
Ar
39.95
K
39.10
Ca
40.08
Sc
44.96
Ti
47.88
V
50.94
Cr
52.00
Mn
54.94
Fe
55.85
Co
58.93
Ni
58.69
Cu
63.55
Zn
65.41
Ga
69.72
Ge
72.61
As
74.92
Se
78.96
Br
79.90
Kr
83.80
Rb
85.47
Sr
87.62
Y
88.91
Zr
91.22
Nb
92.91
Mo
95.94
Tc
[98]
Ru
101.1
Rh
102.9
Pd
106.4
Ag
107.9
Cd
112.4
In
114.8
Sn
118.7
Sb
121.8
Te
127.6
I
126.9
Xe
131.3
Cs
132.9
Ba
137.3
La-Lu
Hf
178.5
Ta
180.9
W
183.8
Re
186.2
Os
190.2
Ir
192.2
Pt
195.1
Au
197.0
Hg
200.6
Tl
204.4
Pb
207.2
Bi
209.0
Po
[210]
At
[210]
Rn
[222]
Fr
[223]
Ra
[226]
Ac-La
Rf
Db
Sg
Bh
Hs
Mt
一、本题包括25小题,每小题2分,共50分。每小题有1个或2个选项符合题意。若该题只有1个选项符合题意,多选或错选均不得分。若该题有2个选项符合题意,选对1个得1分,选对2个得2分;选错1个,该题不得分。
1.下列卤素互化物中,最不稳定的是
(A)ClI3 (B)ClF3 (C)BrF3 (D)ICl3
2.下列各结构式中,最有可能的N2OLewis结构式为
(A)N=N=O (B)N ![]() \s N—O (C)N—N
\s N—O (C)N—N ![]() \s O (D)N=O=N
\s O (D)N=O=N
3.下列各金属碳化物中,与水反应能生成C3H4的是
(A)Be2C (B)Na2C3 (C)Mg2C3 (D)A14C3
4.在一定温度下,某浓度的硝酸与金属锌反应,生成NO2和NO的物质的量之比为1:3
则要使1摩金属锌完全反应,需要HNO3的物质的量为
(A)0.8 (B)2.4 (C)2.6 (D)2.8
5.在恒温条件下,有甲、乙两容器,甲容器为体积不变的密闭容器,乙容器为一个带有理想活塞(即无质量、无摩擦力的刚性活塞)的体积可变的密闭容器,两容器起始状态完全相同,都充有C气体,若发生可逆反应C(g) ![]() \s A(g) B(g),经一段时间后,甲、乙两容器反应都达到平衡。下列说法中正确的是
\s A(g) B(g),经一段时间后,甲、乙两容器反应都达到平衡。下列说法中正确的是
(A)平均反应速度:乙>甲 (B)平衡时nc(甲)>nc(乙)
(C)平衡时C的转化率: 乙>甲 (D)平衡时A的物质的量甲>乙
6.对手由CrO42—转化为Cr2O72—的下列各叙述中,正确的是
(A)这是Lewis酸碱反应 (B)这是氧化还原反应
(C)加酸,该反应向右移动 (D)加酸,该反应向左移动
7.在水溶液中,KHSO3(aq)的电荷平衡式为
(A)[H3O ]十[K ]=[OH—] [HSO3—] [SO32— ]
(B) [H3O ]十[K ]=[OH—] [HSO3—] 2[SO32— ]
(C) [H3O ]十[K ]=[OH—] [HSO3—] 1/2[SO32— ]
(D) [H3O ]十2[K ]=[OH—] [HSO3—] 2[SO32— ]
8.下列各组离子中,能在强碱性溶液中共存,且在滴加盐酸过程中会生成气体和沉淀的是
(A)Na 、CrO2—、SO42—、CO32— (B)NH4 、A1O2—、SO42—、CO32—
(C)K 、A1O2—、SO42—、HCO3— (D)K 、ZnO2—·、SO42—、CO32—
9.已知Al和Ga是同族元素,且都是两性元素,并知A1(OH)3的碱性比Ga(OH)3大。若将等物质的量的的Al和Ga溶于NaOH溶液中,然后再通入CO2,则
(A)Ga(OH)3先沉淀 (B)A1(OH)3和Ga(OH)3同时沉淀出来
(C)Al(OH)3先沉淀 (D)无法判断两种沉淀的先后次序
10.在抢救大出血的病危病人时,常需静脉点滴0.9%氯化钠溶液(从俗称“生理盐水’’),是由于人体血液的“矿化度”(即无机盐的含量)为0.9%。另有研究表明,30亿年前地表原始海水的“矿化度”即为0,9%。对此,下列猜测或评论中不足取的是
(A)人类祖先可能是从原始海洋逐渐进化到陆地上来的
(B)人体血液和原始海水的“矿化度”都为0.9%纯属巧合
(C)人体血液和原始海水之间存在着某种尚未认识的关系
(D)人体血液仍然带有原始海水的某些印痕
11.2004年4月16日重庆天原化工总厂的氯气贮罐发生泄漏,严重影响了附近群众的生命安全。下列有关安全措施中不正确的是
(A)可用毛巾蘸取石灰水捂嘴 (B)在氯气泄漏的地区人应站在高处
(C)向氯气中喷洒水 (D)将泄漏的氯气在空气中点燃除去
12.14C是宇宙射线与大气中的氮通过核反应产生的,它和12C以一定比例混合存在于空气中的二氧化碳里。14C随生物体的吸收代谢,经过食物链进入活的生物体中。当生物死亡之后新陈代谢停止,在以后年代里,12C通常不再发生变化,其数量固定下来,而14C具有放射性,仍不断衰变减少。与其有关的说法中不正确的是
(A) 14C与12C互为同位素
(B)0.012kg的14C中含有NA个碳原子数(NA表示阿伏加德罗常数)
(C)等物质的量的14C与12C所含的中子数不同
(D)可根据14C在生物体内的含量来计算生物体的死亡年代
13.下列离子方程式正确的是
(A)NaHCO3的水解:HCO3— H2O ![]() \s H3O CO32—
\s H3O CO32—
(B)过量的氯气通入溴化亚铁溶液中:3C12 2Fe2 4Br-=C1— 2Fe3 2Br2
(C)在NaHSO4溶液中滴入Ba(OH)2溶液至中性:
Ba2 2OH— 2H SO42—=BaSO4↓ 2H2O
(D)鸡蛋壳溶解在醋酸中:CaCO3 2H =Ca2 H2O CO2↑
14.A、B两元素的原子分别得到2个电子形成稳定结构时,A放出的能量大于B放出的能量:C、D两元素的原子分别失去一个电子形成稳定结构时,D吸收的能量大于C吸收的能量。若A、B、C、D间分别形成化合物时,属于离子化合物可能性最大的是
(A)D2A (B)C2B (C)D2B (D)C2A
15.下面四种化合物按酸性减弱的顺序排列正确的是
①CH3CH2COOH ②CH3CH2CH2OH ③ ![]() \s -OH ④CH3C
\s -OH ④CH3C ![]() \s CH
\s CH
(A)①>③>②>④ (B)②>①>④>③
 (C)②>③>①>④ (D)③>②>④>①
(C)②>③>①>④ (D)③>②>④>①
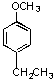
\s ![]() 16.反应 主要产物是
16.反应 主要产物是
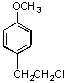
![]()
![]()
![]()
(A) (B) (C) (D)
![]()
![]()
17.反应 CH3CH2Br→+NaBr的反应类型是
(A)消除反应 (B)亲核取代反应 (C)亲电加成反应 (D)氧化反应
18.下列化合物中,能与H2O/H (Hg2 作催化剂)反应产生酮类化合物的是
![]()
![]()
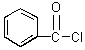
![]()
(A) (B) (C) (D)
 19.下列反应中,以高产率生成羧酸的反应是
19.下列反应中,以高产率生成羧酸的反应是
![]()
\s ![]() (A)CH3COOH (B)
(A)CH3COOH (B)
![]()
![]()
(C) (D) CH3C ![]() \s CCH3
\s CCH3
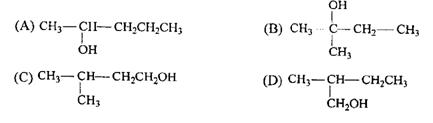 20.下列化合物中,最不易在酸性条件下被CrO3氧化的是
20.下列化合物中,最不易在酸性条件下被CrO3氧化的是
21.下列化合物中,沸点最高的是

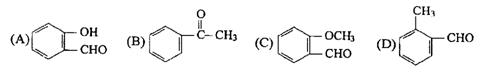
22.下列化合物中,与FeCl3反应生成有颜色产物的是
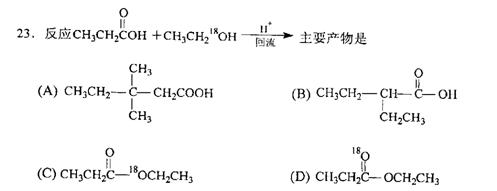
24.下列反应中,属于芳香族亲电取代反应的是
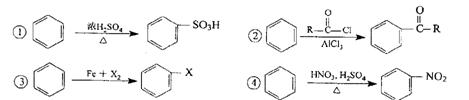
(A)①和② (B) ②和④ (C) ①、②和③ (D) ①、②、③和④
25.高氯酸是化合物中最强的酸,纯的高氯酸的沸点为130℃,市售浓度为70%(w/w),当浓度大于60%时,受热易分解,热而浓的高氯酸是强氧化剂,遇有机物易发生爆炸。在浓缩市售高氯酸时,最好的方法是
(A)磨口仪器,加浓硫酸后蒸馏 (B)磨口仪器,直接蒸馏
(C)磨口仪器,加浓硫酸后减压蒸馏 (D)磨口仪器,加浓磷酸后减压蒸馏
二、本题包括5小题,共22分。
26.(7分)A、B、C、D、E是5种短周期元素,它们的原子序数依次增大。A与D、C与E分别为同一主族元素,B与C为同周期元素。甲是由A与B形成的在常温下为气态的共价化合物:乙是由A和C形成的在常温下为液态的共价化合物;丙是由C和D形成的固态离子化合物。甲、乙、丙的化学式中原子个数比都为1:l。丁是由D和E形成的固态离子化合物,其中阳离子比阴离子少一个电子层。则各物质的化学式为甲_____;乙______或________;丙_______或________;丁________或_________。
27.(5分)科学家P.Tatapudi等人首先使用在酸性条件下电解纯水的方法制得臭氧。臭氧在_____极周围的水中产生,其电极反应式为_________________:在_______极附近的氧气则生成过氧化氢,其电极反应式为________________.电解的化学方程式为__________。
28.(4分)美国和欧洲的科学家合作,在同温层发现破坏臭氧的C12O2。在该化合物中,氯
的氧化数为_________:氧的氧化数为___________。Cl2O2的Lewis结构式为__________,该分子中所有原子____________(填:共或不共)平面。
29.(2分)2004年美国{科学}杂志报导了700'C时,在Rh-CeO2催化剂作用下;湿的乙醇
蒸气与足量空气反应制备氢气的方法。试以1mol乙醇作反应物,写出该反应的化学方程
式___________________________________·
30.(4分)四氧化三铁在强碱性溶液中与次氯酸盐反应,生成高铁(Ⅵ)酸盐,其化学反应方
程式是________________________。高铁酸盐的作用之一是净化水,这是因为__________________、____________________________________ .
三、本题包括6小题,共41分
31.(4分)美国加州大学Zettle教授所在的研究小组发现,在用改进的碳弧法合成C60和C70。得到的产物中发现了C36.已知C60有12个正五边形,20个正六边;C70有12个正五边形,25个正六边形。则C36有___________个正五边形,__________个正六边形。
32.(4分)在碱性溶液中Na2Sx与NaCIO反应,生成两种可溶盐溶液。在该混合液中加入BaCl2或AgNO3溶液都会生成不溶于稀酸的白色沉淀。经测试:1molNa2Sx与消耗6molNaOH恰好完全反应。x的值为_________;Na2Sx与NaCIO反应的离子方程式是______________________________。
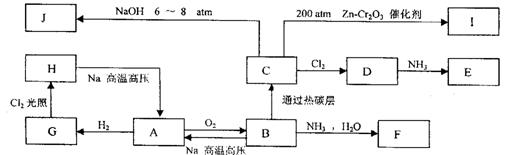 33.(10分)单质A是一种固体,它有多种同素异形体。B、C、H在常温下都是气体,F、E为化肥,但E的肥效和稳定性都比F高,A~J可以发生如下所示的转化:
33.(10分)单质A是一种固体,它有多种同素异形体。B、C、H在常温下都是气体,F、E为化肥,但E的肥效和稳定性都比F高,A~J可以发生如下所示的转化:
试写出A~J的化学式:A__________;B__________;C__________;D__________;F __________;G__________;H__________;I__________;J__________。
34.(10分)从某些性质看,NH3和H2O,NH4 和H3O ,OH—和NH2-,NH2—和O2-两两相似。
(1)试写出乙酸在液态氨中的形式___________.在水溶液中CH3COOH ![]() CH4 CO2,则乙酸在液态氨中的相应反应的方程式为________________________________。
CH4 CO2,则乙酸在液态氨中的相应反应的方程式为________________________________。
(2)在液态氟化氢中,SbF5成为导电强的溶液,其离子方程式为____________________,生成的两种物质的几何构型为______________,__________________。
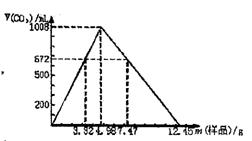 35.(6分)自然界存在的某天然碱(纯净物)的化学组
35.(6分)自然界存在的某天然碱(纯净物)的化学组
成可表示为aNa2CO3·bNaHCO3·cH2O(a、b、
c为正整数)。现称取不同质量的天然碱样品,溶于水后,分别逐滴加入相同浓度的盐酸溶液30mL,产生CO2的体积(标准状况)如右图所示。
(1)若用2.49g样品进行同样的实验时,产生CO2
的体积为多少mL(标准状况)?
(2)另取3.329天然碱样品于200℃加热至完全分解(200℃时Na2CO3不分解),产生CO2112mL(标准状况)和水0.45g,试通过计算确定该天然碱的化学式。
(3)实验中所用盐酸的物质的量浓度为多少?
36.(7分)天然氟矿主要有萤石、氟磷灰石等。由萤石矿制F2的方法是先用浓硫酸与萤石反应,生成HF,在HF中加入KF,再电解得F2。
(1)由萤石矿制F2的主要化学反应的方程式。①___________________②________________;
(2)之所以用硫酸而不用盐酸与萤石反应的理由是_________________________________;
(3)在制取过程中加入KF的作用是_________________________________________;
(4)F-对人体的危害是很严重的。人体中若含有过多的F-,F-会与人体内一种重要的金属阳离子形成难溶物,而带给人体严重的伤害和痛苦。这种阳离子是:__________。
四、本题包括4小题,共18分。
37.(4分)将反应产物填入方框内
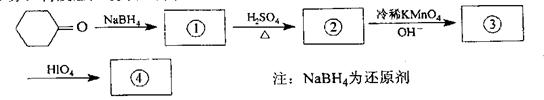
38.(4分)将反应产物填入方框内
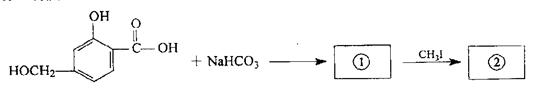
39.(4分)化合物(A)从元素分析可知只含有C、H两种元素,从有机质谱测定其分子量为
134:由红外光谱和核磁共振可知化合物(A)含有苯环,而且是对位二元取代苯;由核磁共
振可知化合物(A)含有五类不同化学环境的氢原子。请写出化合物(A)的结构式并用系统命
名法命名。
40.(6分)化合物(A)的分于式为C5H10O,不溶于水,与Br2/CCl4溶液和金属钠都无反应,
与稀盐酸、稀氢氧化钠反应得到同一化合物(B),分子式为C5H12O2。(B)与等物质量的HIO4
水溶液反应得到HCHO和化合物(C),分子式为C4H8O,(C)可发生碘仿反应。请写出化合
物(A)、(B)、(C)的结构式。
五、本题包括2小题,共19分。
41.(6分)某不活泼金属(A)重0.159g,在氯气中燃烧后,所得到产物经高温灼烧,恒重后得(B),溶于浓盐酸中得到黄色溶液(C)。此金属在氯气中燃烧后的产物再经高温灼烧时所得气体通入KI溶液后,再用0.1000mol/LNa2S2O3标准溶液滴定至终点,消耗25.00mL Na2S2O3溶液。
(1)通过计算写出(A)、(B)、(C)的化学式。
(2)写出由(A)变成(C)的化学反应方程式。
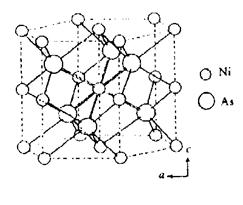 42.(13分)镍砷合金的晶体如右图所示
42.(13分)镍砷合金的晶体如右图所示
(1)试画出该合金的晶胞图
(2)试写出该合金的化学式
(3)试计算该合金的密度(晶胞参数为a=360.2pm, c=500.9pm)
(4)写出各原子分数坐标
(5)Ni利As的配位数分别为多少?它们各占有何种
空隙类型?