原子量:Na—23 Fe—56 Ag—108 Cl—35.5 Br—80 Mn--55
一、选择题
1.下列物质受光照射时,不会发生化学反应的是 ( )
A.H2和Cl2混合 B.H2和O2混合 C.氯水 D.AgBr
2.下列说法正确的是 ( )
A.用鼻子对着盛有氯气的瓶口,就可以闻到氯气的气味
B.用排水集气法便可以收集到纯净的氯气
C.氯气有漂白性
D.自来水常用氯气来杀菌、消毒
3.下列反应中,既能放出气体,又不是氧化还原反应的是 ( )
A.浓盐酸与二氧化锰共热 B.石灰石与稀盐酸反应
C.过氧化钠与水反应 D.铁与稀硫酸反应
4.下列无色有毒的气体是 ( )
A.氯气 B.氟气 C.一氧化碳 D.二氧化碳
5.随着卤素原子半径的增大,下列递变规律正确的是 ( )
A.单质的熔、沸点逐渐降低 B.卤素离子的还原性逐渐增强
C.单质的氧化性逐渐增强 D.气态氢化物的稳定性逐渐增强
6.下列化合物不能通过单质直接化合而得到的是 ( )
A.HI B.AlBr3 C.FeCl2 D.Na2O2
7.木炭、铁粉、二氧化锰、氧化铜、氧化亚铁均为黑色粉末,若只用一种试剂鉴别,应选择下列中的 ( )
A.稀硫酸 B.稀盐酸 C.稀硝酸 D.浓盐酸
8.在KBr和KI混合溶液中,通入足量的氯气,反应后蒸干溶液、灼烧,残留物是( )
A.KCl B.KCl和KBr C.KCl和KI D.KCl、Br2和I2
9.检验氯化氢气体中是否混有氯气,可采用的方法是 ( )
A.用干燥的蓝色石蕊试纸 B.用干燥的有色布条
C.将气体通入硝酸银溶液 D.用湿润的淀粉碘化钾试纸
10.大气或饮水被某种元素污染时,会引起牙齿、骨骼变疏松。这种元素是 ( )
A.汞 B.氟 C.碘 D.氯
11.甲、乙、丙三种溶液各含有一种X-(X-为Cl-、Br-、I-),向甲中加淀粉和氯水,则溶液变为橙色,再加丙溶液,颜色无明显变化.则甲、乙、丙依次含有 ( )
A.Br-、Cl-、I- B.Br-、I-、Cl-
C.I-、Br-、Cl- D.Cl-、I-、Br-
12.下面叙述正确的是 ( )
A.碘易升华,所以要保存在铁盖旋紧的试剂瓶中
B.液溴应保存在棕色磨口玻璃塞的试剂瓶中,并加少量水进行水封
C.漂白粉可置露在空气中保存
D.碘难溶于酒精
13.已知在酸性溶液中,下列物质氧化KI时,自身发生如下变化:Fe3 →Fe2 ;MnO4-→Mn2 ;
Cl2→Cl-;HNO2→NO。如果分别用等物质的量的这些物质氧化足量的KI,得到碘最多的是 ( )
A. Fe3 B. MnO4- C. Cl2 D. HNO2
14.下列离子方程式正确的是 ( )
A.碘化钾溶液跟适量溴水反应:I- Br2 == Br- I2
B.氯气与水的反应:Cl2 H2O == Cl- ClO- 2H
C.二氧化锰与浓盐酸反应:MnO2 4H 2Cl-== Mn2 Cl2↑ 2H2O
D. Cl2与氢氧化钠溶液的反应:Cl2 2 OH-== Cl- ClO- H2O
15.氯气与碘在加热的条件下以一定比例反应可得的一红棕色液体Icl(氯化碘),Icl的性质类似于卤素,有很强的化学活动性。例如:Icl H2O == HCl HIO,
2Zn 2Icl == ZnCl2 ZnI2 ,下列叙述正确的是 ( )
A.在Zn跟Icl的反应中,ZnI2既是氧化产物又是还原产物
B.在H2O跟Icl的反应中, Icl是氧化剂H2O是还原剂
C.在Zn跟Icl的反应中,ZnCl2既是氧化产物又是还原产物
D.在H2O跟Icl的反应中, Icl既是氧化剂又是还原剂
16.实验室用MnO2和浓盐酸制氯气时,有14.6g氯化氢被氧化,所得氯气全部用石灰乳吸收,可制得漂白精的质量是 ( )
A.14.3g B.25.4g C. 28.6g D.50.8g
17、有下列氧化还原反应
①2NaBrO3 Cl2====Br2 2NaClO3 ②HClO3 5HCl====3Cl2 3H2O
③2FeCl3 2KI====2FeCl2 I2 2KCl ④2FeCl2 Cl2====2FeCl3
其中氧化性由强到弱的顺序是
A NaBrO3>HClO3>Cl2>FeCl3>I2 B Cl2>FeCl3>I2>HClO3>NaBrO3
C I2>FeCl3>Cl2>HClO3>NaBrO3 D HClO3>NaBrO3>FeCl3>Cl2>I2
18、砹(At)是原子序数最大的卤族元素,推测砹或砹的化合物最不可能具有的性质是
A HAt很稳定 B砹易溶于某些有机溶剂
C AgAt不溶于水 D砹是有色固体
19、下列说法不正确的是
A某溶液中滴入AgNO3溶液,产生白色沉淀,该溶液中一定含Cl-。
B某溶液与淀粉碘化钾溶液反应后显蓝色,证明溶液是氯水或溴水。
C将氟气通入氯化钠水溶液中,一定有氢氟酸和O2生成。
D实验证明氯水也能导电,但氯水不是电解质。
20、实验室制氯气时有如下操作,操作顺序正确的是
①连接好装置,检查气密性 ②缓缓加热,加快反应,使气体均匀逸出
③在烧瓶中加入二氧化锰粉末 ④往分液漏斗中加入浓盐酸,再缓缓滴入烧瓶中
⑤用向上排空气法收集氯气,尾气导入吸收剂中
A ①②③④⑤ B ④③①②⑤ C ①③④②⑤ D ①④③②⑤
二、填空
21.现有KBr、AgNO3、CuCl2、NaOH四种溶液,置于A、B、C、D四支试管中,进行下列实验:
⑴把A和B中的溶液混合,产生蓝色沉淀
⑵把A和D中的溶液混合,产生白色沉淀
⑶把C和D中的溶液混合,产生浅黄色沉淀
由上述现象判断A、B、C、D四支试管中盛放的溶液分别是________,_________, _________,__________.有关的离子方程式___________________________________, ____________________________,________________________________。
22.除去KCl溶液中少量的KI,加入的试剂为______,化学方程式为__________________ 离子方程式为____________________.
23.有H2和Cl2的混合气体100mL(标准状况)。其中一种气体的体积为45mL,另一种气体的体积为55mL。光照使两种气体发生反应,反应后恢复到标准状况,气体体积为______mL。为了证明反应后的气体中H2或Cl2有剩余,使气体通过10mL水,并使剩余气体干燥后恢复到标准状况,若:
⑴ 剩余有________mL气体,证明有______剩余,理由是__________________________;
⑵溶液有________性质,证明有__________剩余,理由是__________________________。
24、欲除去下列物质中混有的少量杂质,简述所用的试剂及操作方法:
(1)液溴中混有少量的氯气 。
(2)氯气中混有少量的氯化氢气体 。
25.下图是制取无水氯化铜的实验装置图,将分液漏斗中的浓硫酸滴加到盛有固体食盐和二氧化锰混合物的烧瓶中,请回答下列问题:
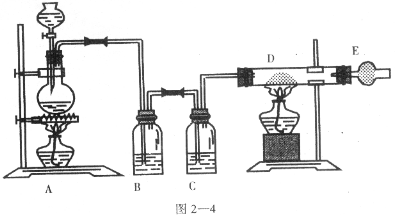
⑴烧瓶中发生反应的化学方程式是__________________________________________
⑵B瓶中的溶液是___________,其作用是________________;C瓶中的溶液是_________,
其作用是____________________。
⑶玻璃管D中发生反应的化学方程式为______________________,现象是__________。
⑷干燥管E中盛有碱石灰,其作用是________________________________________。
⑸开始实验时,应先点燃_______处的酒精灯。
三、计算题
26.铁的某种氯化物FeClx质量为1.625g溶于水后,加入足量的AgNO3溶液,产生的沉淀经洗涤干燥后称得质量为4.305g。求x的值和铁的氯化物的化学式。
27.将22gNaCl和NaBr的混合粉末溶于水,配成100mL溶液,向溶液中通入足量的Cl2后,将溶液蒸干,得到干燥固体的质量为17.55g,求:
⑴ 原混合物中NaCl的物质的量的浓度
⑵ 参加反应中的Cl2在标准状况下的体积
28.将8.7克MnO2和100毫升36.5%(密度为 1.19克每毫升)浓盐酸混合加热充分反应,求:
(1) 生成的氯气的物质的量为多少摩?
(2) 被氧化的HCL为多少克?
