第一节 碳族元素 (1课时)
姓名: 作业时限:40分钟 满分:50分 得分:
一、选择题(本题包括10小题,每小题3分,共30分。每小题有1~2个选项符合题意。)
1.下列物质的导电性介于导体和绝缘体之间的是( )。
(A)碲 (B)铅 (C)硒 (D)石墨
2.碳和硅的性质比较,正确的是( )。
(A)都是非金属,但硅的非金属性比较强
(B)碳和硅的最高正价都是 4价,负价都是-4价
(C)硅元素在地壳里含量居第二位,碳占第三位
(D)碳和硅元素的主要化合价均为 2和 4价
3.硅和碳的性质比较,下列说法正确的是( )。
(A)晶体硅和金刚石晶体结构相似,但晶体硅的硬度比金刚石小
(B)硅和碳都有 4价、 2价、—4价
(C)硅的化合物种类比碳的化合物种类多
(D)碳和硅在自然界都既能以游离态存在,又能以化合态存在
4.按照Si、P、S、C1的顺序,下列说法中正确的是( )。
(A)它们的非金属性由强到弱
(B)它们的单质与氢气化合由易到难
(C)它们的最高价氧化物的水化物的酸性逐渐增强
(D)它们的气态氢化物的稳定性逐渐增强
5.某元素最高价和负价的绝对值相等,核内质子数和中子数相等,该元素在气态氢化物中占87.5%(质量分数),则此元素为( )。
(A)S (B)N (C)C (D)Si
6.下列递变规律正确的是( )。
(A)导电性:石墨>晶体硅>金刚石
(B)稳定性:PbO2>PbO
(C)熔点:金刚石>石墨>Si>锡
(D)酸性:H2CO3>H2SiO3>H2GeO3
7.下列关于碳族元素的描述不正确的是( )。
(A)随着原子序数的增加,熔点逐渐升高
(B)它是非金属性向金属性过渡的典型族
(C)只能形成共价化合物,不能形成离子化合物
(D)除铅外,碳族元素均为 4价稳定化合物
8.某单质能跟浓硝酸反应,若参加反应的单质与硝酸的物质的量之比为1:4,则该元素在反应中所显示的化合价可能是( )。
(A) 1 (B) 2 (C) 3 (D) 4
9.根据锗在元素周期表中的位置,推测其单质及化合物中不可能有的性质是( )。
(A)锗的金属性比非金属性强
(B)二氧化锗易溶于水
(C)SiH4比GeH4稳定
(D)Ge(OH)2的碱性比Pb(OH)2的强
10.若发现114号元素X,它的最外层电子结构和碳相同,比碳多5个电子层,则下列叙述正确的是( )。
(A)X有稳定的气态氢化物
(B)X为非金属元素
(C)X的最高价氧化物为XO2
(D)X的低价氧化物是酸性氧化物
二、填空、简答题(本题包括4小题,共20分。)
11.(2分)课本上说:“……碳、硅、锗、锡的 4价化合物是稳定的,而铅的 2价化合物是稳定的。”根据以上所述判断:锡的 2价化合物(如SnCl2)应具有较强的_________性,铅的 4价化合物应具有较强的_________性。
12.(4分)锗元素的最高价氧化物的化学式是_________,它与盐酸反应的化学方程式是___________________________;氨氧化钠反应的化学方程式是___________________________。
13.(8分)Fe3O4可以写成FeO·Fe2O3,若看作一种盐时,又可写成Fe(FeO2)2。根据化合价规律和这种书写方法,若将Pb3O4用上述氧化物形式表示,其化学式可以写成_________;看成盐可以写成_________。等物质的量的Fe3O4和Pb3O4分别在一定条件下和浓盐酸反应时,所消耗HCl的物质的量相等;不同的是,高价铅能将盐酸氧化而放出氯气。写出Fe3O4、Pb3O4分别和浓盐酸反应的化学方程式:____________________________________。
14.(6分)工业生产的纯碱常常含有少量NaCl等杂质。下图为测定纯碱纯度的方法之一。 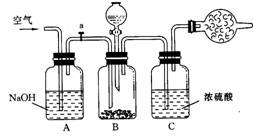
操作步骤是:
(1)检查气密性后,在干燥管中装入碱石灰,称 得重Wl g。
(2)称取一定量纯碱试样(W2g),放入B瓶。
(3)从分液漏斗中缓缓加入稀硫酸,直到不再产 生气体为止。
(4)打开开关d,缓缓鼓入空气5分后,再称得 干燥管总质量为W3 g。
回答下列问题:
(1)鼓入气体的目的是_________。
(2)装置A的作用是_________。
(3)装置C的作用是_________。
(4)纯碱的纯度计算式为_________。
(5)若去掉A,测定结果将_________ (填“偏大”、“偏小”、“无影响”)。
(6)若去掉C,测定结果将_________ (填“偏大”、“偏小”、“无影响”)。
第七章 硅和硅酸盐
第一节 碳族元素 (1课时)
一、1C;2B;3A;4CD;5D;6AD;7AC;8BD;9BD;10C
二、11.还原、氧化
12. CeO2,CeO2 4HCl=CeCl4 2H2O CeO2 2NaOH=Na2CeO3 H2O
13. 2PbO·PbO2或Pb2(PbO4),化学方程式为:
Fe3O4 8HCl=FeCl2 2FeCl3 4H2O Pb3O4 8HCl=3PbCl2 O2↑ 4H2O
14. (1)赶走残留在广口瓶以及装置中的二氧化碳,使二氧化碳全部进入干燥管保证二氧化碳全部被吸收 (2)防止空气中的二氧化碳的干扰 (3)防止水蒸气进入干燥管导致结果误差
(4) ![]() (5) 偏大 (6) 偏大
(5) 偏大 (6) 偏大
