说明:
1. 本卷分第I卷(选择题)和第Ⅱ卷(非选择题)两部分,满分100分,考试时间90分钟。
2. 答题前,考生务必将自己的班级、姓名、座号填写在试卷指定位置。
3. 答案写在各题指定的答题处。
可能用到的相对原子质量:H 1 C 12 N 14 O 16 S 32 Cu 64 Na 23 Mg 24 Al 27 Cl 35.5
第Ⅰ卷(选择题 共54分)
一、选择题(本题包括18小题,每小题3分,共54分,每小题只有一个正确答案):
1.2008年9月25日晚9时10分,我国“神舟七号”载人飞船顺利升入太空。
此次火箭的主要燃料是偏二甲肼(用R表示)和四氧化二氮,在火箭发射时,两者剧烈反应产生大量气体并释放出大量的热,该反应的化学方程式为:
R 2N2O4 = 3N2 4H2O 2CO2,下列叙述错误的是 ( )
A.此反应是氧化还原反应
B.反应瞬间产生大量高温气体,推动火箭飞行
C.在反应中N2O4做还原剂
D.R的分子式为C2H8N2
2、银耳本身为淡黄色,某地生产的一种“雪耳”,颜色洁白如雪。制作如下:将银耳堆放在密闭状态良好的塑料棚内,棚的一端支口小锅,锅内放有硫磺,加热使硫磺熔化并燃烧,两天左右,“雪耳”就制成了。“雪耳”炖而不烂,对人体有害,制作“雪耳”利用的是 ( )
A.硫的还原性 B.硫的漂白性
C.二氧化硫的还原性 D.二氧化硫的漂白性
3、下列物质中,不含有硅酸盐的是 ( )
A.水玻璃 B.硅芯片 C.黏土 D.普通水泥
4.下列有关试剂的保存方法,错误的是 ( )
A.浓硝酸保存在无色玻璃试剂瓶中
B.少量的钠保存在煤油中
C.氢氧化钠溶液保存在带橡皮塞的玻璃试剂瓶中
D.新制的氯水通常保存在棕色玻璃试剂瓶中
5、下列说法正确的是 ( )
A、硫酸、纯碱、醋酸钠和生石灰分别属于酸、碱、盐和氧化物
B、蔗糖、硫酸钠和水分别属于非电解质、强电解质和弱电解质
C、点燃的镁条不能在二氧化碳气体中继续燃烧
D、含0.2molH2SO4的浓硫酸与足量的铜反应,生成标准状况下的气体2.24L
6、下列装置所示的实验中,能达到实验目的的是 ( )
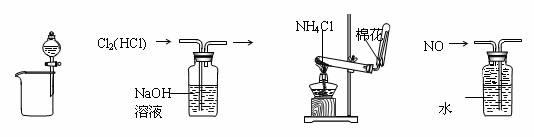
A.分离碘和酒精 B.除去Cl2中的HCl C.实验室制氨气 D.排水法收集NO
7、某无色酸性溶液中,则该溶液中一定能够大量共存的离子组是 ( )
A.Fe2 、Ba2 、NO3-、Cl- B.Na 、NH4 、SO42-、Cl-
C.Na 、K 、SO32-、NO3- D.Na 、K 、MnO4-、Br-
8.下列反应的离子方程式书写正确的是 ( )
A.用FeCl3溶液腐蚀印刷电路板:Fe3++Cu=Fe2++Cu2+
B.氯气跟水反应:Cl2 H2O= H+ Cl- HClO
C.钠与水的反应:Na+H2O=Na++OH-+H2↑
D.AlCl3溶液中加入足量的氨水:Al3 3OH- ══ Al(OH)3↓
9、实验室制备氨气,检验是否收集满的正确方法是 ( )
A、用手扇动收集的气体,有气味则已收集满
B、将润湿的淀粉-KI试纸接近瓶口,试纸变蓝则已收集满
C、将润湿的红色石蕊试纸伸入瓶内,试纸变蓝则已收集满
D、用玻璃棒一端蘸取浓盐酸,接近瓶口,产生大量白烟,证明已收集满
10.a mol O2气体和a mol O3气体相比较,下列叙述一定正确的是 ( )
A.体积相同 B.原子数相等 C.分子数相等 D.质量相等
11.下列关于复合材料的说法中,不正确的是 ( )
A.复合材料一般具有强度高、质量轻、耐高温、耐腐蚀等优异性能,在综合性能上超过了单一材料。
B.玻璃钢是以玻璃纤维和树脂组成的复合材料,它可做船体、汽车车身等,也可做印刷电路板。
C.制造网球拍用的复合材料是在合成树脂的基体中加入了碳纤维做增强体
D.由两种或两种以上金属(或非金属)熔合而成的物质叫复合材料
12.判断下列有关化学基本概念的依据正确的是 ( )www.ks5u.com
A.氧化还原反应:元素化合价是否变化.
B.纯净物与混合物:是否仅含有一种元素
C.强弱电解质:溶液的导电能力大小
D.溶液与胶体:本质不同的原因是能否发生丁达尔效应
13、从海水(含氯化镁)中提取镁,可按如下步骤进行:
①把贝壳制成石灰乳[Ca(OH)2]; ②在引入的海水中加入石灰乳,沉降、过滤、洗涤沉淀物; ③将沉淀物与盐酸反应,结晶过滤、在HCl气体氛围中干燥产物; ④将得到的产物熔融电解得到镁。下列说法不正确的是 ( )
A.此法的优点之一是原料来源丰富
B.①②③步骤的目的是从海水中提取MgCl2
C.以上提取镁的过程中涉及分解、化合和复分解反应
D.第④步电解不是氧化还原反应
14.用NA代表阿伏加德罗常数的值,下列有关说法正确的是 ( )
A.3mol NO2与足量H2O反应,转移的电子数为NA
B.常温常压下,22.4L氦气含有NA个氦原子
C.标准状况下,22.4L单质溴所含有的原子数目不为2NA
D.钠在氧气中燃烧,1 mol O2作氧化剂时得到的电子数为4NA
15、某单质在氧气中燃烧,能生成氧化物有两种,且常温下均为气体,则该单质为 ( )
A.S B.N2 C.C D.Si
16、鉴别NaCl、NaBr、NaI可以采用的试剂是 ( )
A.碘水、淀粉溶液 B.碘化钾淀粉溶液 C.溴水、苯 D.氯水、CCl4
17、为检验一种氮肥的成分,某学习小组的同学进行了以下实验: = 1 \* GB3 ①加热氮肥样品生成两种气体,其中一种气体能使湿润的红色石蕊试纸变蓝,另一种气体能使澄清石灰水变浑浊。 = 2 \* GB3 ②取少量该氮肥样品溶于水,并加入少量BaCl2溶液,没有明显变化。由此可知该氮肥的主要成分是 ( )
A.NH4HCO3 B.NH4Cl C.(NH4)2CO3 D.NH4NO3
18.锌与很稀的硝酸反应生成Zn(NO3)2 、NH4NO3和水。当生成1mol硝酸锌时,被还原的硝酸的物质的量为 ( )
A.0.25mol B.0.5mol C.1mol D.2mol
第Ⅱ卷(共46分)
19、(4分)下列实验方法合理的是 。(多选不给分)
A、可用盐酸与BaCl2溶液来鉴定某未知试液中是否含有SO42-。
B、用加热法除去食盐固体中的氯化铵。
C、将碘的饱和水溶液中的碘提取出来,可用四氯化碳进行萃取
D、实验室制取Al(OH)3:往AlCl3溶液中加入NaOH溶液至过量。
E、用澄清石灰水鉴别Na2CO3溶液和NaHCO3溶液。
F、往FeCl2溶液中滴入KSCN溶液,检验FeCl2是否已氧化变质。
20、(4分)SiO2广泛存在自然界中,其用途也非常广泛,可用于制造光导纤维,也用于生产半导体材料硅。
(1)写出工业上制备粗硅的化学反应方程式 。
(2)SiO2耐腐蚀,但易溶于氢氟酸,写出化学反应方程式:
。
21、(11分)铝是一种重要金属:
(1)生产中曾用铝热反应焊接钢轨,则铝与氧化铁发生反应的化学方程式为:
。
|
高温 |
V2O5 Al ==== Al2O3 V
该反应中氧化剂是 ,要得到1mol金属钒,需要纯铝的质量 g。
(3)铝与NaOH溶液反应的离子方程式为:
。
在同温同压下,等质量铝投入足量盐酸和NaOH溶液中,产生气体的体积之比为 。
22、(10分)某些化学反应可用下式表示
A B ─→ C D H2O
请回答下列问题:
(1)若A、C、D均含有氯元素,且A的化合价介于C与D之间,写出该反应的离子方程式: 。
(2)若C为氯化钠,D能使澄清石灰水变浑浊的无味气体,则A与B的组合是: 或 。
(3)若A为紫红色金属,D为红棕色气体,请写出符合上式的化学方程式:
。
(4)若C、D均为气体且都能使澄清石灰水变浑浊,则A与B的组合是 。
23、(9分)某化学小组欲探究不同价态硫元素间的转化,请回答下列问题:
(1)除胶头滴管、酒精灯外,你认为本实验必不可缺少的一种玻璃仪器 是 。
(2)请帮他们完成以下实验报告:
实验目的:探究三种价态(0、 4、 6)硫元素间的相互转化。
选用试剂:硫磺、浓硫酸、二氧化硫、氯水、硫化氢、铜片、氧气。
实验记录(划斜线部分不必填写):
|
实验编号 |
预期的转化 |
选择的试剂 |
实验现象 |
结论(用化学方程式表示) |
|
① |
S→SO2 |
硫磺、 氧气 |
| |
|
② |
SO2→S |
二氧化硫、 硫化氢 |
|
SO2 2H2S===3S↓ 2H2O |
|
③ |
SO2→H2SO4 |
二氧化硫、 氯水 |
氯水退色 |
|
|
④ |
H2SO4→SO2 |
|
问题讨论:从三种价态(0、 4、 6)硫元素间的相互转化还可得到规律:当硫元素处于最低价时只有还原性,处于最高价时只有氧化性,处于中间价时既有氧化性、又有还原性。
(3)根据以上规律判断,下列物质中既有氧化性,又有还原性的有: 。(填序号)
A.Cl2 B.Na C.Na D.Cl- E.SO2
24、计算题:(8分)
将0.2molMg、Al的混合物用盐酸完全溶解,放出标准状况下5.6L气体,然后再滴入2mol/LNaOH溶液,请回答:
(1) 求该混合物中Mg、Al的物质的量?(写计算过程)
(2) 若该Mg、Al的混合物与盐酸恰好完全反应,在滴加NaOH溶液过程中,欲使Mg2 、Al3 刚好沉淀完全,则滴入NaOH溶液的体积V= ml。
(3) 若该Mg、Al混合物溶于200ml 3mol/L盐酸后,滴入NaOH溶液,使所得沉淀中无Al(OH)3,则滴入NaOH溶液的体积最少为 ml。
高一化学参考答案及评分标准
一、选择题(每小题3分,共54分,每小题只有一个正确答案):
题号
1
2
3
4
5
6
7
8
9
答案
C
D
B
A
B
D
B
B
D
题号
10
11
12
13
14
15
16
17
18
答案
C
D
A
D
C
C
D
A
A
第Ⅱ卷(共46分)
19、(共4分) A、B、C、F 。(选对一个给1分)
20、(共4分)(1)SiO2 2C===Si 2CO↑。(2)SiO2 4HF=SiF4↑ 2H2O(各2分)
21、(共11分)
|
高温 |
(2) 3 V2O5 10Al === 5 Al2O3 6 V(2分)V2O5(1分),45(2分)。
(3)2Al 2OH— 6H2O=2[Al(OH)4]— 3H2↑(2分),1:1(2分)
22、(每空2分,共10分)
(1)Cl2 2OH—=Cl— ClO— H2O。(2)Na2CO3、HCl或NaHCO3、HCl。
(3)Cu 4HNO3(浓)=Cu(NO3)2 2NO2↑ 2H2O。(4)碳与浓硫酸。
23、(9分)(1)试管(1分)
(2)
|
① |
S→SO2 |
硫磺、 氧气 |
蓝紫色火焰(1分) |
|
|
② |
SO2→S |
|
SO2 2H2S===3S↓ 2H2O | |
|
③ |
SO2→H2SO4 |
二氧化硫、氯水 |
氯水退色 |
SO2 Cl2 2H2O=H2SO4 2HCl (2分) |
|
④ |
H2SO4→SO2 |
铜片、 浓硫酸 (1分) |
|
Cu 2H2SO4==CuSO4 SO2↑ 2H2O(2分) |
(3)A、E。(2分,选错、选不全不给分)
24、计算题:(8分)
(1)n(Mg)=0.1mol、(2分)n(Al)=0.1mol(2分)
(2)250(2分)(3)350(2分)



 二氧化硫、硫化氢
二氧化硫、硫化氢