考生须知:
1.全卷分为试题卷和答题卷两部分。试题共有六大题,27小题,满分150分。考试时间120 分钟。
2.本卷答案必须做在答题卷相应位置上,做在试题卷上无效,考后只交答题卷。必须在答题卷上写明县(市)、学校、姓名、准考证号,字迹清楚。
一.选择题(本题包括10小题,每小题4分,共40分,每小题只有1个正确答案)
1.常温时,以下4种溶液pH最小的是
(A)0.01 mol·L-1 醋酸溶液
(B)0.02 mol·L-1醋酸与0.02 mol·L-1NaOH溶液等体积混合液
(C)0.03 mol·L-1醋酸与0.01 mol·L-1NaOH溶液等体积混合液
(D)pH=2的盐酸与pH=12的NaOH溶液等体积混合液
2.某有机物分子组成为C9H12,它不能使溴水褪色,但可以使酸性KMnO4溶液褪色,其可能结构有多少种
(A)6 (B)7 (C)8 (D)9
3.测定相对分子质量的常用方法之一是凝固点下降法。例如水是常用的溶剂,当水中溶解了某种不挥发的溶质时,水的凝固点(即冰点)即会下降,海水在0℃时不会结冰就是这个原因。凝固点下降的程度与溶质的分子数有关,而与溶质是何种物质无关。当溶剂的量确定时,凝固点的降低值与溶质分子数成正比。已知10.0 g樟脑中溶解0.412 g萘,凝固点下降了13℃,即么,组成为C7H6O2的有机物0.23 g溶于15.6 g樟脑中,凝固点下降约多少?
(已知萘的相对分子质量为:128)
(A)5℃ (B)8℃ (C)7℃ (D)12℃
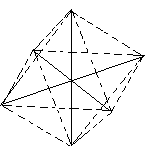 4.已知[Co(NH3)6]3 呈正八面体结构,若其中有两个NH3分子分别被Cl-和H2O取代,所形成的[Co(NH3)2Cl2(H2O)2]3 的几何异构体种数有(不考虑光学异构)几种
4.已知[Co(NH3)6]3 呈正八面体结构,若其中有两个NH3分子分别被Cl-和H2O取代,所形成的[Co(NH3)2Cl2(H2O)2]3 的几何异构体种数有(不考虑光学异构)几种
(A)3种 (B)4种 (C)5种 (D)6种
5.由解放军总装备部军事医学研究所研制的小分子团水,解决了医务人员工作时的如厕难题。新型小分子团水,具有饮用量少、渗透力强、生物利用度高、在人体内储留时间长、排放量少的特点。一次饮用125 mL小分子团水,可维持人体6小时正常需水量。下列关于小分子团水的说法正确的是
(A)水分子的化学性质改变 (B)水分子中氧氢键长缩短
(C)水分子间作用力减小 (D)水分子间结构、物理性质改变
6.往体积不变的密闭容器中充入一种体积比为1:10的气态烃和O2的混合气体,将该混合气体点火引爆,完全反应后在127℃时测得气体压强为p,恢复到常温27℃时测得气体压强为p/2,则该气态烃可能是
(A)CH4 (B)C2H6 (C)C4H8 (D)C6H10
7.氯磺酸(ClSO3H)是一种轻易水解的一元强酸,它能与多种物质发生反应。下列说法正确的是
(A) ClSO3H与甲酸的反应式是:HCOOH ClSO3H——→CO HCl H2SO4
(B) ClSO3H与足量NaOH溶液反应的主要产物是ClSO3Na
(C) ClSO3H的制备既可用氯化氢气体与三氧化硫反应,又可用浓盐酸与浓硫酸反应得到
 (D)同样是0.1 mol·L-1的ClSO3H与HCl分别溶于水制成1L溶液,两者的pH相同
(D)同样是0.1 mol·L-1的ClSO3H与HCl分别溶于水制成1L溶液,两者的pH相同
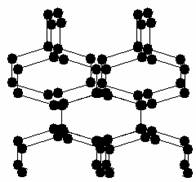
8.2004年7月德俄两国化学家共同公布,在高压下氮气会发生聚合得到高聚氮,这种高聚氮的N-N键的键能为160kJ/mol(N2的键能为942kJ/mol),晶体片段结构如右图所示。又发现从N2可制取出N5、N3。含N5 离子的化合物及N60、N5极不稳定。则下列说法错误的是
(A)按键型分类,该晶体中含有非极性共价键
(B)含N5 离子的化合物中既有离子键又有共价键
(C)高聚氮与N2、N3、N5、N5 、N60互为同素异形体
(D)这种固体的可能潜在应用是烈性炸药或高能材料
9.“熵”可看作是“混乱度”,它的符号是“S”。下列变化中,△S<0(“混乱度”减小)的是
(A)3Fe(s) 4H2O(g)→Fe3O4(s) 4H2(g) (B)2NO2(g)→N2O4(l)
(C)2IBr(l)→I2(s) Br2(g) (D)(NH4)2CO3(s)→2NH3(g) CO2(g) 2H2O(g)
10.下列离子方程式不正确的是
(A)等体积、等物质量浓度的Ca(H2PO4)2溶液与NaOH溶液混合:
Ca2 H2PO4- OH- == CaHPO4↓ H2O
(B)把过量碳酸氢钠溶液加入到氢氧化钡溶液中:
2HCO3- Ba2 2OH- == BaCO3↓ CO32- 2H2O
(C)在Na2HPO4溶液中滴入少量AgNO3溶液:3Ag HPO42- == Ag3PO4↓ H
(D)等体积、等物质的量浓度的明矾溶液和Ba(OH)2溶液混合:
3Ba2 6OH- 2Al3 3SO42- === 2Al(OH)3↓ 3BaSO4↓
二.选择题(本题包括8小题,每小题4分,共32分。每小题有1~2个正确答案。若有两个正确选项,只选一个且正确的给2分,多选、错选都给0分)
11. 现有一瓶失去标签的纯净铵盐,为测定其中的含氮量可以采用“甲醛法”,即:
4NH4 6HCHO→(CH2)6N4 4H 6H2O。现在称取2 g该铵盐溶于水,加入足量的甲醛溶液后,再加入水配成100 mL溶液,取出10 mL,滴入酚酞后再逐滴滴入0.1 mol·L-1的NaOH溶液,当滴到25 mL时溶液呈粉红色,且在半分钟内不褪色,则该铵盐中氮的质量分数是
(A)17.5% (B)17.7% (C)21.2% (D)35%
12.近年来科学家们发现由100个碳原子构成具有完美对称性的C100原子团,每个碳原子可形成4个化学键,最内部是由20个碳原子构成的正十二面体,外层的60个碳原子形成12个分立的正五边形,处于中间层次的碳以单键方式将内外层碳原子连接在一起,当它与氟的单质反应形成分子时,其分子式应为
(A)C100F60 (B) C100F20 (C) C100F12 (D) C100F40
13.相对分子质量为342的糖,其结构简式为
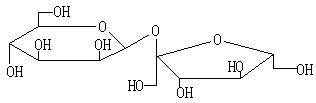 |
已知这种糖跟氯酸钾反应后生成的产物是氯化钾、二氧化碳和水,则反应中氧化产物跟还原产物的物质的量之比为
(A)3:2 (B)2:3 (C)8:1 (D)11:8
14.有编号为1、2、3、4的四瓶无色液体,仅知道是苯、甲苯、氯苯和二甲苯中的分别一种,现在要求甲、乙、丙、丁四位同学进行鉴别,而且每人只鉴别两瓶,告诉学生两瓶鉴别都正确得满分,只有一瓶正确的可以及格。四位同学的结果如下:
甲
1号为甲苯
4号为二甲苯
老师评价:四位同学都及格,但是没有一个满分。
乙
1号为氯苯
3号为甲苯
丙
1号为苯
2号为甲苯
丁
4号为甲苯
2号为氯苯
根据实验结果及老师的评价,以下对四瓶无色液体的成分判定正确的是
(A)1号是苯 (B)2号是二甲苯 (C)3号是氯苯 (D)4号是甲苯
 15.氢气是重要而洁净的能源,要利用氢气作能源,必须安全有效地储存氢气。有报道称某种合金材料有较大的储氢容量,其晶体结构的最小单元如右图所示。则这种合金的化学式为
15.氢气是重要而洁净的能源,要利用氢气作能源,必须安全有效地储存氢气。有报道称某种合金材料有较大的储氢容量,其晶体结构的最小单元如右图所示。则这种合金的化学式为
(A)LaNi6 (B) LaNi3
(C) LaNi4 (D) LaNi5
16.分别配制H3PO4、KOH的乙醇溶液,取10 mL磷酸溶液在不断振荡下,滴加KOH溶液立即产生白色沉淀,并不断增多,继而又逐渐减少至消失,然后又逐渐增多到一定量不再消失,以上事实说明
(A)K2HPO4学溶于无水乙醇 (B)KH2PO4、K3PO4不溶于无水乙醇
(C)KH2PO4、K2HPO4不溶于无水乙醇 (D)K2HPO4溶于无水乙醇
17,加拿大阿尔贡天文台在星际间发现了HC9N链状分子,其结构式为:CH≡C-C≡C-C≡C-C≡C-C≡N,这是人类发现的最重星际有机分子,有关该分子的说法不正确的是
(A)该物质属于不饱和烃
(B)该分子碳、氮原子均满足八电子结构
(C)该分子所有原子处在一条直线上
(D)1mol该物质在一定条件下可与8molH2发生加成反应
18.有一包白色固体,可能有①(NH4)2SO4,②Al2(SO4)3,③NaCl,④AgNO3,⑤KOH,⑥KI,⑦BaCl2中的一种或几种组成,该固体溶于水得到澄清溶液,而且该溶液能使酸酞呈红色,若在该溶液中加入适量的稀硝酸,可得到白色沉淀。该白色固体可能的组成是
(A)②③⑤ (B)②⑤⑦ (C)①③④⑤ (D)①④⑤⑦
三、填空题(本题包括3个小题,共20分)
19.(6分)0.1 mol某有机物A在O2中完全燃烧,生成的气体通过足量的澄清石灰水生成沉淀13.9 g,则有机物A的分子式为 ,A在O2中燃烧的化学方程式为
。
20.(8分)电子可以和其它阴离子一样,以溶剂化形式存在于氨、醇和水溶液中。
(1)当用高能射线照射液态水时,水分子便按照一种新的方式电离,写出水分子电离的方程式 。
(2)电离出来的高能电子经频繁碰撞后,被若干水分子以氢键方式形成的网捕捉形成水合电子,这种水合电子可以用 通式来表示。
(3)与电子同时生成的阳离子通过与水反应生成羟基自由基(·OH),该反应的离子方程式为 .
(4)经过高能射线照射的水的最主要的化学性质为 和 。
21.(6分)将一定量的晶体物质A,放在真空的密闭容器中加热到200℃时,A全部分解为4种气体,而且它们的物质的量相等。若再冷却容器到一定温度时,又发现有晶体物质B生成,此时原4种气体中有一种没有参加反应,已知该种气体在相同条件下相对于氢气的密度为14,而且能够在空气中燃烧。
(2)上述A分解所得的4种气体中有2种气体在一定条件下若以2:1 的物质的量进行反应可以生成常见的有机化肥C,则C的结构简式 。
四.简答题(本题包括2个小题,共19分)
22.(8分)石灰氮(固体甲)是一种古老而多用途的有效肥料,它很轻易用廉价的普通化学品乙来生产,乙高温加热分解产生白色固体A和无色气体B,后者不支持燃烧。用碳高温还原A生成灰色固体C和气体D,C和D能进一步氧化,且C必须密封保存,否则遇潮湿空气即产生含碳质量分数最高的常见气态烃,C与氮气反应,最终生成固体甲。经测定固体甲由三种元素组成,其中钙元素占50.00%、碳占15.00%(元素质量分数)
(1)完成下列合成固体甲的反应方程式:
|
①乙—————→A B
②A 碳——→C D
③C 氮气——→甲 单质
(2)写出固体甲水解的反应方程式 。
23.(8分)MMT是用于提高汽油辛烷值的四乙基铅被禁用后于1976年首先在加拿大出现的汽油添加剂。该化合物的结构可以看作是两种较早合成的金属有机化合物二茂铁Fe(C5H5)2和四羰基合镍Ni(NO)4的杂交变种。经测定MMT的相对分子质量 O2的6.8125倍,组成元素的质量分数分别为:C 49.54%、Mn 25.23%、H 3.21%、O 22.02%。通过计算确定MMT的化学式,并画出它的合理的结构简式。
24.(6分)化学中有许多有趣的实验,如下介绍的“蓝瓶子”实验就是一例。
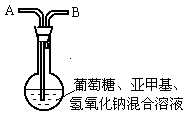 在250 mL平底烧瓶中依次加入2g氢氧化钠、100mL蒸馏水、2g葡萄糖(粉末),振荡使其溶解。滴入4~6滴0.2%的亚甲基蓝溶液,塞上瓶塞(如图),振荡烧瓶,溶液呈蓝色。静置,约3分钟后蓝色消失,变为无色。再次振荡,无色溶液又呈蓝色。可反复多次。为探究是什么原因引起的,有人做了以下实验。
在250 mL平底烧瓶中依次加入2g氢氧化钠、100mL蒸馏水、2g葡萄糖(粉末),振荡使其溶解。滴入4~6滴0.2%的亚甲基蓝溶液,塞上瓶塞(如图),振荡烧瓶,溶液呈蓝色。静置,约3分钟后蓝色消失,变为无色。再次振荡,无色溶液又呈蓝色。可反复多次。为探究是什么原因引起的,有人做了以下实验。
(1)从烧瓶中取出溶液注满一支试管,塞上橡皮塞。试管中的溶液由蓝色变为无色,再振荡试管溶液不能变蓝。
(2)在原烧瓶中经A处鼓入空气,又慢慢变蓝了。静置片刻后,蓝色又消失。再次鼓入空气,又慢慢变蓝。
(3)为了进一步弄清是何种成分引起的,他又继续探索。从A处改通纯净的N2、CO2,都不能使烧瓶中的无色溶液变蓝。把制得的氧气从A处通入,发现上述无色溶液慢慢变为蓝色,到此为止,“蓝瓶子”实验原理有了科学结论,请总结“蓝瓶子”实验的变色原理:
。
五.(本题包括2个小题,共24分)
25.(14分)(1)在某天然产物中得到一种有机物分子X,分子式为C10H14,经酸性高锰酸钾氧化后得到有机物A和B,A经高碘酸氧化后得到分子式为C2H4O2的酸和CO2。而B是二元羧酸,可由环戊二烯和乙烯经双烯加成的产物用酸性高锰酸钾氧化得到。请给出化合物A、B和X的结构简式(可用键线式表示)。
 提示:① ②
提示:① ②
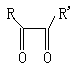 |
HIO4 H2O→RCOOH R’COOH HIO3
A B X
(2)A、B、C、D四种烃,摩尔质量之比是1:2:3:4,且它们的实验式都是C7H5,都只有3 种一硝基取代物。
写出A、B、C、D的结构简式(各写一例);
、 、 、
26.(10分)有机物A的分子式C3H7NO2S,无色晶体,溶于水,不溶于苯、二硫化碳等,可由毛发等蛋白质水解提纯制备。A有两性,等量的A消耗H 、OH-的物质的量比为1:2。A在中性或微碱性溶液中被空气氧化生成有机物B。B的分子式C6H12N2O4S2,白色片状晶体,易与酸、碱反应。结构测定:A中不同环境的H的5种,而B中只有4种。试回答:
(1)A、B的结构简式:A B
(2)A在中性或微碱性溶液中被空气氧化成B的化学方程式
(3)A与强碱反应的离子方程式
(4)A燃烧的化学方程式 .
六、计算题(12分)
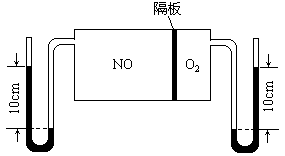
27.如图:V(NO):V(O2)==3:1。当抽去NO和O2之间的隔板后,NO和O2反应后成NO2,部分NO2聚合成N2O4(N2O4此时为气态)。当体系达到平衡后,U形毛细管两端汞面高度差由反应前10cm变为7.1cm。假设温度不变,且隔板及U形毛细管的体积都忽略不计,求此时混合气体的平均相对分子质量。
一、选择题(每小题4分,共40分。每小题只有一个正确答案)
1
2
3
4
5
6
7
8
9
10
A
C
A
C
D
C
A
C
B
C
二、选择题(每小题4分,共32分。每小题只有1~2个正确答案,若有两个正确选项,只选一个且正确的给2分,多选或错选都给0分)
11
12
13
14
15
16
17
18
D
A
A
A
D
BD
AD
AC
三、填空题(本题包括3小题,共20分)
19.(6分)CH3F(3分)2 CH3F 3O2——→2CO2 2H2O 2HF(3分)
20.(8分)H2O===H2O e-;e-(H2O)n(或ex(H2O)nx-);H2O H2O==H3O ·OH;(每个2分);酸性;强还原性;(每个1分)
![]() 21.(6分)A的化学式:NH4HC2O4;B的化学式:NH4HCO3;
21.(6分)A的化学式:NH4HC2O4;B的化学式:NH4HCO3;
C的结构简式:CO(NH2)2或
(化学式、结构简式每个2分)
四、简答题(本题包括3小题,共22分)
22.(8分)由“石灰氮是化肥”可知固体甲中含钙、氮元素,含碳量最高的气态烃必是C2H2,可知C是CaC2,甲中含氮元素质量分数35.00%,故甲是CaCN2。(以上推理过程不作要求)
(1)CaCO3 ![]() CaO CO2↑ CaO 3C===CaC2 CO↑ CaC2 N2==CaCN2 C
CaO CO2↑ CaO 3C===CaC2 CO↑ CaC2 N2==CaCN2 C
(2)CaCN2 3H2O===CaCO3↓ 2NH3↑ (反应式各2分)
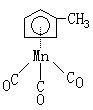 23.(8分)MMT的化学式为:C9H7O3Mn,结构简式为:
23.(8分)MMT的化学式为:C9H7O3Mn,结构简式为:
(化学式,结构简式各4分)
24.(6分)
首先亚甲基蓝被葡萄糖还原,还原后的无色物,又被空气中氧气氧化,又成为亚甲基蓝。反复作用。(答出氧化,还原各得3分)
五、(本题包括2小题,共24分)
25.(14分)
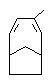
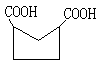
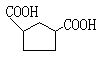
 (1)
(1)
, 或
 (2)
(2)
(每个结构2分)其它合理的答案同样给分)
26.(10分)(1)结构简式A: ![]() (半胱氨酸)
(半胱氨酸)
B:
(2)
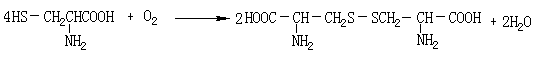 |
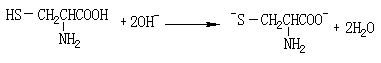
(3) 
(4) 
(结构、反应式每个2分)
六、计算题(12分)
27.设反应前NO为3 mol;O2为1 mol;NO2转化率为x
![]() 2NO O2=====2NO2 2NO2 N2O4
2NO O2=====2NO2 2NO2 N2O4
2 1 (2)平衡: 2-2x x
因为n平==n NO n NO2 n N2O4==(3-x)mol
所以T、V恒定时 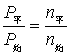 则
则 ![]() 所以x=0.16 (7分)
所以x=0.16 (7分)
所以 ![]()
![]() (5分)(答43.0同样正确)
(5分)(答43.0同样正确)
