| 高一第二学期期末测试题 |
|
一、选择题(本题包括10小题,每小题2分。每小题只有一个选项符合题意) 1.飘尘是物质燃烧时产生的( )粒状漂浮物,颗粒很小,不易沉降。漂尘在空气中与 A.氧化剂 B.还原剂 C.催化剂 D.吸附剂 2.下列物质不能使品红溶液褪色的是( ) A.硫化氢 B.二氧化硫 C.氯气 D.过氧化钠 3.下列物质露置于空气中,均会变质,其中不是因为发生氧化还原反应而变质的是( ) A.氢硫酸 B.烧碱溶液 C.亚硫酸钠 D.氯水 4.石墨炸弹爆炸时能在方圆几百米范围内撒下大量石墨纤维,造成输电线、电厂设备损坏,这是由于石墨( ) A.有放射性 B.易燃、易爆 C.能导电 D.有剧毒 5.关于非金属元素N、O、Cl、C的叙述,正确的是( ) A. 在通常状况下其单质均为气体 B. 其单质都是双原子分子 C. 都属于主族元素 D.每种元素仅生成一种氢化物 6.下列氧化物按其形成的含氧酸酸性递增顺序排列的是( ) A. C. 7.放在敞口容器中的下列溶液,久置后溶液中该溶质的浓度会变大的是( ) A.浓硫酸 B.氢氧化钠溶液 C.氯水 D.氯化钠溶液 8.下列各物质的用途(括号内为用途),错误的是( ) A.硅(半导体材料) B.二氧化硅(光导纤维) C.溴化银(感光材料) D.碳酸钡(医疗上“钡餐”) 9.下列说法中,不正确的是( ) A. 硫既可做氧化剂,又可做还原剂 B. C. 可以用铁罐贮运冷的浓 D.氢硫酸既有氧化性,又有还原性 10.医疗上使用放射性核素 A.19 B.53 C.72 D.125 二、选择题(本题包括15小题,每小题2分,共30分。每小题有1-2个选项符合题意) 11.元素的性质随原子序灵敏的递增,呈现周期性变化的原因是( ) A. 元素原子核外电子排布呈现周期性变化 B. 元素原子的电子层数呈现周期性变化 C. 元素的化合价呈现周期性变化 D.元素的原子半径呈现周期性变化 12.既有离子键,又有非极性共价键的化合物是( ) A. 13.下列各组性质比较中正确的是( ) A. 酸性: B. 碱性: C. 稳定性: D.还原性: 14.可用以判断铝的金属性活泼性比钠强的是( )。 A. 原子电子层数的多少 B. 原子在化学反应中失去电子的多少 C. 最高价氧化物水化物的碱性强弱 D.置换水或酸中氢的能力 15.元素 A. 16.某元素R的气态氢化物的化学式符合 A. 17.下列分子中所有原子都满足最外电子层8电子稳定结构的是( ) A. 18.在通常状况下,下列各组气体能共存,又都能用浓 A. C. 19.将木炭与浓 A. 烧碱溶液 B. 饱和 C. 足量 D.溴水 20.下列各组离子,能在溶液中大量共存的是( ) A. C. 21.已知反应: A. 此反应中,每生成 B. 生成物 C. 生成的 D.生成 22.下列叙述中正确的是( ) A. 阳离子一定是金属离子,阴离子一定只含非金属元素 B. 某金属元素的阳离子与某非金属元素的阴离子组成的物质一定是纯净物 C. 离子化合物都是强电解质,都易溶于水 D.阳离子的半径小于其原子的半径,阴离子的半径大于其原子的半径 23. A. B. C. D. 24.通常状况下,将 A.6mL B.12 mL C.15mL D.18mL 25.有一瓶无色气体,可能含有 ①原气体肯定有 A.①②③ B.①④⑤ C.①③⑥ D.①③⑤⑥ 三、填空题(本题包括3小题,共23分) 26.氢元素有H、D、T三种同位素,它们形成____________种氢分子,化学式分别为____________________。 27.物质的组成可用不同形式表示。 (1)将下列硅酸盐改写成氧化物形式(改写时金属氧化物在前,非金属氧化物在后, ①镁橄榄石( ②高岭石 (2)许多含氧酸及其盐均可改写成氧化物形式表示组成,试改写以下物质: 通过以上改写,可知 28.有原子序数均小于20的A、B、C、D四种元素,已知:①A和B在同一主族,C和D在同一周期;②四元素相互间可形成 与C的阴离子核外电子层结构相同;④ (1) 写出A和D两元素的名称:A_______、D_______;画出B离子和C离子的结构示意图______________,两种离子中,半径较小的是_______。 (2) 写出
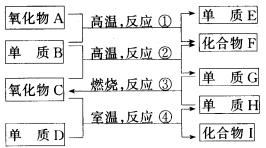
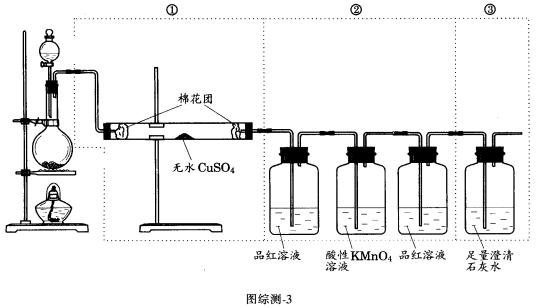
写出 四、推断题(本题包括2小题,共18分) 29.有物质A~I,它们之间的相互转化关系如下图所示。已知:①单质E可用为半导体材料;②化合物F是不能生成盐的氧化物;③化合物I能溶于水呈弱酸性,它能与氧化物A发生非氧化还原反应生成C和另一种化合物。 据此,请回答: (1) 化合物F是___________。 (2) 化合物I是___________。 (3) 反应③的化学方程式是___________。 反应④的化学方程式是___________。 30.图综测-3虚线框中的装置可用来检验浓 (1) 如果将装置中①、②、③三部分仪器的连接顺序变为②、①、③,则可以检出的物质是___________;不能检出的物质是___________。 (2) 如果将仪器的连接顺序变为①、③、②,则可以检出的物质是___________;不能检出的物质是___________。 (3) 如果将仪器的连接顺序变为②、③、①,则可检出的物质是___________;不能检出的物质是___________。 五、计算题(19分) 31.现有物质的量浓度为18.4mol/L的浓硫酸20.0mL,加入铜屑共热一段时间后,冷却,滤去多余的铜屑,将滤液加水到100.0mL,测得溶液中 第二学期期末测试题 一、(每小题2分,共20分) 1.C 2.A 3.B 4.C 5.C 6.B 7.D 8.D 9.B 10.A 二、(每小题2分,共30分) 11.A 12.C 13.AC 14.CD 15.AC 16.B 17.AC 18.CD 19.AD 20.D 21.B 22.D 23.CD 24.B 25.A 三、(共23分) 26.(4分) 6, 27.(7分)
28.(12分)
四、(18分) 29.(6分) (1)CO (2)HF 30.(12分) (1) (2) (3) 五、(9分)
|
教育最重要的是使人变得更聪明。教育就是要开启人的心智,使人身体好,更主动、积极,行动能力强,更能干。
中文域名: 古今中外.com
英文域名: www.1-123.com
丰富实用的教育教学资料