|
ЩшБОвГЮЊЪзвГЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
ЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁМгШыЪеВи |
|
| жаЮФгђУћ: ЙХНёжаЭт.comЁЁЁЁЁЁЁЁЁЁЁЁ
гЂЮФгђУћЃКwww.1-123.comЁЁЁЁЁЁЁЁЁЁЗсИЛЪЕгУЕФНЬг§НЬбЇзЪСЯ |
| |
| |
| |
|
|
ЖўЁЂЬюПеЬтЃЈ25ЁфЃЉ 21ЁЂ(4Ёф)(1) жмЦк зх (2) ЃЈИї1ЗжЃЉ (3) ЁЃ(2Зж) 22ЁЂ(14Ёф) ЃЈ1ЃЉЛЏбЇЪНЃКBЮЊ ЃЌFЮЊ ЁЃЃЈИї1ЗжЃЌЦфгрИї2ЗжЃЉ ЃЈ2ЃЉгУЕчзгЪНБэЪОDЕФаЮГЩЙ§ГЬЮЊЃК ЁЃ ЃЈ3ЃЉвбжЊHЕФУмЖШБШПеЦјДѓЃЌдђ = 1 \* GB3 ЂйжаЫљЩцМАЕФЗДгІЕФЛЏбЇЗНГЬЪНЮЊЃК ЃЛ ЁЃ ЃЈ4ЃЉаДГіFгызуСПYЗДгІЩњГЩJЕФРэгЩЃК ЃЈ5ЃЉаДГіAгыDШмвКЗДгІЩњГЩBЕФРызгЗНГЬЪНЃК ЁЃ аДГіAдквЛЖЈЬѕМўЯТгыЫЎЗДгІЕФЛЏбЇЗНГЬЪНЃК ЁЃ 23ЁЂ(4Ёф)ЃЈ1ЃЉМзШмвКЮЊЃК ЃЌввШмвКЮЊЃК ЁЃ ЃЈ2ЃЉЕЮМг45mLввШмвКЕФЙ§ГЬжаЗЂЩњЕФРызгЗНГЬЪНЮЊЃК ЁЃ ЃЈ3ЃЉввШмвКЕФЮяжЪЕФСПХЈЖШЮЊЃК ЁЃ 24ЁЂ(3Ёф)ШмвКжавЛЖЈКЌга РызгЃЌвЛЖЈВЛДцдк РызгЃЌ ПЩФмКЌга ЁЃ Ш§ЁЂЪЕбщЬтЃЈ14ЁфЃЉ 25ЁЂ(8Ёф)ЕкЖўВНЃК ; ЕкШ§ВНЃК ; ЕкЫФВНЃК ЁЃ ЃЈ3ЃЉбљЦЗжаКЌгаKClЁЄMgCl2ЁЄ6H2OЃЈЯрЖдЗжзгжЪСП277.5ЃЉЕФ жЪСПЗжЪ§БэДяЪНЃК ЁЃ 26ЁЂ(6Зж)ЃЈ1ЃЉдкЪдЙмЂёРяМгШыЕФЪдМСЪЧ ЁЃЃЈ1ЗжЃЉ ЃЈ2ЃЉдкЪдЙмЂђРяМгШыЕФЪдМСЪЧ ЁЃЃЈ1ЗжЃЉ ЃЈ3ЃЉЮЊСЫжЦЕУАзЩЋFe(OH)2ГСЕэЃЌдкЪдЙмЂёКЭЂђжаМгШыЪдМСЃЌДђПЊжЙЫЎМаЃЌШћНєШћзгКѓЕФЪЕбщВНжшЪЧ ЁЃ ЃЈ4ЃЉетбљЩњГЩЕФFe(OH)2ГСЕэФмНЯГЄЪБМфБЃГжАзЩЋЃЌЦфРэгЩЪЧ ЁЃ ЫФЁЂМЦЫуЬтЃЈ11ЗжЃЉ 27ЃЎЛЗБЃЛЏбЇжаЃЌCODЃЈChemical Oxygen DemandЃЉЪЧЖШСПЫЎжаЛЙдадЮлШОЮяЕФживЊжИБъЁЃВтЖЈCODЗНЗЈЪЧЃКгУЧПбѕЛЏМСЃЈШчKMnO4ЁЂNaClOЕШЃЉДІРэ1 LЫЎбљЃЌЕБЫЎжаЛЙдадЮлШОЮяЧЁКУБЛЭъШЋбѕЛЏЪБЃЌВтГіЯћКФЕФбѕЛЏМСЕФСПЁЃШЛКѓНЋДЫбѕЛЏМСЕФСПЭЈЙ§ЕчзгЕУЪЇЙиЯЕЃЌЛЛЫуГЩвдO2зїбѕЛЏМСЪБЫљашЕФO2ЕФжЪСПЃЈa mgЃЉЃЌИУЫЎбљЕФCODМДЮЊa mgЁЄLЃ1ЁЃЯжгаФГЗЯЫЎбљЦЗ50.00 mLЃЌМгШы0.0200 molЁЄLЃ1 KMnO4ШмвК10.00 mLЃЌВЂМгШыЪЪСПСђЫсКЭДпЛЏМСЃЌЗХШыЗаЫЎдЁжаМгШШвЛЖЮЪБМфЃЌГфЗжЗДгІКѓЃЌMnO4ЃБЛЛЙдЮЊMn2ЃЋЁЃгУ0.0200 molЁЄLЃ1 Na2C2O4БъзМвКЕЮЖЈЖргрЕФKMnO4ЃЌЯћКФNa2C2O4ШмвК5.00 mLЁЃЧѓИУЗЯЫЎбљЦЗЕФCODЁЃ ЃЈ2KMnO4ЃЋ5Na2C2O4ЃЋ8H2SO4ЃНK2SO4ЃЋ5Na2SO4ЃЋ10CO2ЁќЃЋ2MnSO4ЃЋ8H2OЃЉ 28ЃЎ2.80gЬњгы100mLЯЁЯѕЫсЛьКЭКѓГфЗжЗДгІЃЌВњЩњЕФЦјЬхЮЊNOЃЌЗДгІКѓЬњЁЂЯѕЫсОљЮоЪЃгрЁЃЯђЗДгІКѓЕФШмвКжаМгШы100mL 0.2 molЁЄLЃ1ЕФЕтЛЏМиШмвКЃЌЧЁКУНЋШмвКжаЕФFe3 ШЋВПЛЙдЃЌЧѓдЯѕЫсШмвКЕФЮяжЪЕФСПХЈЖШЁЃ ИпЖўФъМЖЦкФЉМьВтЛЏбЇЪдЬтВЮПМД№АИ
| ЬтКХ
| 1
| 2
| 3
| 4
| 5
| 6
| 7
| 8
| 9
| 10
| Д№АИ
| D
| A
| C
| D
| C
| B
| C
| A
| B
| B
| ЬтКХ
| 11
| 12
| 13
| 14
| 15
| 16
| 17
| 18
| 19
| 20
| Д№АИ
| D
| A
| D
| A
| D
| D
| D
| D
| B
| D |
21ЃЎЃЈ1ЃЉЮхжмЦк = 2 \* ROMAN IIAзхЃЈ2ЃЉЧПМю
ЃЈ3ЃЉШЁТШЛЏяШШмвКЃЌгУpHЪджНВтЖЈШмвКЕФЫсМюадЃЌЯдЪОжаадЃЌжЄЪЕЪЧЧПМюЁЃ
22ЃЎЃЈ1ЃЉBЃКH2 FЃКFeCl2
ЃЈ2ЃЉ ![]()
![]()
ЃЈ3ЃЉ2Na2O2 2H2O=4NaOH O2Ёќ FeCl3 3NaOH=Fe(OH)3Ё§ 3NaCl
(4) Na2O2ОпгабѕЛЏадЃЌЧвгыЫЎЗДгІЩњГЩМюЃЌЙЪFe2 дкДЫЬѕМўЯТПЩБЛбѕЛЏЩњГЩFe(OH)3
(5)Fe 2H =Fe2 H2Ёќ 3Fe 4H2O===Fe3O4 4H2Ёќ(ИпЮТ)
23ЃЎ(1)AlCl3 NaOH
(2)Al3 3OH- =Al(OH)3Ё§ Al(OH)3 OH-=AlO2- 2H2O
(3)0.16molЁЄL-1
24ЃЎSO42- Al3 Mg2 ЃЛCO32- Fe3 NH4 ЃЛNa
25ЃЎЕкЖўВНЃКМгШыAmLamol/LNaOHШмвК(Й§СП)ЃЌГфЗжЗДгІ
ЕкШ§ВНЃКжБНгдкЗДгІКѓЕФШмвКжаЕЮМгЗгЬЊжИЪОМС2ЁЋ3ЕЮ
ЕкЫФВНЃКгУcmol/LHClШмвКЕЮЖЈжСгЩЧГКьЩЋ жСЮоЩЋЃЌЯћКФHClШмвКCmL
KClЁЄMgCl2ЁЄ6H2O% 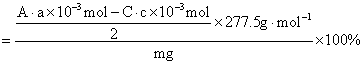
26ЃЎЃЈ1ЃЉЯЁ H2SO4 ЬњаМЃЈ2ЃЉNaOHШмвК
ЃЈ3ЃЉМьбщЪдЙмЂђГіПкДІХХГіЕФЧтЦјЕФДПЖШЁЃЕБХХГіЕФH2ДПОЛЪБЃЌдйМаНєжЙЫЎМаЁЃ
ЃЈ4ЃЉЪдЙмЂёжаЗДгІЩњГЩЕФH2ВМТњСЫЪдЙмЂёКЭЪдЙмЂђЃЌЧвЭтНчПеЦјВЛЧсвзНјШыЁЃ
27ЃЎ128mg/L
28ЃЎ1.6 molЁЄLЃ1 n(Fe)=2.8g/56gЁЄmol-1=0.05mol n[Fe(NO3)3]=n(I-)=0.1LЁС0.2 molЁЄLЃ1=0.02mol
ЙЪn[Fe(NO3)2]ЃНn(Fe)Ѓn[Fe(NO3)3]ЃН0.05molЃ0.02molЃН0.03mol
гЩЕУЪЇЕчзгЪиКуЃК3n[Fe(NO3)3]ЃЋ2n[Fe(NO3)2]ЃНn(NO)ЁС3
3ЁС0.02molЃЋ2ЁС0.03molЃНn(NO)ЁС3 n(NO)ЃН0.04mol
гЩЕЊдзгЪиКуЃКn(HNO3)= n(NO) 3n[Fe(NO3)3] 2n[Fe(NO3)2]=0.16mol
c(HNO3)= 0.16mol/0.1L=1.6 molЁЄLЃ1
РДдДЃКжаЙњемЪПЭј
НЬЪІбЇЩњМвГЄ ЛЏИпЖўЩЯФЉзЪСЯ БИПЮПМЪдНЬбЇ
НЬг§зЪСЯ [зщЭМ]ЕквЛбЇЦкИпЖўФъМЖЦкФЉМьВтЛЏбЇЪдЬт ЮФеТ
| |
| |
| |
| 2004-2010ЁЁ жаЙњемЪПЭјАцШЈЫљгаЁЁв§гУБОеОФкШнЧыжИУїРДдДЁЁ ИјБОеОЭЖИхЁЁ ЁЁБИАИађКХ ЪёICPБИ05009253КХЁЁ
|