|
ЩшБОвГЮЊЪзвГЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
ЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁМгШыЪеВи |
|
| жаЮФгђУћ: ЙХНёжаЭт.comЁЁЁЁЁЁЁЁЁЁЁЁ
гЂЮФгђУћЃКwww.1-123.comЁЁЁЁЁЁЁЁЁЁЗсИЛЪЕгУЕФНЬг§НЬбЇзЪСЯ |
| |
| |
| |
|
|
15.ФГЬхЛ§ПЩБфЕФУмБеШнЦї,ЪЂгаЪЪСПЕФAКЭBЕФЛьКЯЦјЬх,дквЛЖЈЬѕМўЯТЗЂЩњЗДгІ:A 3B ЂйдЛьКЭЦјЬхЕФЬхЛ§ЮЊ1.2VЩ§ ЂкдЛьКЭЦјЬхЕФЬхЛ§ЮЊ1.1VЩ§; ЂлДяЦНКтЪБЦјЬхAЯћКФЕє0.05VЩ§; ЂмДяЦНКтЪБЦјЬхBЯћКФЕє0.05VЩ§; 16.дквЛИіЙЬЖЈЬхЛ§ЕФУмБеШнЦїжаЃЌ2molAКЭ1molBЗЂЩњЗДгІ2A(g) B (g) A.3molC 1molB B.1molA 0.5molB 1.5molC 0.5molD C.4molA 2molB D.3molC 1molD 2molA 1molB
бЁдёЬтД№АИ(ЙВ48Зж)
ЕкIIОэЃЈЙВ52ЗжЃЉ 17ЃЎЃЈ9ЗжЃЉ IЃЎПЩФцЗДгІA(g) 2B(g) ИФ
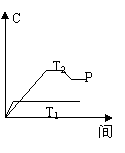 БфЬѕМўЃЌНЋБфЛЏНсЙћ(ЬюЁАдіДѓЁБЁЂЁАМѕаЁЁБЛђЁАВЛБфЁБ)ЃЌЬюШыПеИёЁЃ БфЬѕМўЃЌНЋБфЛЏНсЙћ(ЬюЁАдіДѓЁБЁЂЁАМѕаЁЁБЛђЁАВЛБфЁБ)ЃЌЬюШыПеИёЁЃ
ЃЈ1ЃЉЩ§ИпЮТЖШЃЌBзЊЛЏТЪ ЃЌ ЃЈ2ЃЉБЃГжЮТЖШКЭбЙЧПВЛБфЃЌМгШыЯЁгаЦјЬхЃЌдђCЕФЮяжЪЕФСП ЁЃ ЃЈ3ЃЉБЃГжЮТЖШКЭЬхЛ§ВЛБфЃЌдйМгШыЯЁгаЦјЬхЃЌAЕФзЊЛЏТЪ ЁЃ IIЃЎ.дквЛЖЈЬѕМўЯТЃЌПЩФцЗДгІA B ЂХЮТЖШT1 T2ЃЈЬюЁАДѓгкЁБЁЂЁАЕШгкЁБЛђЁАаЁгкЁБЃЉ ЂЦе§ЗДгІЪЧ ЗДгІЃЈЬюЁАЮќШШЁБЛђЁАЗХШШЁБЃЉ ЂЧМйШчAЁЂBЁЂCОљЮЊЦјЬхЃЌдђm 2ЃЈЬюЁАДѓгкЁБЁЂЁАЕШгкЁБЛђЁАаЁгкЁБЃЉ
18ЃЎЃЈ11ЗжЃЉгвЭМЪЧФГЛЏбЇАЎКУаЁзщЭЌбЇЩшМЦЕФбаОПЭКЭЯЁЯѕЫсЗДгІЫйТЪ[Ід(NO)]ЕФЪЕбщзАжУЭМЁЃЪдЛиД№ЯТСаЮЪЬтЃКЂХаДГіЭКЭЯЁЯѕЫсЗДгІЕФЛЏбЇЗНГЬЪН_____________________________ ЁЃ ЂЦЮЊВтЖЈЭКЭЯЁЯѕЫсЗДгІЫйТЪ[Ід(NO)]ЃЌБОЪЕбщашвЊМЧТМЕФЪЕбщЪ§ОнЮЊЃК________ ЁЂ________ ЂЧЪЕбщЧАдѕбљМьбщзАжУЕФЦјУмад __________________________________
ЂШЮЊБЃжЄЪЕбщЕФГЩЙІЃЌМгШывЛЖЈСПЯЁЯѕЫсЪЧКмживЊЕФВйзїЃЌФуШЯЮЊгІдѕбљВйзїЃП
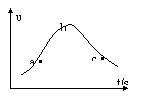 ____________________________ЃЌКѓНЋЭфЧњЕФЭЫПбИЫйЩьШыШмвКВЂПЊЪМ____________________________ЁЃ ____________________________ЃЌКѓНЋЭфЧњЕФЭЫПбИЫйЩьШыШмвКВЂПЊЪМ____________________________ЁЃ
ЂЩИУАЎКУаЁзщЭЌбЇЖдЪЕбщЪ§ОнНјааДІРэКѓЕУЕНгУNOБэЪОЭКЭЯЁЯѕЫсЕФЗДгІЫйТЪКЭЪБМфЕФЙиЯЕЭМШчЯТЭМЫљЪОЁЃдђЃК ЂйaЁњb.Ід(NO)БфЛЏЕФжївЊдвђЪЧ________________________ ЂкbЁњc.Ід(NO)БфЛЏЕФжївЊдвђЪЧ_________________________ ЁЃ 19. ЃЈ10ЗжЃЉЯТЭМжаЕФУПвЛИіЗНИёжаЕФзжФИБэЪОгаЙиЕФвЛжжЗДгІЮяЛђЩњГЩЮяЃЌЦфжаAЁЂCЮЊЮоЩЋЦјЬхЃЌCФмЪЙЪЊШѓЕФКьЩЋЪЏШяЪджНБфРЖЁЃвбжЊXВЛгыТШЛЏБЕЗДгІЃЌЧыЬюаДЯТСаПеАзЃК ЂХЛЏбЇЪНЃКX ЃЌC ЃЌ
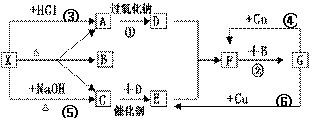 F ЃЌG ЁЃ F ЃЌG ЁЃ
ЂЦЗДгІЂмЕФРызгЗНГЬЪНЪЧЃК ЃЛ ЂЧCКЭDЗДгІЕФЛЏбЇЗНГЬЪНЃК
ЂШЗДгІЂнЕФЛЏбЇЗНГЬЪН
ЧыЛиД№ЃК(1)ШєЦ№ЪМЗДгІДгФцЗДгІПЊЪМДяЕНЯрЭЌЕФЦНКтзДЬЌЪБЃЌQЕФзЊЛЏТЪЮЊ___________ЁЃ ЃЈ2ШєЦ№ЪМЪБЗДгІЯђФцЗДгІЗНЯђНјааЃЌдђQЕФГѕЪМЮяжЪЕФСПn(Q) ЕФШЁжЕЗЖЮЇЪЧ_______
(2)ШєгыЩЯЪіЦНКтБЃГжЭЌЮТЃЌгквЛУмБеШнЦїжаГфШыXЃЈЦјЃЉКЭYЃЈЦјЃЉЕФЮяжЪЕФСПЗжБ№МЧЮЊaЁЂbЃЌЦНКтЪБZЕФЬхЛ§ЗжЪ§вВЧЁКУЮЊ0.4ЁЃШєКугаm< 22.ЃЈ8ЗжЃЉЭгывЛЖЈХЈЖШHNO3ЗДгІЪБЃЌЗНГЬЪНПЩБэЪОЮЊЃК Cu HNO3ЈDCu(NO3)2 NO2 NO H2OЃЈЮДХфЦНЃЉ ЃЈ1ЃЉИУЗДгІжаHNO3БэЯжЕФаджЪЪЧ_____________________, ЛЙдВњЮяЪЧ______________ ЃЈ2ЃЉ0.3molCuБЛЭъШЋШмНтКѓЃЌЪЇШЅЕФЕчзгЪ§ЪЧ__________ЃЈгУКЌNAБэЪОЃЉ; ШєЕУЕНNO2КЭNOЕФЮяжЪЕФСПЯрЭЌЃЌдђВЮМгЗДгІЕФHNO3ЮяжЪЕФСПЮЊ____________ ШєгУХХЫЎЗЈЪеМЏетаЉЦјЬхЃЌПЩЕУЕНБъзМзДПіЯТЕФЦјЬхЬхЛ§ЮЊ____________ ЃЈ3ШєВЮМгЗДгІЕФCuЃЌHNO3ЮяжЪЕФСПжЎБШЪЧ5ЃК14ЃЌаДГіВЂХфЦНИУЗДгІЕФРызгЗНГЬЪН ____________________________________________________________________
ЕкШ§бЇЦкЛЏбЇАыЦкЪдЬтД№АИ
17ЃЈ9ЗжЃЉI.(1) МѕаЁ. діДѓ (2) МѕаЁ (3) ВЛБф IIЃЎЂХДѓгкЁЁЃЈ2ЃЉЗХШШЁЁЃЈ3ЃЉДѓгкЁЁЃЈ4ЃЉдіДѓ ВЛ 18ЃЈ11ЗжЃЉЂХ3Cu 8HNO3 == 3Cu(NO3)2 2NOЁќ 4H2OЃЈ2ЗжЃЉ ЂЦNOЕФЬхЛ§ЁЂЗДгІЪБМфЃЈИї1ЗжЃЉ ЂЧЙиБеЗжвКТЉЖЗИЧbКЭЛюШћaЃЌДгUЙмГЄЙмДІМгЫЎжСUЙмГЄЙмжавКУцИпгкЖЬЙмжавКУцЃЌЙ§вЛЛсЃЌШєвКУцВюБЃГжВЛБфЃЌдђзАжУЦјУмадСМКУЁЃЃЈ2ЗжЃЉ ЂШДђПЊЗжвКТЉЖЗИЧbКЭЛюШћaЃЌДгUЙмгвЖЫзЂШыЯЁHNO3жСХХОЁUЙмзѓЖЫПеЦјЃЌЙиБеЛюШћaЃЛЃЈ2ЗжЃЉ МЧТМЪБМфЃЛЃЈ1ЗжЃЉ ЂЩЂйЭКЭЯЁЯѕЫсЗДгІЪЧЗХШШЗДгІЃЌЬхЯЕЮТЖШЩ§ИпЃЌЗДгІЫйТЪМгПьЁЃЃЈ1ЗжЃЉ ЂкЗДгІНјаавЛЖЮЪБМфКѓЃЌЬхЯЕгыЛЗОГЕФЮТВюДѓЃЌЩЂШШМгПьЃЌЬхЯЕЮТЖШБфЛЏВЛДѓЩѕжСгаЫљЯТНЕЃЌc(HNO3)НЕЕЭЃЌЗДгІЫйТЪНЕЕЭЁЃЃЈ1ЗжЃЉ 19ЃЈ10ЗжЃЉЂХ NH4HCO3 ЁЂNH3 ЁЂNO2 ЁЂHNO3ЃЈИї1ЗжЃЉ ЂЦCu 4H NO3-ЃЈХЈЃЉ===Cu2 2NO2 Ёќ 2H2OЃЈ2ЗжЃЉ ЂЧ4 NH3 5 O2 ЂШNH4HCO3 2NaOH 20ЃЈ6ЗжЃЉЂХ20% ЂЦ0.8<n(Q)Ём1 21ЃЈ8ЗжЃЉЂХ 0.4 5/3L ЂЦ m= 0.5 n= 5 22ЃЈ8ЗжЃЉ(1)ЫсадЃЌбѕЛЏадЃЛNO2КЭNO ЂЦ0.6NA, 0.9mol, 4.48L(ЮоЕЅЮЛЮЊИјЗж) ЂЧ 5Cu 14H 4NO3-=5Cu2 NO2Ёќ 3NOЁќ 7H2O(ИУПе3Зж,ЦфЫќИї1Зж) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
РДдДЃКжаЙњемЪПЭј НЬЪІбЇЩњМвГЄ ЛЏИпЖўЩЯФЉзЪСЯ БИПЮПМЪдНЬбЇ НЬг§зЪСЯ [зщЭМ]ИпжаЛЏбЇЕкШ§бЇЦкАыЦкЪдЬт ЮФеТ |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |
| |
| |
| 2004-2010ЁЁ жаЙњемЪПЭјАцШЈЫљгаЁЁв§гУБОеОФкШнЧыжИУїРДдДЁЁ ИјБОеОЭЖИхЁЁ ЁЁБИАИађКХ ЪёICPБИ05009253КХЁЁ
|