可能用到的相对原子质量:H—1 C—12 N—14 O—16 Na—23 Al—27 Fe—56
一.选择题(每小题只有一个选项符合题意。每小题2分,共50分)
1.SO2是大气主要污染物之一。造成大气中SO2含量急剧增加的主要原因是
A. 实验室逸出的SO2 B. 火山爆发产生的SO2
C. 燃烧煤和石油产生的SO2 D. 硫酸厂排放废气中的SO2
2.下列有机物中,属于烃的衍生物的是
A.C2H6 B. C2H2 C. C6H6 D. C2H4O
3.下列各组物质中,互为同位素的是
A. ![]() 和
和 ![]()
![]() B. O2和O3 C. H2O和H2O2 D. CO和CO2
B. O2和O3 C. H2O和H2O2 D. CO和CO2
4.某陨石中含有镁的一种放射性同位素 ![]() ,
, ![]() 原子核内的中子数是
原子核内的中子数是
A. 12 B. 16 C. 28 D. 40
5.下列物质易溶于水的是
A. 苯 B. 甲烷 C. 油脂 D. 葡萄糖
6.下列气体中,有颜色的是
A. HCl B. CO2 C. NO2 D. NH3
7.下列仪器中,能用于加热的是
A. 烧杯 B. 量筒 C. 容量瓶 D. 分液漏斗
8.用于居室装修的某些材料会不同程度地释放出某种无色、有刺激性气味的有害气体,该气体是
A. 甲烷 B. 甲醛 C. 氮气 D. 二氧化碳
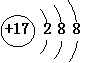
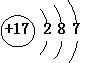
9.下列粒子的结构示意图中,表示阳离子的是
|
17 |
|
2 |
|
8 |
|
8 |
|
17 |
|
2 |
|
8 |
|
7 |
|
11 |
|
2 |
|
8 |
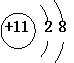
|
10 |
|
2 |
|
8 |
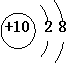
A. B. C. D.
10.下列材料中,不属于通常所说的三大合成材料的是
A. 塑料 B. 合金 C.合成纤维 D.合成橡胶
11.下列元素中,金属性最强的是
A.钾 B. 钠 C. 镁 D. 铝
12.有机物 ![]() 的名称是
的名称是
A.2-甲基丙烷 B. 2-甲基丁烷
C. 三甲基甲烷 D. 1,1-二甲基乙烷
13.某主族元素的原子,核外有四个电子层,最外层有7个电子,下列关于此元素的说法中正确的是
A.其单质的氧化性比Cl2强 B.其氢化物的稳定性比HCl强
C.其原子半径比氯的原子半径大 D.其简单阴离子的还原性比Cl—弱
14.下列各组物质中,互为同分异构体的是
A.CH2=CHCH3 和CH2=CHCH2CH3 B.CH2=CHCH2CH3和CH3CH=CHCH3 C.CH3CH2CH2CH3 和CH3CH=CHCH3 D.CH≡CCH2CH3 和CH2=CHCH2CH3
15.下列物质中,属于弱电解质的是
A.H2O B.NaCl C.NaOH D.H2SO4
16.下列物质中,酸性最强的是
A. H4SiO4 B. H3PO4 C. H2SO4 D. HClO4
17.下列电子式中,书写正确的是
![]()
18.下列物质中,只含离子键的是
A.N2 B.HCl C.NaCl D.KOH
19.下列物质中,溶于水后可生成两种酸的是
A. Cl2 B. HCl C. SO2 D. CO2
20.下列关于纤维素的说法中,不正确的是
A. 纤维素没有甜味 B. 纤维素易溶于水
C. 纤维素可用于造纸 D. 纤维素水解的最终产物为葡萄糖
21.下列有关物质用途的说法中,正确的是
①臭氧可用于漂白和消毒 ②碳酸氢钠可用于治疗胃酸过多
③二氧化硅可用于制作光导纤维 ④苯酚的水溶液具有杀菌防腐性能
A . 只有①② B. 只有②③ C. 只有①②③ D. 全部正确
22.在一定条件下,对于密闭容器中进行的可逆反应:
2HI (g) SHAPE \* MERGEFORMAT ![]()
![]() H2 (g) I2 (g),下列说法中可以充分说明这一反应已经达到化学平衡状态的是
H2 (g) I2 (g),下列说法中可以充分说明这一反应已经达到化学平衡状态的是
A.HI、H2 、I2的浓度相等
B. HI、H2 、I2的浓度不再发生变化
C.HI、H2 、I2在密闭容器中共存
D. 反应停止,正、逆反应速率都等于零
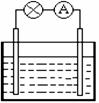 23.对于铜-锌原电池,以下说法不正确的是
23.对于铜-锌原电池,以下说法不正确的是
A.铜为正极
B. 锌片上发生氧化反应
C. 它是一种把化学能转化为电能的装置
D. 铜片向外电路提供电子,锌片从外电路得到电子
24. 下列离子方程式中,书写正确的是
A. HCO3- + H2O === H2CO3 + OH-
B. CO32- + 2H2O === H2CO3 + 2OH-
C. Fe3 + 3H2O SHAPE \* MERGEFORMAT ![]()
![]() Fe(OH)3 + 3H
Fe(OH)3 + 3H
D. NH4 + H2O SHAPE \* MERGEFORMAT ![]()
![]() NH3·H2O + OH-
NH3·H2O + OH-
25. 某有机物与氧气反应的产物是CH3CH2CHO, 原有机物是
A. 乙醇的同系物 B. 乙醛的同系物
C. 丙醇的同分异构体 D. 丙醛的同分异构体
二、填空题(共 分)
1.(3分)工业上可用碳在高温下还原二氧化硅的方法制取少量粗硅:SiO2 2C ![]() Si 2CO↑。在该反应中,作为氧化剂的物质是 (填化学式),作为还原剂的物质是 (填化学式);若反应中生成了1 mol Si,则需消耗 mol SiO2。
Si 2CO↑。在该反应中,作为氧化剂的物质是 (填化学式),作为还原剂的物质是 (填化学式);若反应中生成了1 mol Si,则需消耗 mol SiO2。
2.(3分)在①乙醇、②乙醛、③乙酸三种物质中,具有酸性的是 (填序号,下同),能发生银镜反应的是 ,可在医疗上用作消毒剂的是 。
3.(4分)某无色溶液由①K 、②Cl-、③Al3 、④SO42-中的若干种离子组成。取部分该溶液,分装在四支试管中,分别进行实验:
(1)进行焰色反应,透过蓝色钴玻璃观察火焰呈紫色,说明一定含有的离子是 (填序号,下同)。
(2)滴加氢氧化钠溶液,产生白色沉淀,继续滴加,白色沉淀逐渐消失,说明一定含有的离子是 。
(3)加入少量稀硝酸使溶液酸化,再加入硝酸钡溶液,无白色沉淀产生,说明不含有的离子是 。
(4)加入少量稀硝酸使溶液酸化,再加入硝酸银溶液,产生白色沉淀,说明一定含有的离子是 。
4.(4分)钠、铝和铁是三种重要的金属。请回答:
(1)三种金属中,常温下遇浓硫酸或浓硝酸不会发生钝化现象的是 (填化学式);既能与酸反应,又能与碱反应的是 (填化学式)。
(2)三种金属在一定条件下均能与水发生反应。其中铁与水蒸气在高温下反应的化学方程式为 ;钠与水反应时可观察到的实验现象有 (填字母)。
a.钠浮在水面上 b.钠熔成小球 c.钠四处游动 d. 溶液变为红色
5.(8分)现有原子序数依次增大的X、Y、Z、W四种短周期元素。X与W同主族。Y与Z同周期且位置相邻,其单质在常温下均为无色气体。W的质子数等于Y与Z两原子的最外层电子数之和。
已知Z与W可形成离子化合物W2Z2 ,X与Y可形成阳离子YX4 ,X、Y、Z可形成化合物XYZ3。请回答:
(1)W在元素周期表中的位置为 。
(2)W2Z2与水反应的离子方程式为 。
(3)实验室中检验YX4 的操作方法及有关实验现象是:
取少量含YX4 的溶液,
,则证实溶液中含有YX4 。
(4)XYZ3在一定条件下易发生分解反应,若反应中转移电子数为9.03×1022,则有 mol XYZ3发生分解。
三、实验题(共分)
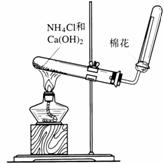 |
6.(4分)右图是实验室制取氨气的装置图。请回答:
(1)实验室制取氨气的化学方程式为
。
(2)因为氨气的密度比空气的
(填“大” 或“小”),所以收集氨气的方法
是 (填序号)。
① 向上排空气法 ② 向下排空气法
(3)干燥氨气可选用的试剂是
(填序号)。
① 碱石灰 ② 浓硫酸
7.(8分)利用右图装置,选用适当试剂,可完成实验(1)和(2),并得出相应的实验结论(见下表)。
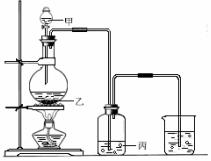
请填写表中的空格(从A~H中选择,填字母):
实验
所 用 试 剂
实验结论
甲
乙
丙
(1)
浓盐酸
KI淀粉
溶液
(2)
Cu
SO2具有
漂白性
A.浓硫酸 B.品红溶液 C.NaCl粉末
D.MnO2粉末 E.澄清石灰水 F.NaOH溶液
G.氧化性:Cl2 >I2 H.浓硫酸具有氧化性
8.(8分)实验室制取乙烯时,常伴有少量SO2等杂质气体生成。现利用下图所示装置制取较纯净的乙烯,并检验乙烯的化学性质。
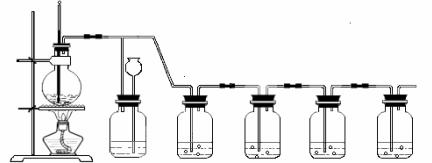
请回答:
(1)实验室制取乙烯的化学方程式为 。
(2)装置B可检验后续装置中是否发生堵塞。若发生堵塞,则B中的现象为 。
(3)装置C、D中所盛试剂的作用依次是 。
(4)根据装置E中的实验现象,可以说明乙烯是否具有不饱和性。下列反应能说明乙烯具有不饱和性的是 (填序号)。
①水解反应 ②加成反应 ③加聚反应 ④消去反应 ⑤酯化反应
四、计算题(共 分)
9.(4分)将标准状况下11.2 L NH3与足量的HNO3溶液充分反应。试计算:
(1)生成NH4NO3的物质的量为多少?
(2)生成NH4NO3的质量为多少?
10.(4分)Fe和Al是两种重要的金属,将它们按一定的质量比组成混合物。
(1)取一定质量的该混合物,若加入足量的NaOH溶液,生成的气体在标准状况下体积为n L;若加入足量的稀硫酸,生成的气体在标准状况下体积为m L。则原混合物中Fe的物质的量为 mol(用含n、m的代数式表示)。
(2)取一定质量的该混合物,在纯氧中充分燃烧。向所得产物中加入过量的NaOH溶液,充分反应后将不溶物过滤、洗涤、干燥后称量,测得该不溶物的质量与原混合物的质量恰好相等。则原混合物中Fe与Al的质量比为 。
答案:
题号
1
2
3
4
5
6
7
8
9
10
答案
C
D
A
B
D
C
A
B
C
B
题号
11
12
13
14
15
16
17
18
19
20
答案
A
A
C
B
A
D
B
C
A
B
题号
21
22
23
24
25
答案
D
B
D
C
A
一、填空题(共22分)
1.(3分) SiO2 ………………………………………………1分
C …… …………………………………1分
1 …………… ………………………1分
2.(3分) ③ ……………………………………………………………1分
② ……………… ……………………………1分
① ……………………………………………1分
3.(4分) (1) ① ………………………………………………………1分
(2) ③ ………………………………………………………1分
(3) ④ ………………………………………………………1分
(4) ② …………………………………………………1分
4.(4分) (1)Na …………………………………………………… 1分
Al ………………………………………1分
(2)3Fe 4H2O(g) ![]() Fe3O4 4H2 ……………1分
Fe3O4 4H2 ……………1分
a b c ………………………………………………… 1分
5.(8分)(1)第三周期IA族 ……………………………………………2分
(2)2Na2O2 2H2O == 4Na 4OH- O2↑ … ………2分
(3)加入氢氧化钠溶液并加热,产生能使湿润的红色石蕊试纸变蓝的气体 2分
(4)0.15 ……………………………………………2分
二、实验题(共20分)
6.(4分)(1)Ca(OH)2 2NH4Cl ![]() CaCl2 2NH3↑ 2H2O 1分
CaCl2 2NH3↑ 2H2O 1分
(2) 小 ………………………………………………………1分
② ……………………………………………………1分
(3) ① ……………………………………………………1分
7.(8分)
实验
所 用 试 剂
实验结论
甲
乙
丙
(1)
D
(2分)
G
(2分)
(2)
A
(2分)
B
(2分)
8.(8分)(1)CH3CH2OH ![]() CH2=CH2↑+H2O ………2分
CH2=CH2↑+H2O ………2分
(2)集气瓶中水面下降,长颈漏斗中水面上升 ………2分
(3)除去SO2等杂质气体,检验SO2是否除净 ………………2分
(4)② ③ ……………… ……………………………2分
三、计算题(共8分)
9.(4分)(1) 解: HNO3 NH3 === NH4NO3 ……1分
22.4 L 1 mol
11.2 L n (NH4NO3) ………1分
n (NH4NO3) = ![]() ……………1分
……………1分
(2)m (NH4NO3) = 0.5 mol×80 g / mol = 40 g …………1分
答:(略)
10.(4分)(1) ![]() ……………………………2分
……………………………2分
(2)21∶8 …………………………………………2分
