高一化学晚练习题
可能用到的相对原子质量:H—1 C—12 N—14 O—16 Na—23 Mg—24 Al—27 P—31 S—32 Cl—35.5 Fe—56 Cu—64
一、选择题(每小题4分,有1~2个选项符合题意)
1. 为了除去镀在铝表面的铜镀层,可选用的试剂是
A. 浓硫酸 B. 稀硝酸 C. 浓盐酸 D. 浓硝酸
2. 通常状况下,下列各组物质可以共存并能用浓硫酸干燥的是
A. ![]() B.
B. ![]()
C. ![]() D.
D. ![]()
3. 制备干燥氨气所需的药品是
A. ![]() 溶液、
溶液、 ![]() 溶液、碱石灰
溶液、碱石灰
B. ![]() 固体、碱石灰、消石灰
固体、碱石灰、消石灰
C. ![]() 溶液、
溶液、 ![]() 固体、浓
固体、浓 ![]()
D. 饱和氨水
4. NO是危害极大的气体,下列的几种作用是由NO造成的是:(1)破坏臭氧层(2)造成酸雨(3)与人体血红蛋白结合
A. 只有(3) B. 只有(1)(2) C. 只有(2)(3) D. 全部
5. 在反应 ![]() 中,氧化产物与还原产物的物质的量之比为
中,氧化产物与还原产物的物质的量之比为
A. 5:3 B. 3:5 C. 1:1 D. 2:1
6. 锌和稀硝酸反应时,若两者以2:5的物质的量之比恰好完全反应时,则还原产物可能是
A. NO B. ![]() C.
C. ![]() D.
D. ![]()
7. 将含有等体积 ![]() 的混合气体依次通过盛有
的混合气体依次通过盛有 ![]() 和
和 ![]() 溶液的装置充分反应后,最后得到的气体是
溶液的装置充分反应后,最后得到的气体是
A. ![]() B.
B. ![]()
C. ![]() D.
D. ![]()
8. 将a g铜片投入到足量一定浓度的硝酸溶液中,反应消耗的 ![]() 为b g,若
为b g,若 ![]() ,则反应中起酸性作用的硝酸的质量为
,则反应中起酸性作用的硝酸的质量为
A. ![]() B.
B. ![]() C.
C. ![]() D.
D. ![]()
9. 氮化钠 ![]() 是离子化合物,它与水反应可产生氨气。试判定下列说法中正确的是
是离子化合物,它与水反应可产生氨气。试判定下列说法中正确的是
A. 在 ![]() 与水的反应中,
与水的反应中, ![]() 作还原剂
作还原剂
B. ![]() 与
与 ![]() 离子的电子层结构都与氩原子结构相同
离子的电子层结构都与氩原子结构相同
C. 在 ![]() 的固体中,
的固体中, ![]() 半径大于
半径大于 ![]() 半径
半径
D. ![]() 与盐酸反应时可生成两种盐
与盐酸反应时可生成两种盐
10. 在相同状况下,容积相同的三支试管中分别盛满氨气、氯化氢和二氧化氮,将三支试管倒立于水中,充分溶解后,试管内溶液的物质的量浓度之比为(假设试管内溶液未扩散到水槽中)
A. 3:3:2 B. 1:1:1 C. 2:2:1 D. 2:2:3
11. 有甲、乙、丙三种气体,甲无色,一定条件下,甲能与氧气反应生成乙;乙不溶于水,但能与氧气进一步反应生成丙;甲、丙皆溶于水,但其水溶液酸碱性恰好相反,则
A. 甲: ![]() 乙:
乙: ![]() B. 甲:
B. 甲: ![]() 乙:
乙: ![]()
C. 甲: ![]() 丙:
丙: ![]() D. 甲:
D. 甲: ![]() 乙:
乙: ![]()
12. 某温度下,在体积一定的密闭容器中适量的 ![]() (气)和
(气)和 ![]() (气)恰好完全反应,若反应产物中只有
(气)恰好完全反应,若反应产物中只有 ![]() (气)和
(气)和 ![]() (固),则反应前后容器中压强比应接近于
(固),则反应前后容器中压强比应接近于
A. 7:11 B. 11:7 C. 11:1 D. 1:11
13. 浓硝酸往往显黄色是因为
A. 溶有溴在其中 B. 其中含有 ![]()
C. 溶有硫黄在其中 D. 溶有自身分解的 ![]()
14. 在强酸性溶液中,可以大量共存的离子组是
A. ![]() B.
B. ![]()
C. ![]() D.
D. ![]()
15. 在某100mL混合酸中, ![]() 物质的量浓度为0.4mol/L,
物质的量浓度为0.4mol/L, ![]() 的浓度为
的浓度为 ![]() 。向其中加入2.56g铜粉,微热,待充分反应后,溶液中
。向其中加入2.56g铜粉,微热,待充分反应后,溶液中 ![]() 物质的量浓度约为
物质的量浓度约为
A. ![]() B.
B. ![]()
C. ![]() D. 无法计算
D. 无法计算
班级______ 姓名__________ 座号_____ 成绩_______
选择题答题卡
|
题号 |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
|
答案 |
||||||||
|
题号 |
9 |
10 |
11 |
12 |
13 |
14 |
15 |
|
|
答案 |
二、填空题(每空2分,共30分)
16. 已知A、B、C、D、E都是含氮元素的化合物,有下列几个反应(未配平):
① A + O2 → C ② C + H2O → A + B
③ D + O2 → A + H2O ④ B + D → E
写出上述五种化合物的分子式:A是 ,B是 ,
C是 ,D是 , E是 。
17. 用实验确定两种氮肥混合物的组成
(1)取少量样品跟消石灰共热,放出使湿润的红色石蕊试纸变蓝的气体。这种气体是_____________。证实化肥中含有____________离子。
(2)把上述反应后所得固体投入盐酸,产生无色无味气体。这种气体通过澄清石灰水,溶液出现浑浊现象。此气体是______________,证实化肥中含有____________离子或________离子。
(3)另取少量试样溶于水,加入氯化镁溶液后无明显变化,可知化肥中一定含有_____________离子,而排除___________离子。
(4)向试样的水溶液中加入用盐酸酸化的氯化钡溶液,立即产生白色沉淀,可知化肥中含有_______________离子。
以上事实说明,两种化肥是_____________和_____________。
三、计算题(10分)
18. 3.84g铜粉和一定量的浓硝酸反应,随着铜的不断减少,反应生成的气体颜色也逐渐变浅。当铜全部反应时,共收集到标准状况下的气体2.24L,求反应中消耗的硝酸的物质的量是多少?
【附加题】
1. 将一定量的铜制成硝酸铜有三种途径:① 将铜直接溶于浓硝酸,其反应的离子方程式是 ;② 将铜直接溶于稀硝酸,其反应的离子方程式是 ;③ 将铜先在空气中完全氧化,其反应的化学方程式是 , 然后再将产物溶于稀硝酸中,其反应的离子方程式是 。
试问第 种方法最好且耗酸量最少。
2.图1-1装置是某种气体X的发生装置和收集装置(必要时可加热)。所用的试剂从下列试剂中选取2~3种,硫化亚铁、二氧化锰、铜屑、氯化铵、稀硝酸、浓盐酸、蒸馏水。
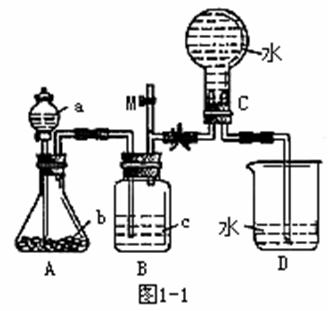
请回答下列问题。
(1)气体X的化学式是______。
(2)所选药品a中是_____,b是_____,装置B的作用是_______。
(3)用所选的药品制X时离子方程式是______。
(4)在反应刚开始时A中的主要现象是______。
(5)开关M的作用_____。
试题答案
1. D 2. D 3. B 4. D 5. A
6. CD
提示:利用氮原子守恒及氧化剂得电子总数=还原剂失电子总数求解。
7. A
8. D
提示:本题未明确硝酸的浓度,因此硝酸作为氧化剂,其还原产物无法判定。已知硝酸是足量的,说明a g铜全部转化为 ![]() ,利用铜原子守恒,作为酸参加反应的硝酸的物质的量就可求出:
,利用铜原子守恒,作为酸参加反应的硝酸的物质的量就可求出: ![]() ,
,
![]() 。
。
9. D
10. B
提示: ![]() 均极易溶于水,认为试管内布满溶液,即原气体的体积与所形成溶液的体积相等,物质的量浓度相同。而
均极易溶于水,认为试管内布满溶液,即原气体的体积与所形成溶液的体积相等,物质的量浓度相同。而 ![]() 溶于水则发生如下反应
溶于水则发生如下反应 ![]() ,有的同学会误认为此溶液较稀而错选为A。在本题中需注重
,有的同学会误认为此溶液较稀而错选为A。在本题中需注重 ![]() 难溶于水,溶液中溶质为
难溶于水,溶液中溶质为 ![]() ,溶液的体积为试管容积的
,溶液的体积为试管容积的 ![]() ,应选B。
,应选B。
11. C
12. C
提示: ![]() 利用阿伏加德罗定律的推论,同温、同体积下气体的物质的量之比等于其压强比。
利用阿伏加德罗定律的推论,同温、同体积下气体的物质的量之比等于其压强比。
13. D 14. B
提示:题目中酸性溶液说明溶液中存在大量 ![]() ,A中
,A中 ![]() 与
与 ![]() 不能大量共存,C中
不能大量共存,C中 ![]() 在酸性条件下具有强氧化性可将
在酸性条件下具有强氧化性可将 ![]() 氧化成
氧化成 ![]() ,D中
,D中 ![]() 与
与 ![]() 不能大量共存。
不能大量共存。
15. B
提示:从题目已知 ![]() 均为稀酸,可利用离子反应解题。
均为稀酸,可利用离子反应解题。
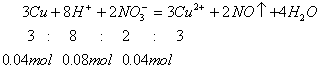
![]() 是由硝酸与硫酸共同提供的,从各物质的“量”上看“
是由硝酸与硫酸共同提供的,从各物质的“量”上看“ ![]() ”将完全反应,铜剩余
”将完全反应,铜剩余 ![]() ,
, ![]() 剩余
剩余 ![]() ,则生成
,则生成 ![]() 。
。
16. NO;HNO3;NO2;NH3;NH4NO3
17. (1) ![]()
(2) ![]()
(3) ![]()
(4) ![]()
两种化肥是 ![]()
18. 解析: ![]() ,
,
气体的物质的量 ![]()
法一: ![]()
![]()

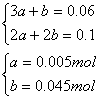
![]()
法二:利用原子守恒
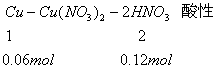
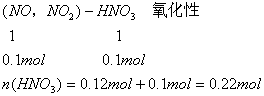
【附加题】1.① Cu+NO ![]() +4H
+4H ![]() =Cu
=Cu ![]() +NO2↑+2 H2O; ② 3Cu+2NO
+NO2↑+2 H2O; ② 3Cu+2NO ![]() +8H
+8H ![]() =3Cu
=3Cu ![]() +2NO↑+ 4H2O; ③ 2Cu+O2
+2NO↑+ 4H2O; ③ 2Cu+O2 ![]() 2CuO;CuO+2H
2CuO;CuO+2H ![]() =Cu
=Cu ![]() +H2O; ③
+H2O; ③
2.(1)NO
(2)稀HNO3、铜屑、蒸馏水,洗去NO2
(3)3Cu 8H 2NO3-=3Cu2 2NO↑ 4H2O
(4)铜屑溶解,溶液为浅蓝色,有气泡产生,瓶内上方出现棕红色气体
(5)收集X前,打开M,排出装置内空气
