苏教版高二化学反应速率与化学平衡检测试题
一、单项选择题(本题包括8小题,每小题4分共32分。每小题只是一个选项符合题意)
1、已经建立化学平衡的某可逆反应,当改变条件使平衡向正反应方向移动时,下列有关叙述中正确的是
A.生成物的质量分数一定增加 B.生成物的物质的量一定增加
C.反应物的转化率一定增加 D.反应物的浓度一定降低
2、一定条件下,可逆反应X(g) 3Y(g) ![]() 2Z(g),若X、Y、Z起始浓度分别为c1、c2、c3(均不为0,单位mol/L),当达平衡时X、Y、Z的浓度分别为0.1mol/L,0.3mol/L,0.08mol/L,则下列判定不合理的是
2Z(g),若X、Y、Z起始浓度分别为c1、c2、c3(均不为0,单位mol/L),当达平衡时X、Y、Z的浓度分别为0.1mol/L,0.3mol/L,0.08mol/L,则下列判定不合理的是
A.c1:c2 = 1:3 B.平衡时,Y和Z的生成速率之比为3:2
C.X、Y的转化率不相等 D.c1的取值范围为0 < c1 < 0.14mol/L
3、某化学反应其△H== —122 kJ·mol-1,∆S== 231 J·mol-1·K-1,则此反应在下列哪种情况下可自发进行
A.在任何温度下都能自发进行 B.在任何温度下都不能自发进行
C.仅在高温下自发进行 D.仅在低温下自发进行
4、将固体NH4I置于密闭容器中,在某温度下发生下列反应.
NH4I(s) ![]() NH3(g)+HI(g),2HI(g)
NH3(g)+HI(g),2HI(g) ![]() H2(g)+I2(g)。当反应达
H2(g)+I2(g)。当反应达
到平衡时,c(H2)=0.5 mol·L-1,c(HI)=4 mol·L-1,则NH3的浓度为( )
A.3.5 mol·L-1 B.4 mol·L-1 C.4.5 mol·L-1 D.5 mol·L-1
5、在一密闭容器中,反应 aA(g) ![]() bB(g)达平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,A的浓度变为原来的60%,则
bB(g)达平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,A的浓度变为原来的60%,则
A、平衡向正反应方向移动了 B、平衡向逆反应方向移动了
C、物质B的质量分数增加了 D、a<b
6、可逆反应:2NO2 ![]() 2NO O2 在密闭容器中反应,达到平衡状态的标志是:
2NO O2 在密闭容器中反应,达到平衡状态的标志是:
①单位时间内生成n molO2的同时生成2n molNO2
②单位时间内生成n molO2 的同时,生成2n mol NO
③用NO2、NO、O2 的物质的量浓度变化表示的反应速率的比为2 : 2 : 1的状态
④混合气体的颜色不再改变的状态 ⑤混合气体的密度不再改变的状态
⑥ 混合气体的平均相对分子质量不再改变的状态
A. ①④⑥ B.②③⑤ C.①③④ D. ①②③④⑤⑥
7、甲、乙两容器都发生反应 2A(g) B(g ) ![]() xC(g),两容器温度和初始压强都相同。甲容器中充入 2 molA 和 1 molB,达平衡后,C 在平衡混合气中的体积分数为φ、物质的量为 n1;乙容器中充入 1.4 molA,0.7 molB 和 0.6 molC,达平衡后 C 在平衡混合气中的体积分数为φ、物质的量为 n2。下列说法中正确的是
xC(g),两容器温度和初始压强都相同。甲容器中充入 2 molA 和 1 molB,达平衡后,C 在平衡混合气中的体积分数为φ、物质的量为 n1;乙容器中充入 1.4 molA,0.7 molB 和 0.6 molC,达平衡后 C 在平衡混合气中的体积分数为φ、物质的量为 n2。下列说法中正确的是
A.若甲、乙两容器均为恒容容器,则 x必等于 2
B.若甲、乙两容器均为恒压容器,则 x必等于 3
C.若甲为恒压容器、乙为恒容容器,且 x≠3,则 n1必大于 n2
D.若甲为恒容容器、乙为恒压容器,且 x= 3,则 n1必大于 n2
8、可用右侧示意图象表示的是
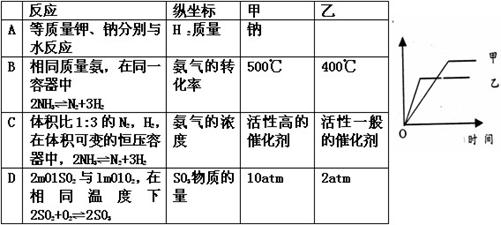
二、不定项选择题(本题包括8小题,每小题4分,共32分。每小题有一个或两个选项符合题意。若正确答案只包括一个选项,多选时,该题为0分;若正确答案包括两个选项,只选一个且正确的得2分,选两个且都正确的得满分,但只要选错一个该小题就为0分)
9、下列事实不能用勒夏特列原理解释的是
A.由H2、I2蒸气、HI组成的平衡体系加压后颜色变深
B.黄绿色的氯水光照后颜色变浅
C.使用催化剂可加快SO2转化为SO3的速率
D.在含有Fe(SCN)2+的红色溶液中加铁粉,振荡静置,溶液颜色变浅或褪去
10、对于平衡体系:aA(g) bB(g) ![]() cC(g) dD(g);正反应放热,有下列判定,其中正确的是:
cC(g) dD(g);正反应放热,有下列判定,其中正确的是:
A.若温度不变,容器体积扩大一倍,此时A的浓度是原来的0.48倍,则a b大于c d
B.若从正反应开始,平衡时,A、B的转化率相等,则A、B的物质的量之比为a:b
C.若平衡体系中共有气体M mol,再向其中充入bmolB,达到平衡时气体总物质的量为M bmol,则a b=c d
D.若a b=c d ,则当容器内温度上升时,平衡向左移动,容器中气体的压强不变。
11、在容积固定的密闭容器中存在如下反应: A(g) B(g) ![]() 3 C(g); (正反应为放热反应)某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,并根据实验数据作出下列关系图:
3 C(g); (正反应为放热反应)某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,并根据实验数据作出下列关系图:
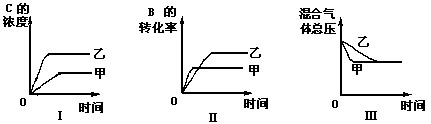
下列判定一定错误的是
A、图I研究的是不同催化剂对反应的影响,且乙使用的催化剂效率较高
B、图Ⅱ研究的是压强对反应的影响,且甲的压强较高
C、图Ⅱ研究的是温度对反应的影响,且甲的温度较高
D、图Ⅲ研究的是不同催化剂对反应的影响,且甲使用的催化剂效率较低
12、某化学科研小组研究在其他条件不变时,改变某一条件对化学平衡的影响,得到如下变化规律(图中P表示压强,T表示温度,n表示物质的量):

根据以上规律判定,上列结论正确的是
A 反应Ⅰ:△H>0,P2>P1 B 反应Ⅱ:△H<0,T1>T2
C 反应Ⅲ:△H>0,T2>T1;或△H<0,T2<T1 D 反应Ⅳ:△H<0,T2>T1
13、如图,Ⅰ是恒压密闭容器,Ⅱ是恒容密闭容器。

其它条件相同时,在Ⅰ、Ⅱ中分别加入2mol X和2mol Y,起始时容器体积均为V L,发生如下反应并达到平衡(X、Y状态未知):2X(?)+Y(?) ![]() aZ(g)。此时Ⅰ中X、Y、Z的物质的量之比为1:3:2,则下列说法一定正确的是
aZ(g)。此时Ⅰ中X、Y、Z的物质的量之比为1:3:2,则下列说法一定正确的是
A.若X、Y均为气态,则平衡时气体平均摩尔质量:Ⅰ>Ⅱ
B.若X、Y不均为气态,则平衡时气体平均摩尔质量:Ⅰ>Ⅱ
C.若X为固态,Y为气态,则Ⅰ、Ⅱ中从起始到平衡所需时间相同
D.平衡时Ⅰ容器的体积小于V L
14、可逆反应A B(s) ![]() C达到平衡后,无论加压或降温。B的转化率都增大,则下列结论正确的是气体
C达到平衡后,无论加压或降温。B的转化率都增大,则下列结论正确的是气体
A. A为固体C为气体,正反应为放热反应 B. A为气体C为固体,正反应为放热反应
C. A为气体C为固体,正反应为吸热反应 D. A、C均为气体,正反应为吸热反应
 15、下图为某化学反应速率—时间图。在t1时刻升高温度或增大压强,都符合下图所示变化的反应是
15、下图为某化学反应速率—时间图。在t1时刻升高温度或增大压强,都符合下图所示变化的反应是
A.2SO2 (g)+O2 (g) ![]() 2SO3 (g) ;△H<0
2SO3 (g) ;△H<0
B.4NH3 (g)+O2 (g) ![]() 4NO(g)+6H2O (g) ;△H<0
4NO(g)+6H2O (g) ;△H<0
C.H2 (g)+I2 (g) ![]() 2HI (g) ;△H>0
2HI (g) ;△H>0
D.C (s)+H2O (g) ![]() CO (g)+H2 (g) ;△H>0
CO (g)+H2 (g) ;△H>0
|
υ(ClO3-) |
|
t1 t2 t |
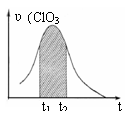 16.KClO3和KHSO3能发生反应:ClO3- HSO3-→SO42- Cl- H (未配平)。已知该反应的速率随c(H )的增大而加快。右图为用ClO3-在单位时间内物质的量浓度变化表示的该反应υ-t图。下列说法正确的
16.KClO3和KHSO3能发生反应:ClO3- HSO3-→SO42- Cl- H (未配平)。已知该反应的速率随c(H )的增大而加快。右图为用ClO3-在单位时间内物质的量浓度变化表示的该反应υ-t图。下列说法正确的
A.反应开始时速率增大可能是c(H )所致
B.纵坐标为υ(Cl-)的υ-t曲线与图中曲线不能完全重合
C.后期速率υ下降的主要原因是反应向逆反应方向进行
D.图中阴影“面积”可以表示t1-t2时间内c(Cl-)增加量
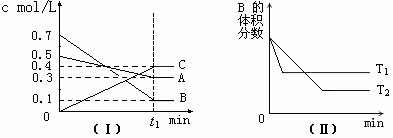
17、T℃时,A气体与B气体反应生成C气体。反应过程中A、B、C浓度变化如图(Ⅰ)所示,若保持其他条件不变,温度分别为T1和T2时,B的体积分数与时间的关系如图(Ⅱ)所示,则下列结论正确的是
A.在 t1时间内用B表示该反应的平均速率为0.6/ t1mol·L-1·min-1
B.在(t1 10)min时,保持其他条件不变,增大压强,平衡向逆反应方向移动
C.T℃时,在相同容器中,若由0.3mol·L—1 A、0.1 mol·L—1 B和
0.4 mol·L—1 C反应,达到平衡后,C的浓度仍为0.4 mol·L—1
D.其他条件不变,升高温度,正、逆反应速率均增大,且A的转化率增大
苏教版选修4《化学反应速率与化学平衡》单元检测试题
答 题 卷
班级_________姓名_____________学号________得分______________
一、单项选择题(本题包括8小题,每小题4分,共32分。每小题只是一个选项符合题意)
![]() 二、不定项选择题(本题包括12小题,每小题4分,共48分。每小题有一个或两个选项符合题意。若正确答案只包括一个选项,多选时,该题为0分;若正确答案包括两个选项,只选一个且正确的得2分,选两个且都正确的得满分,但只要选错一个该小题就为0分)
二、不定项选择题(本题包括12小题,每小题4分,共48分。每小题有一个或两个选项符合题意。若正确答案只包括一个选项,多选时,该题为0分;若正确答案包括两个选项,只选一个且正确的得2分,选两个且都正确的得满分,但只要选错一个该小题就为0分)
![]()
三、(本题包括3小题)
18、在20L恒容的密闭容器中,加入3mo1SO3(g)和lmo1氧气,在一定温度下使其反应,反应至4min时,氧气的浓度为0.09 mol·L-1,当反应到8min时,反应到达平衡,此时三氧化硫浓度c(SO3)= a mol·L-1。
(1)0min~4min内生成O2平均速率v(O2)= mol·L-1·min-1
(2)达到平衡时c(O2)=c(SO2),则a= mol·L-1,在下列坐标系中作出
0min~8min及之后SO2、O2、SO3浓度随时间变化曲线.
(3)若起始时按下表数据投料,相同温度下达到平衡时,三氧化硫浓度大于a mol·L-1的是
19、在某温度下,分别向容积相等的甲、乙两容器中通入0.6molN2O4气体,立即出现红棕色,此反应为吸热反应。反应过程中,甲容器保持体积不变,乙容器保持压强不变。乙容器达到平衡时,混合气体中各物质的物质的量相等。请回答下列问题:
(1)容器中气体出现红棕色的原因是(用化学方程式表示)___________________;
(2)反应达到平衡时,两容器中所需要的时间:甲______乙
(填“大于”、“小于”或“等于”);
(3)乙容器中反应达到平衡时,N2O4的转化率是_______________;
(4)若使甲、乙两容器中反应达到平衡时N2O4的浓度相等,不能采取的措施是(填序号);
A.保持温度不变,适当压缩乙容器的体积 ______________
B.保持容器体积不变,适当升高甲容器的温度
C.保持容器体积不变,向甲容器中通入适量的N2O4
(5)若保持温度不变,乙容器起始时NO2的物质的量为0.4mol,达到平衡时,NO2的物质的量为0.8mol,混合气体中各物质的物质的量仍相等,则起始时容器中N2O4物质的量为________________;
20、可逆反应3A(g) ![]() 3B(?) C(?)(正反应吸热)达到化学平衡后,
3B(?) C(?)(正反应吸热)达到化学平衡后,
(1)升高温度,用“变大”、“变小”、“不变”或“无法确定”填空。
①若B、C都是气体,气体的平均相对分子质量 ;
②若B、C都不是气体,气体的平均相对分子质量 ;
③若B是气体,C不是气体,气体的平均相对分子质量 ;
(2)假如平衡后保持温度不变,将容器体积增加一倍,新平衡时A的浓度是原来的60%,则B是 态,C是 态。
(3)假如B为气体,C为固体,取3molA恒温下在1L容器中充分反应,平衡时测得B的浓度为2.1mol/L。若使反应从逆反应开始,起始时在容器中加入3molB ,同样条件下,要使平衡时B的浓度仍为2.1mol/L,则C的取值范围应该是 。
四、(本题包括3小题)
|
K |
|
A |
B |
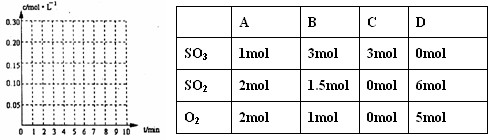
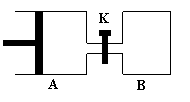 21、如图所示,容器A左侧是可平行移动的活塞。向A中充入1molX和1molY,向B中充入2molX和2molY,起始时V(A)=V(B)=aL。在相同温度和有催化剂存在的条件下,两容器各自发生:X(g) Y(g)
21、如图所示,容器A左侧是可平行移动的活塞。向A中充入1molX和1molY,向B中充入2molX和2molY,起始时V(A)=V(B)=aL。在相同温度和有催化剂存在的条件下,两容器各自发生:X(g) Y(g) 达到平衡时V(A)=1.2aL。试回答:
⑴A中X的转化率为 。
⑵A、B中X转化率大小关系为A B(填“>”、
“<”、“=” )
⑶打开K,一段时间后又达到新的平衡时,A的体积为 L(连通管中气体体积不计)
⑷在⑶达到平衡后,同时等幅升高A、B的温度,达到平衡后,A的体积 (填变大、不变、或变小),其理由是
22、CuCl2溶液有时呈黄色,有时呈黄绿色或蓝色,这是因为在CuCl2的水溶液中存在如下平衡:[Cu(H2O)4]2 4C1一 ![]() [CuCl4]2- 4H2O
[CuCl4]2- 4H2O
蓝色 黄色
现欲使溶液由黄色变成黄绿色或蓝色,请写出两种可采用的方法
⑴ ⑵ 。
23、A是由导热材料制成的密闭容器,B是一耐化学腐蚀且易于传热的气球。关闭K2,将等量且少量的NO2通过K1、K3分别充人A、B中,反应起始时,A、B的体积相同。
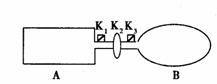 (已知:2NO2
(已知:2NO2 ![]() \s N2O4;△H<0)
\s N2O4;△H<0)
(1)一段时间后,反应达到平衡,此时A、B中生成的N2O4的速率是VA_________VB。(填“>”、“<”、“=”);若打开活塞K2,气球B将__________(填:变大、变小、不变)。
(2)若在A、B中再充人与初始量相等的NO2,则达到平衡时,NO2的转化率
αA将_________ (填增大或减小、不变);若通人等量的Ne气,则达到平衡时,A中NO2的转化率将_________,B中NO2的转化率将_________(填:变大、变小、不变)。
(3)室温下,若A、B都保持体积不变,将A套上一个绝热层,B与外界可以进行热传递,则达到平衡时,_________中的颜色较深。
(4)若在容器A中充人4.6g的NO2,达到平衡后容器内混合气体的平均相对分子质量为57.5,则平衡时N2O4的物质的量为_________。
五、(本题包括3小题)
24、(12分)在一固定容积的密闭容器中,保持一定条件下进行以下反应:
X(气)+2Y(气) ![]() 3Z(气),已知加入1 molX和3molY。达到平衡后,生成a mol Z。
3Z(气),已知加入1 molX和3molY。达到平衡后,生成a mol Z。
(1)在相同实验条件下,若在同一容器中改为加入2 mol X和6 mol Y,达到平衡后,Z的物质的量为 mol。
(2)在相同实验条件下,若在同一容器中改为加入2 mol X和8 mol Y,若要求在反应混合气体中Z体积分数不变,则还需加入Z mol。
(3)在相同实验条件下,若在同一容器中改为加入0.5molX,则需加入 mol Y,
mol Z,才能使平衡时Z为0.9a mol。
25、在某一容积为VL的密闭容器内,加入等物质的量的X和Y,在一定的条件下发
生如下反应:X(g)+Y(g) ![]() 2Z (g)。(正反应是放热反应)(1)反应达到平衡后,降
2Z (g)。(正反应是放热反应)(1)反应达到平衡后,降
低温度,化学反应速率 ,Z的浓度 。(填“增大”、“减小”或“不变”)。
(2)图1、图2表示该反应在t1时达到平衡、在t2时因改变某个条件而发生变化的曲线:
|
|
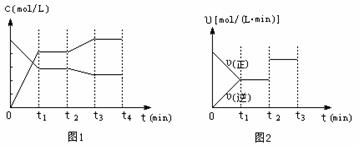
由图1判定,反应进行至t2 min时,曲线发生变化的原因是 (用文字表达)。由图2判定,t2 min到t3 min 的曲线变化的原因可能是 (填编号)
a.降低温度 b.加了催化剂 c.增加Z的量 d.缩小容器体积
 26、(10分)向一定压的仪器中充入4LN2和H2的混合气体,反应后恢复
26、(10分)向一定压的仪器中充入4LN2和H2的混合气体,反应后恢复
到原温度,体积变为3.4L,容器内气体对相同条件下H2的相对密度为5。
⑴反应达到平衡时V(NH3)= L,
反应前V(N2):V(H2)= ,N2的转化率为 。
⑵向平衡后的容器中再充入0.2molNH3,再达到平衡,测得吸收了6.44kJ的热量。
①从开始到重新平衡,混合气体对H2的相对密度变化为 ;
A、先增大后变小 B、先减小后增大 C、一直减小 D、一直不变
②写出合成氨的热化学方程式:
六、(本题包括2小题)
27、一定条件下,某容积为1L的密闭容器中发生如下反应:C(s) H2O(g) ![]() CO(g) H2(g)
CO(g) H2(g)
(Ⅰ)(1)维持温度不变,向该容器中充入2 mol C(s)和2 mol H2O(g),达到平衡后混合气体的平均相对分子质量为Mr,则Mr的范围为 。
(2)在(1)中若充入的是2.5 mol CO(g)和4 mol H2(g),达到平衡后混合气体的平均相对分子质量为 ;若要求达到平衡后混合气体的平均相对分子质量始终大于该值,则充入的CO、H2混合气体的总质量m和总物质的量n必须满足的关系为 。
(Ⅱ)维持温度不变,若在(1)中同时充入1 mol Br2(g),发生如下反应:H2(g) Br2(g) ![]() 2HBr(g)(忽略其他反应)
2HBr(g)(忽略其他反应)
(3)当上述体系达到平衡后,测得容器中c(H2O)平=0.4 mol·L-1,c(Br2)平=0.6 mol·L-1,则平衡时c(H2)平=_______mol·L-1。
(4)当上述体系达到平衡时,欲求其混合气体的平衡组成,则至少还需要知道两种气体的平衡浓度,但这两种气体不可能同时是: 和 ,或 和 (填化学式)。
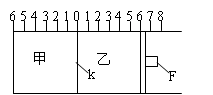 28、(Ⅰ)如图所示,甲、乙之间的隔板K和活塞F都可左右移动,甲中充入2molA和1molB,乙中充入2molC和1molHe,此时K停在0处。在一定条件下发生可逆反应:2A(g) B(g)
28、(Ⅰ)如图所示,甲、乙之间的隔板K和活塞F都可左右移动,甲中充入2molA和1molB,乙中充入2molC和1molHe,此时K停在0处。在一定条件下发生可逆反应:2A(g) B(g) ![]() 2C(g); 反应达到平衡后,再恢复至原温度。回答下列问题:
2C(g); 反应达到平衡后,再恢复至原温度。回答下列问题:
(1)可根据 现象来判定甲、乙都已达到平衡。
(2)达到平衡时,隔板K最终停留在0刻度左侧a处,则a的取值范围是 。
(3)若达到平衡时,隔板K最终停留在左侧刻度1处,则甲中C的物质的量为 mol,
乙中C的转化率 50%(填:>、<、=),此时,乙中可移动活塞F最终停留在右侧
刻度 处(填下列序号:① <6 ② >6 ③ =6)
(4)若达到平衡时,隔板K最终停留在左侧刻度靠近0处,则乙中可移动活塞F最终停留在右侧的刻度不大于 ;若K最终停留在左侧刻度靠近2处,则乙中F最终停留在右侧的刻度不小于 。
(Ⅱ)若一开始就将K、F固定,其它条件均不变,则达到平衡时:
(1)甲、乙中C的物质的量是 (填:“甲>乙”或“甲<乙”或“甲=乙” );
(2)测得甲中A的转化率为b,则乙中C的转化率为 ;
(3)假设乙、甲两容器中的压强比用d表示,则d的取值范围是 。
七、(本题包括2小题)
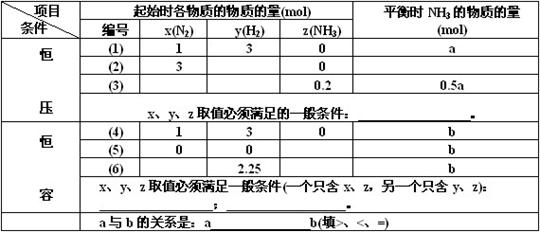
29、密闭容器中,保持一定温度,进行如下反应:N2(g) 3H2(g) ![]() 2NH3(g)。 已知加入1 mol N2和3 mol H2,在恒压条件下,达到平衡时生成a mol NH3[见下表中编号(1)的一行];在恒容条件下,达到平衡时生成b mol NH3[见下表中编号(4)的一行]。若相同条件下,
2NH3(g)。 已知加入1 mol N2和3 mol H2,在恒压条件下,达到平衡时生成a mol NH3[见下表中编号(1)的一行];在恒容条件下,达到平衡时生成b mol NH3[见下表中编号(4)的一行]。若相同条件下,
达到平衡时混合物中各组分的百分含量不变,请填空:
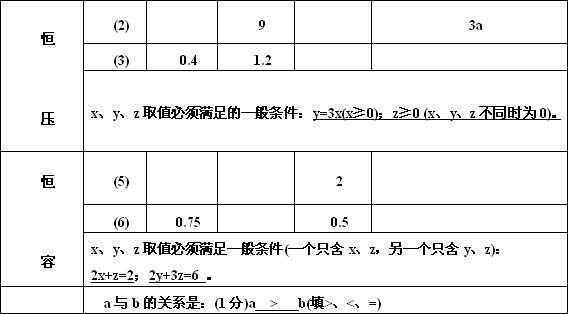
30、反应aA(g) +bB(g) ![]() cC(g)+dD(g)在容积不变的密闭容器中达到平衡,且起始时A与B的物质的量之比为a∶b。则
cC(g)+dD(g)在容积不变的密闭容器中达到平衡,且起始时A与B的物质的量之比为a∶b。则
(1)平衡时A与B的转化率之比是_______________。
(2)若同等倍数地增大A、B的物质的量浓度,要使A与B的转化率同时增大,(a+b)与(c+d)所满足的关系是(a+b) (c+d) (填 >、=、< 或没关系)。
(3)设定a=2 ,b=1,c=3,d=2,在甲、乙、丙、丁4个容器中A的物质的量依次是2 mol、1 mol、2 mol、1 mol,B的物质的量依次是1 mol、1 mol、2 mol、2 mol,C和D的物质的量均为0。则在相同温度下达到平衡时,A的转化率最大的容器是 ,B的转化率由大到小的顺序是 (填容器序号)。
苏教版选修4《化学反应速率与化学平衡》单元检测试题
答 案
1、B 2、C 3、D 4、D 5、B 6、B 7、D 8、A
9、AC 10、BC 11、AD 12、BC 13、AC 14、B 15B 16、AD 17、AC
18、(1) 0.01mol/L. min(2) a=0.05 mol/L 图象如右(3) BD
19、(1)N2O4 ![]() 2NO2 ;(2)小于;(3)33.3%;(4)C;(5)1mol。
2NO2 ;(2)小于;(3)33.3%;(4)C;(5)1mol。
20、 = 1 \* GB2 ⑴ 变小 不变 变小 = 2 \* GB2 ⑵ 固体或液体 固体或液体或气体 = 3 \* GB2 ⑶ c(C)>0.3mol
21、⑴40% ⑵> ⑶2.6aL
⑷变大,升高温度,平衡逆向移动,但温度升高使气体的体积增大,气体浓度减小,平衡向正向移动,且压强不变时,气体体积与温度成正比,为线性关系,是体积变化的主要原因。
22、⑴加水稀释 ⑵加AgNO3溶液
23、(1)< 变小 (2)增大 不变 变小 (3)A (4)0.02mol
24、1 80% 0.6 mol /(L·min)
25、减小,增大 t2 时对平衡体系降温 b d
26、⑴0.6L;1:3;30%;⑵①A;②N2(g) 3H2(g) ![]() 2NH3(g)△H=—92kJ/mol
2NH3(g)△H=—92kJ/mol
27、(1)15<Mr<18 (2)12; m>12n (3)1.2 (4)H2O和CO或Br2和HBr
28、Ⅰ(1)K、F不再移动(2)0<a<2 (3)1mol、〉、② (4)8、4
Ⅱ(1)甲=乙(2)1-b(3)4/3<a<3/2
29、
 30、(1)1:1(2)〉(3)丁(4)甲〉乙〉丙〉丁
30、(1)1:1(2)〉(3)丁(4)甲〉乙〉丙〉丁
