|
гІДКЯў ЯЩОгГЧЗхжабЇ
ПЩФмгУЕНЕФЯрЖддзгжЪСПЃКH-1 C-12 N-14 O-16 S-32
вЛЁЂбЁдёЬт(БОЬтга28аЁЬтЃЌУПаЁЬт2ЗжЃЌЙВ56ЗжЁЃУПаЁЬтжЛга1ИібЁЯюЗћКЯЬтвтЃЌВЛбЁЁЂЖрбЁЁЂДэбЁОљВЛИјЗж)
1ЃЎЛЗБЃВПУХЮЊСЫЪЙГЧЪаЩњЛюРЌЛјЕУЕНКЯРэРћгУЃЌНќФъРДж№ВНЪЕЪЉСЫЩњЛюРЌЛјЗжРрЭЖЗХЕФАьЗЈЁЃЦфжаЫмСЯДќЁЂЗЯжНЁЂОЩЯ№НКжЦЦЗЕШЪєгк
A ЮоЛњЮя B гаЛњЮя C бЮРр D ЗЧН№ЪєЕЅжЪ
2.ЯТСаЮяжЪжаЪєгкКЯН№ЕФЪЧ
AЁЂЛЦН№ BЁЂАзвј CЁЂИж DЁЂЫЎвј
3ЃЎЯТСаЛЏбЇУћДЪе§ШЗЕФЪЧ
AЁЂфхБП BЁЂЩеМю CЁЂввЫсввжЌ DЁЂШмСПЦП
4. ЯТСаЮяжЪЪєгкДПОЛЮяЕФЪЧ
AЁЂУК BН№ИеЪЏ CЪЏгЭ DПеЦј
5.дкЙњМЪЕЅЮЛжЦжаЃЌФІЖћжЪСПЕФЛљБОЕЅЮЛЪЧ
AЁЂKg BЁЂmol CЁЂm3 DЁЂg/mol
6ЃЎдјЖдЛЏбЇЦНКтНјаабаОПВЂЬсГіЦНКтвЦЖЏРэТлЕФЛЏбЇМвЪЧ
AЁЂРеЯФЬиСа BЁЂУХНнСаЗђ CЁЂЕРЖћЖй DЁЂРЭпЮ§
7ЃЎЯТСаЗжзгжаЕФИїдзгОљдкЭЌвЛжБЯпЩЯЕФЪЧ
AЁЂC2H4 BЁЂCH4 CЁЂCH==CH DЁЂCH3ЁЊCH3
8ЃЎНёга0.1mol/L Na2SO4ШмвК300mLЃЌ0.1mol/L MgSO4ШмвК200mLКЭ0.1mol/L Al2(SO4)3ШмвК100mLЃЌетШ§жжШмвКжаСђЫсИљРызгХЈЖШжЎБШЪЧ
A 1ЉU1ЉU1 B 3ЉU2ЉU1
C 3ЉU2ЉU3 D 1ЉU1ЉU3
9. ЯТСаЙ§ГЬжаЃЌВЛПЩФцЕФЪЧ
A.ЕААзжЪЕФбЮЮі B.ѕЅЕФЫсДпЛЏЫЎНт
C. ТШЛЏЬњЕФЫЎНт D. ЕААзжЪЕФБфад
10ЃЎЪЕбщЪвгУAl2(SO4)3жЦШЁAl(OH)3ЃЌзюКЯЪЪЕФЪдМСЪЧ
A.NaOH B.H2SO4 C.NH3ЁЄH2O D.KOH
11ЃЎгаЙиЛЏбЇгУгяе§ШЗЕФЪЧ
AЁЂввЯЉЕФзюМђЪНC2H4 BЁЂввДМЕФНсЙЙМђЪНC2H6O
CЁЂЫФТШЛЏЬМЕФЕчзгЪНeq Cl:\O\AC(C,\S\UP8(..),\S\UP12(Cl),\S\DO2(..),\S\DO10(Cl)):Cl\S\UP8(.. DЁЂГєбѕЕФЗжзгЪНO3
12ЃЎЯТСаН№ЪєвБСЖЕФЗДгІдРэЃЌДэЮѓЕФЪЧЃЈ ЃЉ
AЁЂ2NaCl(ШлШк) 2Na Cl2Ёќ BЁЂMgO H2 Mg H2O
CЁЂFe2O3 3CO 2Fe 3CO2 DЁЂ2Ag2O 4 Ag O2Ёќ
13.ЯТСаЮяжЪЕФШмвКжа,ФмЗЂЩњвјОЕЗДгІЕФЪЧ
A.ввЫс B.ввДМ C.ввШЉ D. ввЫсввѕЅ
14.ЯТСавЧЦїжа,ВЛФмгУгкМгШШЕФЪЧ
A.ЪдЙм B.СПЭВ C.ЩеБ D.зЖаЮЦП
15ЃЎНЋ0.l molЁЄ 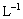 ДзЫсШмвКМгЫЎЯЁЪЭЃЌЯТСаЫЕЗЈе§ШЗЕФЪЧ ДзЫсШмвКМгЫЎЯЁЪЭЃЌЯТСаЫЕЗЈе§ШЗЕФЪЧ
AЃЎШмвКжаcЃЈH ЃЉКЭcЃЈ 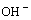 ЃЉЖММѕаЁ BЃЎШмвКжаcЃЈH ЃЉдіДѓ ЃЉЖММѕаЁ BЃЎШмвКжаcЃЈH ЃЉдіДѓ
CЃЎДзЫсЕчРыЦНКтЯђзѓвЦЖЏ DЃЎШмвКЕФpHдіДѓ
16ЃЎЯТСаЙигкЁАЙ§бѕЛЏЧтЁБЕФЫЕЗЈжаЃЌе§ШЗЕФЪЧ
AЁЂ Й§бѕЛЏЧтПЩвдЗЂЩњЗжНтЗДгІ
BЁЂ Й§бѕЛЏЧтЪЧРызг ЛЏКЯЮя
CЁЂ Й§бѕЛЏЧтОпгаЩБОњЯћЖОзїгУЃЌЪЧЧПЫс
DЁЂЙ§бѕЛЏЧтЪЧЫЎЕФЭЌЗжвьЙЙЬх
17ЃЎдкЯТСаЙ§ГЬжаЃЌашвЊдіДѓЛЏбЇЗДгІЫйТЪЕФЪЧ
A. ИжЬњИЏЪД B. ЪГЮяИЏАм C. ЫмСЯРЯЛЏ D. ЙЄвЕКЯГЩАБ
18ЃЎгыЫсЛђМюЖМФмЗДгІЕФРызгЪЧ
A.Fe3 B. HCO3Ѓ C. AlO2Ѓ D. Al3
19ЃЎЯТСаа№Ъіе§ШЗЕФЪЧ
A. ЗЂЩњЛЏбЇЗДгІЪБЪЇШЅЕчзгдНЖрЕФН№ЪєдзгЃЌЛЙдФмСІдНЧП
B. Н№ЪєбєРызгБЛЛЙдКѓЃЌвЛЖЈЕУЕНИУдЊЫиЕФЕЅжЪ
C. КЫЭтЕчзгзмЪ§ЯрЭЌЕФдзгЃЌвЛЖЈЪЧЭЌжждЊЫиЕФдзг
D. ФмгыЫсЗДгІЕФбѕЛЏЮяЃЌвЛЖЈЪЧМюадбѕЛЏЮя
20ЃЎЯТСаРызгЗНГЬЪНжае§ШЗЕФЪЧ
AЁЂ аЁЫеДђШмвКгыЯЁСђЫсЛьКЯЃКCO32Ѓ 2HЃЋ=CO2Ёќ H2O
BЁЂ ТСЦЌгыЧтбѕЛЏФЦШмвКЗДгІЃКAl 2OHЃ=AlO2Ѓ H2Ёќ
CЁЂ ДѓРэЪЏгыбЮЫсЗДгІЃКCaCO3 2 HЃЋ=Ca2ЃЋ H2O CO2Ёќ
DЁЂЬњЦЌЗХШыЯѕЫсвјШмвКжаЃКFe AgЃЋ=Fe2ЃЋ Ag
21ЃЎЩшNAЮЊАЂЗ№МгЕТТоГЃЪ§ЃЌЯТСаа№Ъіжае§ШЗЕФЪЧ
AЁЂдкГЃЮТГЃбЙЯТЃЌ11.2LN2КЌгаЕФЗжзгЪ§ЮЊ0.5NA
BЁЂдкГЃЮТГЃбЙЯТЃЌ1mol NeКЌгаЕФдзгЪ§ЮЊNA
CЁЂ1 L 1 mol/LДзЫсШмвКжаРызгзмЪ§ЮЊ2NA
DЁЂ18gЫЎжаЫљКЌЕФЕчзгЪ§ЮЊ8NA
22ЃЎNaHCO3ШмвКжаЃЌИїРызгХЈЖШЙиЯЕжае§ШЗЕФЪЧ
AЁЂc(Na )ЃКc (HCO3_)>1 BЁЂc(Na )ЃКc (HCO3_)=1
BЁЂc(Na )ЃКc (HCO3_)<1 DЁЂЮоЗЈШЗЖЈ
23ЃЎЧрУЙЫиЪдбщеыгУЫќЕФЯЁЪЭвКЃЈ200ЙњМЪЕЅЮЛЧрУЙЫи/mLЃЉЃЌЯжга1аЁЦП20ЭђЙњМЪЕЅЮЛЧрУЙЫиЃЌ1.0 mLзЂЩфЦїЃЈЗжПЬЖШ0.1 mLЃЉЃЌзЂЩфгУЫЎКЭМИИіИЩОЛаЁЦПЁЃЯжШЁ1.0 mLзЂЩфгУЫЎЕЮзЂШыЕквЛЦПФкШмНтЧрУЙЫиЁЃЮќШЁ0.1 mLШмвКдкЕк2ЦПжагУЫЎЯЁЪЭГЩ1.0 mLЁЃдйЮќШЁ0.1 mLдкЕк3ЦПжаЯЁЪЭГЩ1.0 mLЃЌгжЁЁдкЕкМИИіаЁЦПжаЯЁЪЭКѓЧрУЙЫиХЈЖШЮЊ200ЙњМЪЕЅЮЛ/mLЃК
A. 3 B. 4 C. 5 D. 6
24ЃЎЯТСаЪЕбщжаЃЌе§ШЗЕФЪЧ
A. ЪЕбщЪвгУТШЫсМижЦбѕЦјНсЪјЪБЃЌЯШДгЫЎВлжавЦГіЕМЦјЙмЃЌдйЯЈУ№ОЦОЋЕЦ
B. ГЦСПЙЬЬхЪБЃЌНЋвЉЦЗжБНгЗХдкЬьЦНЭаХЬЩЯ
C. ЯШНЋpHЪджНгУеєСѓЫЎШѓЪЊКѓЃЌдйВтЖЈШмвКЕФpH
D. дкСПЭВжаЯЁЪЭХЈСђЫс
25ЃЎШє1 molФГЦјЬЌЬўCxHyЭъШЋШМЩеЃЌашгУ3 mol O2ЃЌдђ
A. xЃН2ЃЌyЃН2 B. xЃН2ЃЌyЃН4
C. xЃН3ЃЌyЃН6 D. xЃН3ЃЌyЃН8
26ЃЎЯТСаЕчРыЗНГЬЪНжаЃЌВЛе§ШЗЕФЪЧ
AЁЂ Na2 SO4ЃН2Na SO42-
BЁЂ CuCl2ЃНCu2 2Cl-
CЁЂ CH3COOH 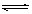 CH3COO- H CH3COO- H
DЁЂH2CO3 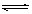 2 H CO3 2 H CO3
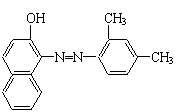 27ЃЎЫеЕЄКьЪЧКмЖрЙњМвНћжЙгУгкЪГЦЗЩњВњЕФКЯГЩЩЋЫиЁЃНс ЙЙМђЪНШчгвЭМЁЃЙигкЫеЕЄКьЫЕЗЈДэЮѓЕФЪЧ 27ЃЎЫеЕЄКьЪЧКмЖрЙњМвНћжЙгУгкЪГЦЗЩњВњЕФКЯГЩЩЋЫиЁЃНс ЙЙМђЪНШчгвЭМЁЃЙигкЫеЕЄКьЫЕЗЈДэЮѓЕФЪЧ
AЁЂЗжзгжаКЌБНЛЗ
BЁЂФмШмгкБН
CЁЂФмБЛЫсадИпУЬЫсМиШмвКбѕЛЏ
EЁЂ ЪєгкЗМЯуЬў
28ЃЎФмКЭЧтбѕЛЏФЦШмвКЗДгІЕФЮяжЪЪЧ
AЃЎМзЭщ B.МзБН C.БНЗг D.ввЯЉ
ЖўЃЎЬюПеЬтЃЈБОЬтга3аЁЬт,ЙВ20ЗжЃЉ
29ЃЎ(10Зж)ЃЈ1ЃЉаДГіввДМгыХЈСђЫсЕФЛьКЯвКдк170OCЪБЗЂЩњЗДгІЕФЛЏбЇЗНГЬЪН Ёј ЁЃИУЗДгІЪєгк Ёј ЗДгІ
ЃЈ2ЃЉаДГіМзБНКЭХЈЯѕЫсЁЂХЈСђЫсЕФЛьКЯвКЗДгІЕФЛЏбЇЗНГЬЪН Ёј
ИУЗДгІЪєгк Ёј ЗДгІ
ЃЈ3ЃЉаДГіNH4ClЫЎНтЕФРызгЗНГЬЪН Ёј ЁЃ
30.ЃЈ6ЗжЃЉ[БОЬтАќРЈ2аЁЬтЃЌУПЮЛЭЌбЇжЛашвЊбЁзівЛаЁЬтЃЌШєСНЬтЖМзіЃЌАДЕкЃЈ1ЃЉаЁЬтМЦЗжЁЃ]
(1) AЪЧЪЏгЭЛЏЙЄЕФдСЯЃЌCЪЧЪГДзЕФжївЊГЩЗж,DЪЧОпгаЙћЯуЮЖЕФвКЬхЁЃдквЛЖЈЬѕМўЯТЃЌЫќУЧЕФбмБфЙиЯЕШчЯТЃК
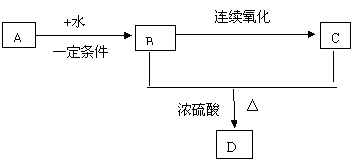
ЪдаДГіAЁЂBЁЂCЕФНсЙЙМђЪНЃК
A Ёј ЃЌB Ёј ЃЌC Ёј ЁЃ
(2) AЁЂBЁЂCЁЂDЫФжжЖЬжмЦкдЊЫиЃЌЦфдзгађЪ§вРДЮдіДѓЃЌетЫФжждЊЫижжжЛгаDЮЊН№ЪєдЊЫиЃЛAгыDЭЌжїзхЃЌBдзгЕФзюЭтВуЕчзгЪ§ЪЧДЮЭтВуЕчзгЪ§ЕФ2БЖЃЌCдЊЫиЮЊЕиПЧжаКЌСПзюЖрЕФдЊЫиЃЌDдзгЕФзюЭтВужЛгавЛИіЕчзгЁЃОнДЫЛиД№ЯТСаЮЪЬтЃК
ЃЈ1ЃЉаДГіBЁЂCЁЂDЕФдЊЫиЗћКХЃКB ЃЌ D ЁЃ
ЃЈ2ЃЉаДГіBC2гыD2C2ЗДгІЕФЛЏбЇЗНГЬЪНЃК
31ЃЎ(4Зж)дквЛЖЈЬѕМўЯТЃЌПЩФцЗДгІЃКCO (g) H2OЃЈgЃЉ 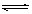 CO2ЃЈgЃЉ H2ЃЈgЃЉ ЃЌШєЩ§Ип CO2ЃЈgЃЉ H2ЃЈgЃЉ ЃЌШєЩ§Ип
ЮТЖШЃЌЦНКтЯђе§ЗДгІЗНЯђвЦЖЏЁЃ
ЧыЛиД№ЯТСаЮЪЬтЃК
ЃЈ1ЃЉИУЗДгІЕФе§ЗДгІЮЊ Ёј ЗДгІЁЃЃЈЬюЁАЮќШШЁБЛђЁАЗХШШЁБЃЉ
ЃЈ2ЃЉШєРЉДѓШнЦїЕФЬхЛ§ЃЌдђИУЗДгІЫйТЪНЋ Ёј ЃЈЬюЁАдіДѓЁБЁЂЁАВЛБфЁБЛђЁАМѕаЁЁБЃЉ
Ш§ЁЂМђД№ЬтЃЈБОЬтга2аЁЬтЃЌЙВ12ЗжЃЉ
32ЃЎ(6Зж)ЧыАДвЊЧѓЬюПеЃК
ЃЈ1ЃЉдкХфжЦAl2(SO4)3ШмвКЪБЃЌЮЊСЫЗРжЙЗЂЩњЫЎНтЃЌПЩвдМгШыЩйСПЕФ____________
ЃЈ2ЃЉввЯЉЪЧЪЏгЭСбНтЕФжївЊВњЮяжЎвЛЃЌНЋввЯЉЭЈШыфхЕФЫФТШЛЏЬМШмвКжаЃЌЙлВьЕНЕФЯжЯѓЪЧ
ЃЈ3ЃЉЪЕбщЪвМьбщШЉЛљЕФГЃгУЪдМСЪЧ
33ЃЎ(6Зж)ШчЯТЭМЫљЪОЃЌAЁЂBЁЂCЪЧЪЕбщЪвГЃгУЕФШ§жжжЦШЁЦјЬхЕФзАжУЃЌЬсЙЉЕФвЉЦЗгаЃКДѓРэЪЏЁЂХЈбЮЫсЁЂЯЁбЮЫсЁЂаПСЃЁЂЖўбѕЛЏУЬЁЂТШЛЏяЇЁЂЪьЪЏЛвЃЎЯжгћРћгУетаЉвЉЦЗЗжБ№жЦШЁNH3ЁЂCl2ЁЂH2ЁЂCO2ЫФжжЦјЬхЃЌЪдЛиД№вдЯТЮЪЬтЃЎ
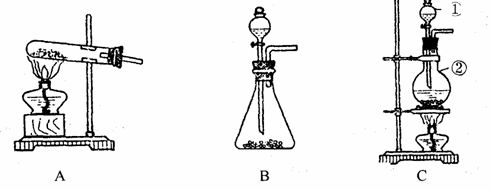
(1) бЁгУBзАжУПЩжЦШЁЕФЦјЬхга________________
(2) (2)БъКХЂйЁЂЂкЕФвЧЦїУћГЦвРДЮЮЊ________________ ЃЌ________________
(3)аДГіРћгУЩЯЪігаЙивЉЦЗжЦШЁАБЦјЕФЛЏбЇЗНГЬЪНЃК___________________________________
ШєвЊжЦЕУИЩдяЕФАБЦјЃЌПЩбЁгУЯТСаИЩдяМСжаЕФ________________(ЬюађКХ)
aЃЎЩњЪЏЛв bЃЌХЈСђЫс C.Ш§ЮхбѕЛЏЖўСз
ЫФЁЂМЦЫуЬтЃЈБОЬтга2аЁЬтЃЌЙВ12ЗжЃЉ
34ЃЎЃЈ6ЗжЃЉ1.12L(БъзМзДПіЯТ)ФГЦјЬЌЬў(CnHm)дкзуСПЕФбѕЦјжаЭъШЋШМЩе,НЋШМЩеВњЮявРДЮЭЈЙ§зуСПЕФХЈСђЫсКЭГЮЧхЪЏЛвЫЎ,ХЈСђЫсдіМг4.5g,,ВЂВњЩњ20gАзЩЋГСЕэ.
(1) ЪдЧѓГіИУЬўЕФЗжзгЪН.
(2) аДГіИУЬўПЩФмЕФНсЙЙМђЪН.
35. ЃЈ6ЗжЃЉдк(NH4)2SO4жаМгШызуСПЕФNaOHШмвК,МгШШ,ГфЗжЗДгІКѓВњЩњ4.48LЦјЬх(БъзМзДПіЯТ).Чѓ(NH4)2SO4ЕФжЪСП.
вЛЁЂ ЕЅЯюбЁдёЬтЃЈУПЬт2ЗжЃЌЙВ56ЗжЃЉ |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
11 |
12 |
13 |
14 | |
B |
C |
B |
B |
D |
A |
C |
D |
D |
C |
D |
B |
C |
D | |
15 |
16 |
17 |
18 |
19 |
20 |
21 |
22 |
23 |
24 |
25 |
26 |
27 |
28 | |
D |
A |
D |
B |
C |
C |
B |
A |
B |
A |
B |
D |
D |
C | |