|
ЩшБОвГЮЊЪзвГЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
ЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁМгШыЪеВи |
|
| жаЮФгђУћ: ЙХНёжаЭт.comЁЁЁЁЁЁЁЁЁЁЁЁ
гЂЮФгђУћЃКwww.1-123.comЁЁЁЁЁЁЁЁЁЁЗсИЛЪЕгУЕФНЬг§НЬбЇзЪСЯ |
| |
| |
| |
|
|
ПЩФмгУЕНЕФЯрЖддзгжЪСПЃКHЁЊ1 CЁЊ12 NЁЊ14 OЁЊ16 ClЁЊ35.5 AgЁЊ108 бЁдёЬтЃЈУПаЁЬтжЛгавЛИібЁЯюЗћКЯЬтвтЁЃУПаЁЬт2ЗжЃЌЙВ50ЗжЃЉ 1.ЯТСаЦјЬхжаЃЌМЋвзШмгкЫЎЕФЪЧ A. Cl2 B. NH3 C. C2H4 D. C2H6 2.ЯТСаЦјЬЌЧтЛЏЮяжаЃЌЮШЖЈадзюЧПЕФЪЧ A. HF B. HCl C. HBr D. HI 3.ЯТСаИїзщдЊЫижаЃЌЪєгкЭЌвЛжїзхЕФЪЧ A. LiЁЂNaЁЂK B. NaЁЂMgЁЂAl C. NЁЂOЁЂF D. OЁЂSЁЂCl 4.ЯТСаН№ЪєжаЃЌжЛФмВЩгУЕчНтЗЈвБСЖЕФЪЧ A. Hg B. Fe C. Na D. Ag 5.ЯТСаИїзщЮяжЪжаЃЌЛЅЮЊЭЌЮЛЫиЕФЪЧ A. 16OКЭ18O B. O2КЭO3 C. COКЭCO2 D. H2OКЭH2O2 6.ЯТСагаЛњЮяжаЃЌгыCH3CH2CH2CH3ЛЅЮЊЭЌЗжвьЙЙЬхЕФЪЧ
C. D. CH2=CHCH2CH3 7.ЯТСагаЛњЮяжаЃЌВЛЪєгкШ§ДѓКЯГЩВФСЯЕФЪЧ A. ЫмСЯ B. ЕААзжЪ C. КЯГЩЯЫЮЌ D. КЯГЩЯ№НК 8. SeЪЧШЫЬхБиашЕФЮЂСПдЊЫиЃЌЫќЕФвЛжжЭЌЮЛЫи A. 34 B. 46 C. 80 D. 114 9.ЯТСаЛЏКЯЮяжаЃЌЪєгкШѕЕчНтжЪЕФЪЧ A. CH3COOH B. NaOH C. NaCl D. HCl ЛЏбЇЪдОэЕкЂёОэЕк1вГЃЈЙВ3вГЃЉ 10.ЯТСаЮяжЪжаЃЌжЛКЌЙВМлМќЕФЪЧ A. NaOH B. Na2O C. HCl D. KCl 11. жЪСПЮЊ32gЕФCH4ЃЌдкБъзМзДПіЯТЬхЛ§дМЮЊ A. 44.8L B. 33.6L C. 22.4L D. 11.2L
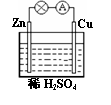 12ЃЎЖдгкаПЁЂЭКЭЯЁСђЫсзщГЩЕФдЕчГиЃЈШчгвЭМЃЉЃЌЯТСагаЙиЫЕЗЈе§ШЗЕФЪЧ 12ЃЎЖдгкаПЁЂЭКЭЯЁСђЫсзщГЩЕФдЕчГиЃЈШчгвЭМЃЉЃЌЯТСагаЙиЫЕЗЈе§ШЗЕФЪЧ
ЂйZnЪЧИКМЋ ЂкCuЪЧе§МЋ ЂлИКМЋЩЯЗЂЩњбѕЛЏЗДгІ Ђме§МЋЩЯЗЂЩњЛЙдЗДгІ AЃЎЂйЂк BЃЎЂкЂл CЃЎЂкЂлЂм DЃЎЂйЂкЂлЂм
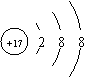
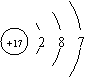
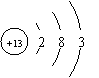 13ЃЎЯТСаСЃзгЕФНсЙЙЪОвтЭМжаЃЌБэЪОТШРызгЕФЪЧ 13ЃЎЯТСаСЃзгЕФНсЙЙЪОвтЭМжаЃЌБэЪОТШРызгЕФЪЧ
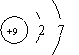
A. B. C. D. 14ЃЎЯТСаЙигкШнСПЦПЕФЪЙгУЗНЗЈжаЃЌе§ШЗЕФЪЧ A. дкШнСПЦПжаПЩжБНгЯЁЪЭХЈСђЫс B. дкШнСПЦПжаПЩжБНгШмНтЧтбѕЛЏФЦЙЬЬх C. ШмвКВЛБиРфШДжСЪвЮТМДПЩзЂШыШнСПЦПжа D. ЯђШнСПЦПжазЊвЦШмвКЪБЃЌашвЊгУВЃСЇАєв§Сї 15ЃЎдкФГвЛЛЏбЇЗДгІжаЃЌЗДгІЮяAЕФХЈЖШдк20 sФкДг1.0 mol / LБфЮЊ0.2 mol / LЃЌдђдкет20 sФкAЕФЛЏбЇЗДгІЫйТЪЮЊ A. 0.04 mol / L B. 0.04 mol / (LЁЄs) C. 0.08 mol / L D. 0.08 mol / (LЁЄs)
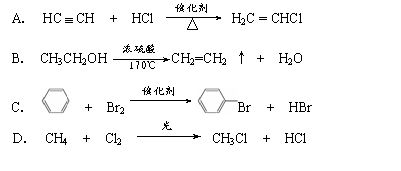 16ЃЎЯТСаЗДгІжаЃЌЪєгкМгГЩЗДгІЕФЪЧ 16ЃЎЯТСаЗДгІжаЃЌЪєгкМгГЩЗДгІЕФЪЧ
AЃЎ B. C. D. ЛЏбЇЪдОэЕкЂёОэЕк2вГЃЈЙВ3вГЃЉ 18ЃЎЯТСаЮяжЪВЛФмЪЙфхЕФЫФТШЛЏЬМШмвКЭЪЩЋЕФЪЧ AЃЎCH2=CH2 BЃЎCH3CH3 CЃЎCH3CЁдCH DЃЎCH3CH=CH2 19ЃЎXЁЂYОљЮЊЖЬжмЦкдЊЫиЃЌXдзгЕФзюЭтВуга2ИіЕчзгЃЌYдзгЕФзюЭтВуга7ИіЕчзгЃЌетСНжждЊЫиаЮГЩЕФЛЏКЯЮяЕФЛЏбЇЪНЪЧ A. XY B. XY2 C. X2Y D. X2Y3 20ЃЎдквЛЖЈЬѕМўЯТЃЌЖдгкУмБеШнЦїжаНјааЕФПЩФцЗДгІЃК2NO2(g) AЃЎNO2ЁЂN2O4ЕФХЈЖШЯрЕШ BЃЎNO2ЁЂN2O4дкШнЦїжаЙВДц CЃЎNO2ЁЂN2O4ЕФХЈЖШОљВЛдйБфЛЏ DЃЎЕЅЮЛЪБМфФкЯћКФ2 mol NO2ЃЌЭЌЪБЩњГЩ1 mol N2O4 21ЃЎББОЉЪаГЩЮЊ2008ФъЕк29НьЯФМОАТдЫЛсЕФОйАьГЧЪаЁЃЮЊЯђЪРНчеЙЯжвЛИіаТББОЉЕФаЮЯѓЃЌгаЙиВПУХЬсГіЯТСаНЈвщЃКЂйПЊЗЂаТФмдДЃЌМѕЩйЛЏЪЏШМСЯЕФШМЩеЃЛЂкЗжРрЛиЪеРЌЛјЃЛЂлЯожЦЪЙгУЫмСЯДќКЭвЛДЮадЫмСЯВЭОпЃЛЂмЬсГЋЪЙгУЪжХСЃЌМѕЩйВЭНэжНЕФЪЙгУЃЛЂнХЉвЕЩЯПижЦЛЏЗЪКЭХЉвЉЕФЪЙгУЁЃФуШЯЮЊПЩвдВЩФЩЕФЪЧ AЃЎЂйЂкЂлЂм B. ЂйЂкЂмЂн C. ЂкЂлЂмЂн D. ШЋВП 22ЃЎФмгУРДМјБ№NaClЁЂNH4ClЁЂK2SO4ЁЂ(NH4) 2SO4ЫФЦПЮоЩЋШмвКЕФЪдМСЪЧ AЃЎNaOHШмвК BЃЎAgNO3ШмвК CЃЎBa(OH)2ШмвК DЃЎBa(NO3)2 ШмвК 23ЃЎЯТСагаЙиЮяжЪгУЭОЕФЫЕЗЈжаЃЌе§ШЗЕФЪЧ ЂйЖўбѕЛЏЙшПЩгУгкжЦдьЙтЕМЯЫЮЌ ЂкТШЦјПЩгУгкздРДЫЎЕФЩБОњКЭЯћЖО ЂлЕЊЦјПЩгУзїКИНгН№ЪєЕФБЃЛЄЦј ЂмЙ§бѕЛЏФЦПЩгУгкЦЏАзжЏЮяЁЂТѓИбAЃЎжЛгаЂйЂк BЃЎжЛгаЂлЂм CЃЎжЛгаЂкЂлЂм DЃЎЖМе§ШЗ 24ЃЎЯТСаРызгЗНГЬЪНжаЃЌе§ШЗЕФЪЧ A. ЯђЫЎжаЭЈШыТШЦјЃКCl2 H2O = 2H Cl- ClO- B. ЯђТШЛЏТСШмвКжаМгШыЙ§СПЕФАБЫЎЃКAl3 4OH- = AlO2- 2H2O C. ЯђСђЫсЬњШмвКжаМгШыЧтбѕЛЏБЕШмвКЃКFe3 3OH- = Fe(OH)3Ё§ D. ЯђЬМЫсЧтФЦШмвКжаМгШыЙ§СПЕФГЮЧхЪЏЛвЫЎЃКHCO3- Ca2 OH- =CaCO3Ё§ H2O 25ЃЎЯТСаЫЕЗЈе§ШЗЕФЪЧ A. Н№ЪєЕЅжЪКЭЫсЗДгІвЛЖЈЗХГіЧтЦј B. КЌН№ЪєдЊЫиЕФРызгвЛЖЈЪЧбєРызг C. ФмгыЫсЗДгІЕФбѕЛЏЮявЛЖЈЪЧМюадбѕЛЏЮя D. КЫЭтЕчзгзмЪ§ЯрЭЌЕФдзгвЛЖЈЪЧЭЌжждЊЫиЕФдзг ЛЏбЇЪдОэЕкЂёОэЕк3вГЃЈЙВ3вГЃЉ ЁЊЁЊЁЊЁЊЁЊЁЊЁЊЁЊЁЊЁЊЁЊЁЊЁЊЁЊЁЊЁЊЁЊЁЊЁЊЁЊЁЊЁЊЁЊЁЊЁЊ вд ЯТ ЮЊ Вн Их жН ЛЏ бЇ Ъд Оэ ЕкЂђОэЃЈЗЧЛњЖСОэ ЙВ50ЗжЃЉ
| ПМ Щњ аы жЊ
| 1ЃЎПМЩњвЊШЯецЬюаДУмЗтЯпФкЕФЧјЯиУћЁЂбЇаЃУћЁЂаеУћЁЂБЈУћКХЁЂПМГЁКХКЭзљЮЛађКХЁЃ 2ЃЎЕкЂђОэАќРЈШ§ЕРДѓЬтЃЌЙВ4вГЁЃД№ЬтЧАвЊШЯецЩѓЬтЃЌПДЧхЬтФПвЊЧѓЃЌАДвЊЧѓШЯецзїД№ЁЃ 3ЃЎД№ЬтБиаыгУКкЩЋЛђРЖЩЋИжБЪЁЂдВжщБЪЃЌзжМЃвЊЙЄећЃЌОэУцвЊећНрЁЃ |
Ьт КХ
вЛ
Жў
Ш§
зм Зж
Зж Ъ§
дФОэШЫ
ИДВщШЫ
ПЩФмгУЕНЕФЯрЖддзгжЪСП: HЁЊ1 CЁЊ12 NЁЊ14 OЁЊ16 ClЁЊ35.5 AgЁЊ108
ЕУЗж
дФОэШЫ
вЛЁЂЬюПеЬтЃЈЙВ24ЗжЃЉ
1ЃЎЃЈ3ЗжЃЉвЛбѕЛЏЬМдкИпЮТЯТПЩгыбѕЛЏЬњЗЂЩњЗДгІЃКFe2O3 3CO ![]() 2Fe 3CO2 ЃЌДЫЗДгІПЩгУгкЙЄвЕЩЯвБСЖН№ЪєЬњЁЃЗДгІжаЃЌзїЮЊбѕЛЏМСЕФЮяжЪЪЧ ЃЈЬюЛЏбЇЪНЃЉЃЌзїЮЊЛЙдМСЕФЮяжЪЪЧ ЃЈЬюЛЏбЇЪНЃЉЁЃдкИУЗДгІжаЃЌШєЯћКФСЫ1mol Fe2O3ЃЌдђЩњГЩ mol FeЁЃ
2Fe 3CO2 ЃЌДЫЗДгІПЩгУгкЙЄвЕЩЯвБСЖН№ЪєЬњЁЃЗДгІжаЃЌзїЮЊбѕЛЏМСЕФЮяжЪЪЧ ЃЈЬюЛЏбЇЪНЃЉЃЌзїЮЊЛЙдМСЕФЮяжЪЪЧ ЃЈЬюЛЏбЇЪНЃЉЁЃдкИУЗДгІжаЃЌШєЯћКФСЫ1mol Fe2O3ЃЌдђЩњГЩ mol FeЁЃ
2ЃЎЃЈ3ЗжЃЉдк ЂйNaClЁЂЂкNH4ClЁЂЂлCH3COONaШ§жжбЮШмвКжаЃЌГЪЫсадЕФЪЧ ЃЈЬюађКХЃЌЯТЭЌЃЉЃЌГЪжаадЕФЪЧ ЃЌГЪМюадЕФЪЧ ЁЃ
3ЃЎЃЈ3ЗжЃЉЖдгкЕкШ§жмЦкЕФЗЧН№ЪєдЊЫиЃЈГ§ArЭтЃЉЃЌДгзѓЕНгвЃЌдзгАыОЖж№НЅ ЃЌЕЅжЪЕФбѕЛЏадж№НЅ ЃЌзюИпМлбѕЛЏЮяЖдгІЫЎЛЏЮяЕФЫсадж№НЅ ЁЃ
ЛЏбЇЪдОэЕкЂђОэЕк1вГЃЈЙВ4вГЃЉ
4ЃЎЃЈ3ЗжЃЉдкЂйгЭжЌЁЂЂкЯЫЮЌЫиЁЂЂлЕААзжЪШ§жжЮяжЪжаЃЌПЩгУгкжЦЗЪдэЕФЪЧ ЃЈЬюађКХЃЌЯТЭЌЃЉЃЌгіХЈЯѕЫсЯдЛЦЩЋЕФЪЧ ЃЌПЩгУгкдьжНЕФЪЧ ЁЃ
5ЃЎЃЈ3ЗжЃЉгаAЁЂBЁЂCШ§жжЮоЩЋЦјЬхЃЌЗжБ№ЪЧN2ЁЂNOЁЂHClЁЂCO2ЁЂNH3ЮхжжжаЕФвЛжжЁЃAФмЪЙЪЊШѓЕФКьЩЋЪЏШяЪджНБфРЖЃЛ AгыBЯргіЃЌгаАзбЬВњЩњЃЛCНгДЅПеЦјСЂМДБфГЩКьзиЩЋЁЃгЩДЫХаЖЈЃК
AЪЧ (ЬюЛЏбЇЪНЃЌЯТЭЌ)ЃЌBЪЧ ЃЌCЪЧ ЁЃ
6ЃЎЃЈ3ЗжЃЉЧтбѕЛЏФЦКЭЧтбѕЛЏТСЪЧСНжжживЊЕФЛЏКЯЮяЁЃЧыЛиД№ЃК
ЃЈ1ЃЉгЩгкФЦЕФН№ЪєадБШТС ЃЌвђДЫЧтбѕЛЏФЦЕФМюадБШЧтбѕЛЏТСЧПЁЃ
ЃЈ2ЃЉдкТШЛЏТСШмвКжаж№ЕЮМгШыЙ§СПЕФЧтбѕЛЏФЦШмвКЃЌЙлВьЕНЕФЪЕбщЯжЯѓЪЧ ЃЈЬюзжФИЃЉЁЃ
a. жЛЗХГіЦјЬх b. ВњЩњАзЩЋГСЕэЃЌЫцКѓГСЕэШмНт
c. жЛВњЩњАзЩЋГСЕэ d. МШВњЩњАзЩЋГСЕэЃЌгжЗХГіЮоЩЋЦјЬх
ЃЈ3ЃЉаДГіЧтбѕЛЏТСгыЧтбѕЛЏФЦШмвКЗДгІЕФРызгЗНГЬЪНЃК
ЁЃ
7ЃЎЃЈ6ЗжЃЉAЁЂBЁЂCДњБэШ§жжЖЬжмЦкдЊЫиЃЌAЪЧЕиПЧжаКЌСПзюЖрЕФдЊЫиЃЛBдЊЫидзгЕФLВуЕчзгЪ§ЪЧKВуЕФ2БЖЃЛCЪЧдзгађЪ§зюаЁЕФдЊЫиЁЃ
ЯжгаМзЁЂввЁЂБћШ§жжжабЇЛЏбЇжаГЃМћЕФЮяжЪЃЌОљгЩAЁЂBЁЂCШ§жждЊЫизщГЩЁЃМздкГЃЮТЯТЮЊЦјЬхЃЌБъзМзДПіЯТЕФУмЖШЮЊ1.34 g / LЃЌЦфЫЎШмвКгаЩБОњЗРИЏадФмЃЛввПЩБЛбѕЛЏГЩБћЃЌБћПЩМЬајБЛбѕЛЏЃЌЕУЕНвЛжжЯрЖдЗжзгжЪСПЮЊМзЕФ2БЖЕФЮяжЪЁЃЧыЛиД№ЃК
ЃЈ1ЃЉМзЕФНсЙЙМђЪНЮЊ ЃЛ
ЃЈ2ЃЉаДГіввдквЛЖЈЬѕМўЯТбѕЛЏЮЊБћЕФЛЏбЇЗНГЬЪНЃК
ЃЛ
ЃЈ3ЃЉдкЪЕбщЪвжаМьбщБћжаЙйФмЭХЕФЪЕбщВйзїЗНЗЈКЭЯжЯѓЮЊЃКдкЪдЙмжаХфжЦЪЪСПЕФвјАБШмвКЃЌЯђЦфжаЕЮМгЩйСПБћЮяжЪЕФШмвКЃЌ
ЁЃ
ЛЏбЇЪдОэЕкЂђОэЕк2вГЃЈЙВ4вГЃЉ
ЕУЗж
дФОэШЫ
ЖўЁЂЪЕбщЬтЃЈЙВ18ЗжЃЉ
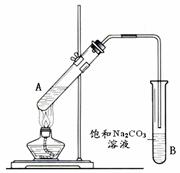 8ЃЎЃЈ4ЗжЃЉЪЕбщЪвРћгУгвЭМЫљЪОзАжУжЦШЁввЫсввѕЅЁЃЧыЛиД№ЃК
8ЃЎЃЈ4ЗжЃЉЪЕбщЪвРћгУгвЭМЫљЪОзАжУжЦШЁввЫсввѕЅЁЃЧыЛиД№ЃК
ЃЈ1ЃЉЪдЙмAжаЪЂЗХЕФЪдМСЮЊввЫсЁЂ КЭХЈСђЫсЃЌЫќУЧжЎМфЗЂЩњЗДгІЩњГЩввЫсввѕЅЕФЛЏбЇЗНГЬЪНЮЊ
ЁЃ
ЃЈ2ЃЉМгШШвЛЖЮЪБМфКѓЃЌПЩЙлВьЕНBЪдЙмжавКУцЩЯгаЮоЩЋ
зДвКЬхЩњГЩЁЃBЪдЙмжаЕФЕМЙмВЛЩьШывКУцЯТЕФдвђЪЧ ЃЈЬюађКХЃЉЁЃ
ЂйЗРжЙШмвКЕЙЮќ ЂкБмУтЗДгІЙ§Пь
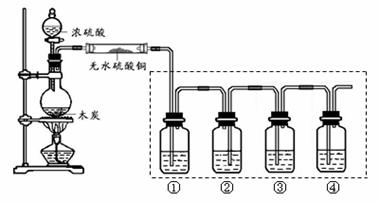 9ЃЎЃЈ8ЗжЃЉЯТЭМЪЧФГЭЌбЇЩшМЦЕФФОЬПКЭХЈСђЫсЗДгІВЂМьбщЫљЕУВњЮяЕФЪЕбщзАжУЁЃЧыЛиД№ЃК
9ЃЎЃЈ8ЗжЃЉЯТЭМЪЧФГЭЌбЇЩшМЦЕФФОЬПКЭХЈСђЫсЗДгІВЂМьбщЫљЕУВњЮяЕФЪЕбщзАжУЁЃЧыЛиД№ЃК
ЃЈ1ЃЉдкзАжУЂйЁЊЂмжаЃЌгаУїЯдДэЮѓЕФвЛИіЪЧ ЃЈЬюађКХЃЉЁЃ
ЃЈ2ЃЉаДГіФОЬПКЭХЈСђЫсЗДгІЕФЛЏбЇЗНГЬЪНЃК ЁЃ
ЃЈ3ЃЉзАжУЂйжаЫљЪЂЪдМСЪЧ ЃЈЬюзжФИЃЉЁЃ
a. ЦЗКьШмвК b. ГЮЧхЕФЪЏЛвЫЎ c. ЫсадИпУЬЫсМиШмвК
ЃЈ4ЃЉзАжУЂлжаЪдМСШєЮЊЦЗКьШмвКЃЌдђЦфзїгУЪЧ ЁЃ
10ЃЎЃЈ6ЗжЃЉФГаЃПЮЭтаЁзщЭЌбЇЩшМЦСЫШчЯТЪЕбщЃЌвдВтЖЈNa2CO3ЁЂNaHCO3КЭBaSO4ЙЬЬхЛьКЯЮябљЦЗжаЬМдЊЫиЕФжЪСПЗжЪ§ЁЃЪЕбщЙ§ГЬШчЯТЭМЫљЪОЃК
|
бљЦЗ W g |
|
ЙЬЬх |
|
ШмвКA |
|
ВйзїЂйЁЂЂк |
|
зуСПЪдМСЂй |
|
ШмвКC |
|
ЦјЬхD |
|
ЪдМСЂкдіжи m g |
|
зуСПЪдМСЂк |
|
ВйзїЂл |
|
ЯДЕг |
|
ШмвКB |
|
ЙЬЬх |

ЧыЛиД№:
ЃЈ1ЃЉВйзїЂйЁЂЂкЕФУћГЦвРДЮЪЧ_____________________ЁЃ
ЃЈ2ЃЉ дбљЦЗжаЬМдЊЫиЕФжЪСПЗжЪ§ЮЊ_________________ЃЈгУКЌWЁЂmЕФДњЪ§ЪНБэЪОЃЉЁЃ
ЃЈ3ЃЉШєИУаЁзщЭЌбЇгЩгкВйзїВЛЕБЖјЪЙВтЖЈНсЙћЦЋИпЃЌЦфдвђПЩФмЪЧ____ЃЈЬюзжФИЃЉЁЃ
a. ЪдМСЂйКЭЂкгУСПВЛзу b. ЙЬЬхЮДОЯДЕг c. ЦјЬхDЮДОИЩдя
ЛЏбЇЪдОэЕкЂђОэЕк3вГЃЈЙВ4вГЃЉ
ЕУЗж
дФОэШЫ
Ш§ЁЂМЦЫуЬтЃЈЙВ8ЗжЃЉ
11ЃЎЃЈ4ЗжЃЉНЋШмгаБъзМзДПіЯТ1.12L HClЦјЬхЕФбЮЫсгызуСПЕФAgNO3ШмвКГфЗжЗДгІЁЃЪдМЦЫуЃЈзюКѓНсЙћОЋШЗжС0.01ЃЉЃК
ЃЈ1ЃЉЩњГЩAgClЕФЮяжЪЕФСПЮЊЖрЩйЃП
ЃЈ2ЃЉЩњГЩAgClЕФжЪСПЮЊЖрЩйЃП
12ЃЎЃЈ4ЗжЃЉАБЪЧвЛжжживЊЕФЛЏЙЄВњЦЗЃЌПЩгУгкжЦШЁЯѕЫсЁЂеЈвЉЁЂЛЏЗЪЕШЁЃ
ЃЈ1ЃЉ дкЙЄвЕКЯГЩАБЕФЗДгІжаЃЌШєЗДгІКѓЦјЬхЕФзмЬхЛ§МѕЩйСЫ5040 m3ЃЈБъзМзДПіЃЉЃЌдђЩњГЩАБЦјЕФжЪСПЮЊ kgЁЃ
ЃЈ2ЃЉЯѕЫсЙЄвЕЕФЮВЦјжажївЊКЌгаNOЁЂNO2ЦјЬхЃЌЙЄвЕЩЯПЩгУАБЦјНјаажЮРэЃЌЪЙЦфзЊЛЏЮЊЮоЖОЕФЕЊЦјЁЃгаЙиЗДгІЕФЛЏбЇЗНГЬЪНЮЊЃК
6NO 4 NH3 ![]() 5N2 6H2O
5N2 6H2O
6NO2 8 NH3 ![]() 7N2 12H2O
7N2 12H2O
ЯжгаNOКЭNO2ЕФЛьКЯЦјЬх60 LЃЌгУАБЦјНјааДІРэЃЌЧЁКУЯћКФЭЌЮТЭЌбЙЯТЕФNH3 68 LЁЃдђдЛьКЯЦјЬхжаNOгыNO2ЕФЮяжЪЕФСПжЎБШЮЊ ЁЃ
ЛЏбЇЪдОэЕкЂђОэЕк4вГЃЈЙВ4вГЃЉ
ЛЏбЇЪдОэД№АИМАЦРЗжВЮПМ
ЫЕУїЃКПМЩњД№АИШчгыБОД№АИВЛЭЌЃЌШєД№ЕУКЯРэЃЌПЩзУЧщИјЗжЃЌЕЋВЛЕУГЌЙ§дЬтЫљЙцЖЈЕФЗжЪ§ЁЃ
ЕкЂёОэЃЈЙВ50ЗжЃЉ
бЁдёЬтЃЈУПаЁЬт2ЗжЃЌЙВ50ЗжЃЉ
ЬтКХ
1
2
3
4
5
6
7
8
9
10
Д№АИ
B
A
A
C
A
C
B
B
A
C
ЬтКХ
11
12
13
14
15
16
17
18
19
20
Д№АИ
A
D
D
D
B
A
D
B
B
C
ЬтКХ
21
22
23
24
25
Д№АИ
D
C
D
D
D
ЕкЂђОэЃЈЙВ50ЗжЃЉ
вЛЁЂЬюПеЬтЃЈЙВ24ЗжЃЉ
1ЃЎЃЈ3ЗжЃЉFe2O3 ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ1Зж
CO ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ1Зж
2 ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ1Зж
2ЃЎЃЈ3ЗжЃЉЂкЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ1Зж
ЂйЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ1Зж
ЂлЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ1Зж
3ЃЎЃЈ3ЗжЃЉМѕаЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ1Зж
діЧПЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ1Зж
діЧПЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ1Зж
4ЃЎЃЈ3ЗжЃЉЂйЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ1Зж
ЂлЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ 1Зж
ЂкЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ1Зж
5ЃЎЃЈ3ЗжЃЉNH3 ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ1Зж
HClЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ1Зж
NOЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ1Зж
6ЃЎЃЈ3ЗжЃЉЃЈ1ЃЉЧП ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ1Зж
ЃЈ2ЃЉb ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ1Зж
ЃЈ3ЃЉAl(OH)3 OH- = AlO2- 2H2O ЁЁЁЁЁЁЁЁЁЁЁ1Зж
|
ДпЛЏМС Ёї |
ЃЈ2ЃЉ2CH3CH2OH O2 2CH3CHO 2H2OЁЁЁЁЁЁЁ2Зж
ЃЈ3ЃЉАбЪдЙмЗХдкШШЫЎжаЮТШШЃЌОВжУМИЗжжгЃЌЙлВьЕНЪдЙмФкБкЩЯИНзХвЛВуЙтССЕФвјОЕ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ 2Зж
ЛЏбЇЪдОэД№АИМАЦРЗжВЮПМЕк1вГЃЈЙВ2вГЃЉ
ЖўЁЂЪЕбщЬтЃЈЙВ18ЗжЃЉ
8ЃЎЃЈ4ЗжЃЉЃЈ1ЃЉввДМЃЈОЦОЋЃЉЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ1Зж
|
Ёї |
|
ХЈСђЫс |
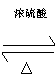 |
CH3COOH CH3CH2OH CH3COOCH2CH3 H2OЁЁ1Зж
ЃЈ2ЃЉгЭ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ1Зж
ЂйЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ1Зж
9ЃЎЃЈ8ЗжЃЉЃЈ1ЃЉЂк ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ2Зж
ЃЈ2ЃЉC 2H2SO4ЃЈХЈЃЉ ![]() CO2Ёќ 2SO2Ёќ 2H2OЁЁЁЁЁЁ2Зж
CO2Ёќ 2SO2Ёќ 2H2OЁЁЁЁЁЁ2Зж
ЃЈ3ЃЉa ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ2Зж
ЃЈ4ЃЉМьбщSO2ЪЧЗёГ§ОЛ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ2Зж
10ЃЎЃЈ6ЗжЃЉЃЈ1ЃЉШмНтЃЌЙ§ТЫЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ2Зж
ЃЈ2ЃЉ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ 2Зж
ЃЈ3ЃЉc ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ2Зж
Ш§ЁЂМЦЫуЬтЃЈЙВ8ЗжЃЉ
11ЃЎЃЈ4ЗжЃЉНтЃК HCl AgNO3 == AgClЁ§ HNO3 ЁЁЁЁЁЁ1Зж
22.4 L 1mol
1.12L n (AgCl) ЁЁЁЁЁЁЁЁ1Зж
ЃЈ1ЃЉn (AgCl)= ![]() ЁЁЁЁЁЁЁЁЁЁЁЁ1Зж
ЁЁЁЁЁЁЁЁЁЁЁЁ1Зж
ЃЈ2ЃЉm (AgCl) = 0.05 molЁС143.5 g / mol = 7.18 g ЁЁЁЁЁЁЁ1Зж
Д№ЃКЃЈТдЃЉ
13ЃЎЃЈ4ЗжЃЉ
ЃЈ1ЃЉ3825 ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ 2Зж
ЃЈ2ЃЉ3:7 ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ 2Зж
ЛЏбЇЪдОэД№АИМАЦРЗжВЮПМЕк2вГЃЈЙВ2вГЃЉ
| |
| |
| |
| 2004-2010ЁЁ жаЙњемЪПЭјАцШЈЫљгаЁЁв§гУБОеОФкШнЧыжИУїРДдДЁЁ ИјБОеОЭЖИхЁЁ ЁЁБИАИађКХ ЪёICPБИ05009253КХЁЁ
|