本试卷分选择题和非选择题两部分,满分100分,考试时间90分钟
第一部分 选择题(共70分)
一、选择题(本题包括35小题,每小题2分,共70分。每小题只有1个选项符合题意)
1.下列元素不属于卤旆元素的是
A. F B. Cl C. C D. I
2.根据元素周期表决断,原子半径最大的是
A.Na B. Al C. Si D. S
3.自然界中有以游离态存在的元素是
A. Si B. Cl C. Na D. N
4.下列物质不能在氯气中燃烧的是
A 铜丝 B 钠 C 红磷 D 氧气
5. 实验室制取下列气体中,只能用排水法收集的是
A. H2 B. NO C. NH3 D. Cl2
6.下列说法正确的是
A. 钠在空气中燃烧生成淡黄色的氧化钠 B. 钠在空气中燃烧生成白色的氧化钠
C. 钠在空气中燃烧生成淡黄色的过氧化钠 D. 钠在空气中燃烧生成白色的过氧化钠
7.下列物质既能与盐酸反应,又能与氢氧化钠溶液反应,而且都没有气体产生的是
 A. Mg B. Al C. Na2CO3 D. Al(OH)3
A. Mg B. Al C. Na2CO3 D. Al(OH)3
8.右图是新制氯水受光照的实验,烧瓶中产生的无色气泡是
A. Cl2 B. O2 C. HCl D. H2
9.将下列溶液敞口放置一段时间,溶液质量增加的是
|
Fe S = FeS |
|
△ |
10 关于反应,下列 , 下列说法正确的是
A. Fe是还原剂,发生了氧化反应 B. Fe是氧化剂,发生了还原反应
C. Fe是还原剂,发生了还原反应 D. Fe是氧化剂,发生了氧化反应
11.下列物质与水混合时, 能发生氧化还原反应的是
A. Cl2 B. NH3 C. SO2 D. SiO2
12.下列物质中不能使酸性高锰酸钾溶液褪色的是
A. 乙烯 B. 乙炔 C. 丙烯 D. 苯
13.下列溶液分别通入CO2后没有浑浊或沉淀出现的是
A. Na2SiO3 B. Ca(OH)2 C. CaCl2 D. Ba(OH)2
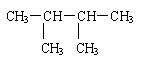
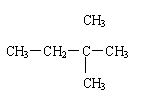
14.烷烃X的名称是2-甲基丁烷, 则X的结构简式是
|
CH3-CH-CH-CH3 |
|
CH3 |
|
CH3 |
|
CH3-CH2-C-CH3 |
|
CH3 |
|
CH3 |
 |
![]()
|
CH2-CH2-CH2-CH3 |
|
CH3 |
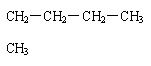 C. D.
C. D. 
![]()
![]()
|

|
 15.如图所示,向淀粉溶液中分别滴加2~3滴碘水和NaI溶液,出现的现象是
15.如图所示,向淀粉溶液中分别滴加2~3滴碘水和NaI溶液,出现的现象是
 A 都变蓝色 B. 都不变蓝色
A 都变蓝色 B. 都不变蓝色
C.变蓝色,不变蓝色 不变蓝色变蓝色
|
|
|
A. 酯化反应 B. 水解反应 C. 加成反应 D. 加聚反应
17.下列物质中既含有离子键,又含有共价键的是
A.NaCl B. NaOH C. CO2 D. HCl
18.科学研究中常用 18O作为示踪原子。下面关于18O的说法正确的是
A. 18O与16O是同素形体 B. 18O与16O是同系物
C. 18O与16O 所含的质子数相同 D. 18O 与16O所含的中子数相同
19.下列关于氧族元素的说法, 正确的是
A. S在空气中燃烧生成SO3 B. 硒是半导体
C. 氧气和臭氧的性质相同 D. 氧族元素都能生成 6价的化合物
20. 将少量固体甲投入足量液体乙中, 产生一种难溶于水的无色气体, 反应后液体中出现白色沉淀或浑浊, 甲和乙可能分别是
|
![]() 21. 某温度下正反应方向放热的反应 A(g) 3B(g) 2C(g)在密闭容器中达到平衡,下列条件变化能使平衡向正反应方向移动的是
21. 某温度下正反应方向放热的反应 A(g) 3B(g) 2C(g)在密闭容器中达到平衡,下列条件变化能使平衡向正反应方向移动的是
A. 增大压强 B. 升高温度 C. 增加催化剂的质量 D. 增大C的浓度
22. 下列各组离子能在溶液中大量共存的是
A Ag 、Na 、CO32—、 Cl— B Na 、 H 、HCO3—、NO3—
C Na 、Ba2 、OH—、NO3— D Mg2 、K 、OH—、NO3—
23. 溶液中, 由于的水解,使得.假如要使更接近于,可采取的措施是
A. 加入少量氢氧化钠 B. 加入少量盐酸 C. 加入少量水 D. 加热
 24. 右下图是浓硫酸与铜反应的实验装置,a处为品红溶液,b为蘸有少量碱液的棉花,下列说法正确的是
24. 右下图是浓硫酸与铜反应的实验装置,a处为品红溶液,b为蘸有少量碱液的棉花,下列说法正确的是
A a处检验是否有SO2生成,b处防止空气进入
B a处检验是否有SO3生成,b处吸收SO3
C a处吸收SO2生成,b处检验是否有SO2逸出
D a处检验是否有SO2生成,b处吸收SO2
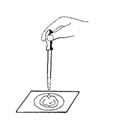 25. 如右下图所示,用脱脂棉包住下列固体物质放在石棉网上,然后用胶头滴管往脱脂棉滴加水,脱脂棉肯定不能着火燃烧的是
25. 如右下图所示,用脱脂棉包住下列固体物质放在石棉网上,然后用胶头滴管往脱脂棉滴加水,脱脂棉肯定不能着火燃烧的是
A Na2CO3 B Na2O2
C K D Na
26. NA为阿伏加德罗常数,下列说法正确的是
A 常温常压下,1 mol N2的体积约是22.4L
B 常温常压下,16 g O2所含的原子数目为NA
C 标准状况下,11.2L Cl2 所含的原子数目为0.5 NA
D 标准状况下,22.4L H2O 所含的分子数目为NA
27. 下列事实不能说明“F、Cl、Br、I”非金属性逐渐减弱的是
A 它们的单质与氢气反应的轻易程度逐渐降低 B 它们的气态氢化物稳定程度逐渐降低
C. 它们的原子半径逐渐增大 D. 除F外,它们的最高价氧化物对应的水化物酸性逐渐减弱.
28. a、b、c分别是Cu、Mg、Al种三种金属中的一种,已知(1)常温下a投入浓硝酸中没有气泡冒出;(2)b插入稀硫酸时,没有气泡产生,但a与b用导线连接后再插入稀硫酸中,b上有气泡产生。由此可推断a、b、c依次为
A. Mg、Al、Cu B. Al、Cu、Mg C. Cu、Al、Mg D. Al、Mg、Cu
29. 下列反应能用离子方程式 H OH— = H2O表示的是
A 氢氧化铜与稀硫酸 B 氧化钙与稀盐酸 C 氢氧化铜与醋酸 D 氢氧化钠与稀硫酸
30. 某同学用下图所示方法,检验粉笔中是否含有微溶于水的硫酸钙。
|
|

 关于①溶液和②溶液,说法正确的是
关于①溶液和②溶液,说法正确的是
![]()
![]() A. ①是稀盐酸,②是BaCl2
A. ①是稀盐酸,②是BaCl2
|

 B. ①是BaCl2,②是稀盐酸
B. ①是BaCl2,②是稀盐酸
|
![]()
![]() D. ①是稀硫酸,②是BaCl2
D. ①是稀硫酸,②是BaCl2
31. X与Y是同一周期的短周期元素,下列说法正确的是
A. X的阳离子与Y的阴离子电子层数相同 B. X的阳离子与Y的阴离子相差一个电子层
C. X与Y的原子的最外层电子数相同 D. X与Y的最高化合价相同
32. 相同温度下氢离子浓度相同的盐酸和醋酸溶液,它们的物质的量浓度分别为c1和c2,c1与c2的关系是
A. c1 = c2 B. c1 > c2 C. c1 < c2 D.
33. 已知某气态烃在标准状况下的密度为2.50g/L。该烃的分子式为
A C2H4 B C4H6 C C4H8 D C4H10
34. 下列除杂质的方法不正确的是
A. 食盐固体中有少量的NH4Cl;将混合物加热
B. NaHCO3固体中混有少量Na2CO3;将混合物加热
C. NO中有少量NO2;将混合气体通过装有水的洗气瓶后再干燥
D. H2中混有少量的HCl气体;将混合气体通过装有NaOH溶液的洗气瓶后再干燥
35. 用一定物质的量浓度的BaCl2溶液,使物质的量浓度相同的FeSO4溶液和Fe2(SO4)3溶液中的SO42—完全沉淀。假如所用的BaCl2溶液的体积比为1:2,FeSO4和Fe2(SO4)3溶液的体积之比为
A. 1:1 B. 1:3 C. 3:1 D. 3:2
第二部分 非选择题(共30分)
二、(本题共6分)
36. (6分)葡萄糖是一种重要的营养物质,它是人类生命活动所需能量的重要来源之一。腹泻病人通常需要进行葡萄糖输液或喝一些葡萄糖水以补充水和营养。
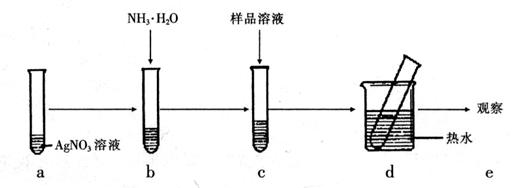 (1)实验室有一瓶没有贴标签的白色粉末,可能是葡萄糖或蔗糖中的一种,某同学用实验来检验。他首先取少量样品酿成溶液,然后按下图所示步骤进行实验:
(1)实验室有一瓶没有贴标签的白色粉末,可能是葡萄糖或蔗糖中的一种,某同学用实验来检验。他首先取少量样品酿成溶液,然后按下图所示步骤进行实验:
本实验的目的是检验样品中是否含有 (填官能团名称),假如观察到 现象时,说明样品中含有这种官能团,从而证实样品为 (填葡萄糖或蔗糖);
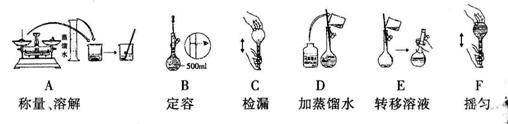 (2)用上述样品配制500L物质的量浓度为的溶液。各步操作如下图所示:
(2)用上述样品配制500L物质的量浓度为的溶液。各步操作如下图所示:
①正确的操作顺序是(填写操作的字母代号) ;
②操作C的具体方法是:往瓶内加入一定量水,塞好瓶塞。用食指摁住瓶塞,另一只手托住瓶底,把瓶倒立过来,观察瓶塞四周是否有水漏出。假如不漏水,将瓶正立并 ,仍把瓶倒立过来,再检查是否漏水。
③某同学进行操作F后,发现溶液的液面低于刻度线,于是又滴加水至刻度线,该同学的操作 (填正确或错误)。
三、(本题共12分)
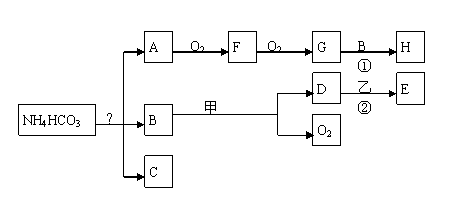
37. (6分)有关关碳酸氢铵的一些转化关系如下图所示(其中有些反应的某些产物图中没有标出)。
SHAPE \* MERGEFORMAT
|
NH4HCO3 |
|
C |
|
B |
|
A |
|
F |
|
G |
|
O2 |
|
D |
|
H |
|
E |
|
O2 |
|
O2 |
|
B |
|
甲 |
|
乙 |
|
① |
|
②②②② |
|
∆ |

已知:
①甲是一种淡黄色的固体化合物,乙是地壳中含量最多的金属元素的单质;
②常温下A、C、F、G均为气体,B为无色液体;
请回答:
(2)反应的化学方程式为:
(3)反应的化学方程式为:
38. (6分)A、B、C、D是四种短周期元素,它们的原子序数依次增大;A位于周期表中第2周期IVA族;B是其同一周期中金属性最强的元素;A原子与B原子的质子数之和等于D原子的质子数;C原子最外层电子数比D的最外层电子数少1。
(1)A的原子结构示意图为 ,B与C形成的化合物的电子式为 。
(2)B的碳酸盐的水溶液显 (填“酸”、“碱”或“中”)性,其原因可用离子方程式表示为:
(3)C的最高价氧化物的水化物在一定条件下与A单质反应的化学方程式为。
四、(本题共6分)
39. 某有机物A的分子式为C4H8O3,已知:
①A能溶于水,其水溶液中滴入紫色石蕊显红色;
②A既能够与乙醇进行酯化反应,也能够与乙酸进行酯化反应;
③A中所含的甲基是其同分异构体中最多的。
回答下列问题:
(1)A中含有的官能团是 和 ;
(2)A与乙醇酯化反应的化学方程式(要注明反应条件)是
(3)根据所学知识推测,除了酯化反应,A还能进行其他化学反应,写出其中一个反应的化学方程式;。
五、(本题共6分)
40. 某氢氧化钠样品含有碳酸钠。取该样品15g 配成100mL溶液,向该溶液中加入Ba(OH)2溶液至不再产生沉淀,过滤,洗涤,干燥,得到沉淀5.91g 。求:
(1)样品中碳酸钠的质量分数。
(2)若所加Ba(OH)2溶液的体积为100mL,则Ba(OH)2溶液的物质的量浓度是多少?
