陈学君 黄岩二高
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 Mg 24 Al 27 Cl 35.5 Fe 56
第Ⅰ卷(选择题 共56分)
一、选择题(28小题,每小题2分,共56分,每小题只有一个选项符合题意。
1.下列物质属于纯净物的是 ( )
A.石油 B.氨水
C.福尔马林 D.冰醋酸
2.据报道,在月球的土壤中含有较丰富的eq \o(\s\up 6( 3),\s\do 2( 2)) 3 2He,它可以作为未来核聚变的重要原料。eq \o(\s\up 6( 3),\s\do 2( 2)) 3 2He原子核内的中子数是 ( )
A.1 B.2 C.3 D.4
3.Cl2摩尔质量为 ( )
A. 71g B. 71 C. 71g/mol D. 71mol
4.下列厨房用品中,其水溶液显碱性的是 ( )
A.食醋 B.料酒 C.食盐 D.纯碱
5.在某一化学反应中,反应物A的浓度在15 s内从3.0 mol/L变成1.5 mol/L,在这15 s内A的化学反应速率为 ( )
A.1.5 mol/(L·s) B.1.5 mol/L
C.0.1 mol/(L·s) D.0.1 mol/L
6.下列金属中,通常采用热还原法冶炼的是 ( )
A.Na B.Al C.Fe D.Ag
7.下列有机物中,不溶于水的是 ( )
A.苯 B.乙醇 C.乙醛 D.乙酸
8.下列分子中,所有原子不可能共处在同一平面上的是: ( )
A、C2H2 B、C6H6 C、C2H4 D、CH3CH3
9.只用一种试剂区分KCl、NH4Cl、FeCl3、AlCl3,这种试剂是 ( )
A.AgNO3 B.HCl C.NaOH D.KSCN
10.有关环境污染的下列说法中,不正确的是 ( )A.焚烧废旧塑料是减少“白色污染”的有效方法
B.二氧化硫是大气的主要污染物之一
C.氟氯烃能破坏大气臭氧层
D.从保护环境考虑,未来最理想的燃料是氢气
11、下列溶液中,c(H )最大的是 ( )
A.0.1mol·L-1HCl溶液 B 0.1mol·L-1H2SO4溶液
C.0.1mol·L-1NaOH溶液 D.0.1mol·L-1CH3COOH溶液
12、下列物质中,既有离子键又有共价键的是 ( )
A H2O B Ba(OH)2 C NaCl D N2
13、碳与浓硝酸反应,显示了浓硝酸的 ( )
A、不稳定性 B、挥发性 C、强氧化性 D、酸性
14. 在反应4 NH3 5 O2 = 4 NO 6 H2O 中,还原剂是 ( )
A、NH3 B、O2 C、NO D、H2O
15、下列物质能发生皂化反应的是 ( )
A、淀粉H2 B、纤维素O2 C、蛋白质 D、油脂
16. CH3CH2CH(CH3)2的正确命名为: ( )
A、3、3-二甲基丙烷 B、1、1-二甲基丙烷
C、2-甲基丁烷 D、3-甲基丁烷
17.下列各组离子,在强酸性溶液中能大量共存的是 ( )
A.Al3 、K 、NO- 3 B. Fe2 、Na 、NO- 3
C.Na 、Cl一、HCO3- D.Na 、SO32一、S2-
18.有标准状况下的四种气体,这四种气体的体积最大的是: ( )
A.6.72L甲烷 B. 3.01´1023个氯化氢分子
C.13.6g硫化氢 D. 0.2mol氨气。
19.下列说法正确的是 ( )
A.1H、2H、3H互为同素异形体 B.O2、O3互为同位素
C.乙酸和甲酸甲酯互为同分异构体 D.乙烷、乙烯、乙炔互为同系物
20.可逆反应N2 3H2 ![]() 2NH3(正反应为放热反应)达到平衡后,下列选项中三种方法都能使平衡向正反应方向移动的是 ( )
2NH3(正反应为放热反应)达到平衡后,下列选项中三种方法都能使平衡向正反应方向移动的是 ( )
A.升高温度、减小压强、增加氢气 B.降低温度、增大压强、分离出部分氨气
C.降低温度、减小压强、增加氮气 D.升高温度、增大压强、增加氨气
21硫酸厂有一辆存放过浓硫酸的铁槽车,某新工人违反操作规程,边吸烟边用水冲洗,结果发生了爆炸事故。下列所述引起爆炸的原因,正确的是 ( )
A.硫酸遇明火发热爆炸 B.浓硫酸遇水发热爆炸
C.铁与水反应产生氢气,氢气接触空气后遇明火爆炸
D.稀释后的硫酸与铁反应产生氢气接触明火爆炸
22.下列除去杂质所用试剂正确的是 (括号内杂质) ( )
A.CH4(C2H4)通入酸性KMnO4溶液
B.Fe2O3(Al2O3)滴加盐酸 ,后过滤
C.苯(苯酚)滴加NaOH溶液,后分液
D.CO2(HCl)通入Na2CO3溶液
23.对下列各组物质性质的比较,正确的是 ( )
A.原子半径:K>Na>Li B.还原性:Fe>Na>K
C.碱性强弱:KOH>Mg(OH)2>Al(OH)3>NaOH
D.与酸反应放出氢气的剧烈程度:Na<Mg<Al
24.在下列有关实验的叙述中,正确的是 ( )
A.用烧杯或烧瓶给液态物质加热时,不用垫石棉网
B.苯酚沾在手上立即用酒精清洗
C.在用托盘天平称量固体药品时,药品放在右盘上
D.假如未知溶液中滴加BaCl2溶液有白色沉淀生成,证实原溶液中一定含有SO42—离子
25.在通常状况下能共存,且能用浓硫酸干燥的一组气体是 ( )
A.H2,O2,N2 B.O2,NO,NO2
C.H2,N2,NH3 D.NH3,HCl,NO2
26.某有机物的结构简式为CH2=C(CH3)-COOH,它不可能具有的性质是 ( )
A.使酸性高锰酸钾溶液褪色. B.发生加聚反应
C.发生银镜反应 D.发生还原反应
27、0.1mol/L的NH4Cl溶液中,离子浓度大小排列正确的是: ( )
A、c(Cl-)> c(NH4 )> c(OH-)> c(H )
B、c(NH4 )> c(Cl-)> c(OH-)> c(H )
C、c(Cl-)> c(NH4 )> c(H )> c(OH-)
D、c(NH4 )> c(Cl-)> c(H )> c(OH-)
28.在用锌片、铜片和稀硫酸组成的原电池装置中,经过—段时间工作后,下列说法正确的是 ( )
A.锌片是正极,铜片是负极 B.电子是从锌片通过导线流到铜片上
C.溶液中H 移向锌片被还原变成H2 D.电解液的pH逐渐变小
第Ⅱ卷(非选择题 共44分)
二、填空题(共33分。)
29.(4分)写出下列反应的化学方程式:
(1)实验室制氨气 ______________________________________ 。
(2) CaCO3与稀盐酸溶液反应(写离子方程式) ___________________________
30.(8分)已知有机物A、B、C、D、E、F间有下图所示转化关系,其中A的分子式是C3H6O2,C是一种可用做果实催熟剂的气体。
|
Ag O2
|
![]() E F
E F
试回答:
(1)A、F的结构简式为:
A、_____________,F__________________。
(2)写出下列转化的化学方程式,并指明有机反应类型:
B→C_______________________________________,反应类型____________
C→D______________________________________,反应类型_____________
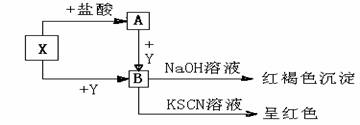 31.(7分)常见金属X,有下列关系图,根据下列图式回答:
31.(7分)常见金属X,有下列关系图,根据下列图式回答:
①写出X的名称 。
②写出A ![]() B的化学方程式 。
B的化学方程式 。
③A溶液与NaOH溶液在空气中反应的现象 。
并写出有关的化学方程式 。
|
A |
|
B |
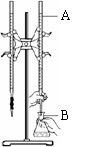 32.(6分) 在实验室用已知浓度的盐酸滴定某未知浓度的NaOH溶液,装置和操作如右图所示。请回答:
32.(6分) 在实验室用已知浓度的盐酸滴定某未知浓度的NaOH溶液,装置和操作如右图所示。请回答:
(1)配制50 mL一定浓度的盐酸,需选用______容量瓶(填字母)。
|
(2)仪器A的名称是_______________________,此滴定管的规格为25.00mL,若C处液面读数为15.00mL,则滴定管内所装溶液的体积为:________
A、10.00mL B、15.00mL C、>10.00mL D、<10.00mL
(3)若以酚酞为指示剂,则达滴定终点时颜色变化为________锥形瓶B中发生反应的离子方程式为_______________________________。
33.(7分)
(1)
|
A |
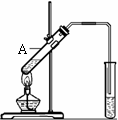 实验室用右图所示装置制取乙酸乙酯,在试管A中加入的试剂有无水酒精、浓硫酸和冰醋酸(CH3COOH)。请写出该反应的化学方程式:________________________________________。
实验室用右图所示装置制取乙酸乙酯,在试管A中加入的试剂有无水酒精、浓硫酸和冰醋酸(CH3COOH)。请写出该反应的化学方程式:________________________________________。
(2)若CH3COOH中的氧都为氧-18,而CH3CH2OH中的氧为氧-16,则所得乙酸乙酯的相对分子量为__________。
|
_____________________________________________将乙酸乙酯从混合溶液中分离出来应采用_______________的方法。
三、计算题(12分)
34.燃烧某有机物A3.0g,生成2.24LCO2(标准状况)和0.1mol水。该有机物的蒸气对空气的相对密度是1.04,求该有机物的分子式。
35.一定量的Mg、Al的混合物中加入足量盐酸,产生标准状况下的气体5.6升,再在此溶液中加入过量NaOH溶液,产生沉淀5.8克,求:
(1)Mg、Al的物质的量各为多少?
(2)若将此混合物投入足量的NaOH溶液中,求标准状况下产生气体的体积。
参考答案(黄二高)
第Ⅰ卷(选择题 共56分)
一、选择题(28小题,每小题2分,共56分)
|
题号 |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
11 |
12 |
13 |
14 |
|
答案 |
D |
A |
C |
D |
C |
C |
A |
D |
C |
A |
B |
B |
C |
A |
|
题号 |
15 |
16 |
17 |
18 |
19 |
20 |
21 |
22 |
23 |
24 |
25 |
26 |
27 |
28 |
|
答案 |
D |
C |
A |
B |
C |
B |
D |
C |
A |
B |
A |
C |
C |
B |
第Ⅱ卷(非选择题 共44分)
二、填空题(共33分。)
|
(1)实验室制氨气 Ca(OH)2 2NH4Cl == CaCl2 2NH3↑ 2H2O 。
![]()
(2) CaCO3与稀盐酸溶液反应(写离子方程式) CaCO3 2H == Ca2 CO2↑ H2O
![]()
30.(8分)
(1)A、F的结构简式为:
![]()
![]() A、 HCOOCH2CH3 ,F、 CH3COOH 。
A、 HCOOCH2CH3 ,F、 CH3COOH 。
|
![]()
|
![]() C→D CH2=CH2 HCl CH3CH2Cl,反应类型:加成反应
C→D CH2=CH2 HCl CH3CH2Cl,反应类型:加成反应
31.(7分)
①写出X的名称:铁。
②写出A ![]() B的化学方程式 2FeCl2 Cl2= 2FeCl3 。
B的化学方程式 2FeCl2 Cl2= 2FeCl3 。
③A溶液与NaOH溶液在空气中反应的现象:开始有白色沉淀产生但马上变为灰绿色最终变为红褐色沉淀 。
并写出有关的化学方程式 FeCl2 2NaOH= Fe(OH)2↓ 2NaCl
4Fe(OH)2 O2 2H2O= 4Fe(OH)3 。
32.(6分)
(1)_ a _
(2)__酸式滴定管__, ___C_____
|
|
(3) 由浅红色变为无色, H OH- = H2O
|
|
(2)90。
|
三、计算题(12分)
34. CH2O
35.
(1)n(Mg)=0.1mol, n(Al) =0.1mol
(2)V(H2)= 3.36L
