何方洁 杜桥中学
相对原子质量:H-1,C-12,O-16,Na -23
一.选择题(每小题只有1个正确选项符合题意。每小题2分,共56分)
1.为了科学地饮食,了解一些与食品相关的化学知识是必要的。油炸虾条、薯片等轻易挤碎的食品,不宜选用真空袋装,而应采用充气袋装。下列气体中最适宜充入的是
A.氮气 B.二氧化碳 C.空气 D.氧气
2.下列说法正确的是
A.在加碘食盐中,碘以单质形式存在
B.纳米材料是指一种称为“纳米”的新物质制成的材料
C.光导纤维是以二氧化硅为主要原料制成的
D.绿色食品是指不含任何化学物质的食品
3.据报道,125 53I可用于治疗肿瘤,该粒子原子核内的中子数为
A.53 B.72 C.75 D.125
4.通常状况下能共存,且能用浓硫酸干燥的一组气体是
A.H2、O2、N2 B.O2、NO、NO2
C.H2、N2、NH3 D.NH3、HCl、NO2
5. 物质的量相等的CO2和O2,它们
A. 原子数相等 B. 分子数相等 C. 质量相等 D. 质子数相等
6.下列仪器中,过滤必须用到的是
|
A. |
|
B |
|
D |
|
C |
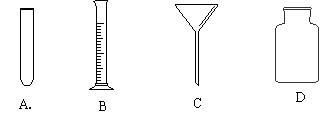
7.下列各项在化学反应中一定发生变化的是
A.元素种类 B.原子数目 C.化学键 D.原子核
8.下列反应中硫元素表现出氧化性的是
A.稀硫酸与锌粒反应 B.浓硫酸与铜反应 C.二氧化硫与氧气反应 D.三氧化硫与水反应
9.下列对于实验室事故的处理,合理的是
A.酒精灯失火后,立即用水 B.金属钠失火,立即用泡沫灭火器灭火
C.苯酚沾在手上,立即用氢氧化钠溶液洗涤
D.不慎将烧碱溶液溅到皮肤上,立即用水冲洗
10. 常温下,下列物质的水溶液的PH大于7的是
A. Na2CO3 B. Na2SO4 C. NH4Cl D. KCl
11 .下列各组物质中,互为同分异构体的是
A.葡萄糖和蔗糖 B.蔗糖和麦芽糖 C.淀粉和纤维素 D.胶棉和火棉
12.下列各组离子,在强碱性溶液中可以大量共存的是
A.K 、Ca2 、HCO3-、Cl- B.Ba2 、Na 、AlO2-、NO3-
C.NH4 、Na 、NO3-、CO32- D.Na 、Fe3 、Cl-、SO42-
13.下列说法中,正确的是
A.在周期表里,元素所在的周期数等于原子核外电子层数
B.在周期表里,主族元素所在的族序数等于原子核外电子数
C.最外层电子数为8的粒子是稀有气体元素的原子
D.元素的原子序数越大,其原子半径也越大
14.对下列各组物质性质的比较中,正确的是
A.原子半径:K > Na > Li
B.还原性:Fe > Na > K
C.碱性强弱:KOH > Mg(OH)2 > Al(OH)3 > NaOH
D.与酸反应放出氢气的剧烈程度:Na < Mg < Al
15.设NA为阿伏加德罗常数,下列说法中不正确的是
A.2.3g金属钠变为钠离子时失去的电子数是0.1NA
B.0.5NA个氯分子所占体积约为11.2L
C.32g氧气所含原子数为2NA
D.18g水所含的质子总数为10NA
16.只用一种试剂,能将NH4Cl、(NH4)2SO4、NaCl、Na2SO4四种溶液区分开,这种试剂是
A.NaOH溶液 B.AgNO3溶液 C.Ba(OH)2溶液 D.BaCl2溶液
17.在下列反应的离子方程式中,正确的是
A.铁与硫酸铜溶液反应:Fe Cu2 ==Fe2 Cu
B.钠与水反应:2Na 2H2O==2Na OH- H2↑
C.碳酸钙与盐酸反应:CO32- 2H ==CO2↑ H2O
D.氢氧化钡与稀硫酸反应:Ba2 OH- H SO42-==BaSO4 H2O
18.下列关于F、Cl、Br、I的比较中,不正确的是
A.它们的原子核外电子层数随原子序数的增加而增多
B.被其它卤素单质从卤化物中置换出来的可能性随原子序数的增加而大
C.它们的氢化物的稳定性随原子序数的增加而增强
D.它们的单质颜色随原子序数的增加而加深
19.在下列反应中,能置换出铁的是
A.Cu FeCl2(溶液) B.Na FeSO4(溶液)
C.Ag FeSO4(溶液) D .Al Fe3O4(高温)
20.A、B、C、D四种金属,将AB用导线连接后,浸在稀硫酸中,在A上有氢气放出,而B溶解;当活泼金属浸在含有A和C两种金属离子可溶性盐溶液里时,在活泼金属上先析出C,把D放入B的硝酸盐溶液中,则D表面有B析出。这四种金属的活动性由强到弱的顺序是
A.A>B>C>D B.D>B>A>C
C.D>C>B>A D.D>B>C>A
21.在N2(g) 3H2(g) ![]() 2NH3(g)的反应中,经过2 s后,氨气的浓度
2NH3(g)的反应中,经过2 s后,氨气的浓度
增加了0.4mol/L,在这2 s 内NH3的化学反应速率是
A.0.1mol/(L·s) B.0.2mol/(L·s)
C.0.3mol/(L·s) D.0.4mol/(L·s)
22.下列是除去括号内杂质的有关操作,其中正确的是
A.乙醇(乙醛)——加水,振荡静置后分液
B.乙酸乙酯(乙酸)——加乙醇、浓硫酸加热
C.乙烯(乙炔)——将气体通过盛KMnO4溶液的洗气瓶
D.苯(苯酚)——加足量NaOH溶液,振荡静置后分液
23 .下列反应中,有沉淀产生且不会消失的是
A.将氨水逐滴滴入硝酸银溶液中,直至过量
B.将NaOH溶液逐滴滴入AlCl3溶液中,直至过量
C.向NaAlO2溶液中逐滴滴入稀硫酸
D.向NaOH溶液中逐滴滴入Fe2(SO4)3溶液直至过量
24.用金属铜制取硝酸铜,从节约原料和防止污染综合考虑,最好的方法是
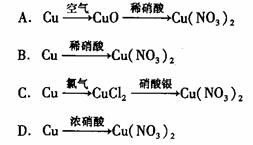
25.下列物质的电子式正确的是

26.下列变化中,由加成反应引起的是
A.乙炔通入高锰酸钾酸性溶液中,高锰酸钾溶液褪色
B.在催化剂作用下,乙烯与水反应生成乙醇
C.新制的Cu(OH)2中加入乙醛加热,有红色沉淀产生
D.在浓硫酸存在下,加热乙醇和乙酸的混合液,有芳香油状液体生成
27.目前,莽草酸是合成抗禽流感药物——达菲的主要原材料,它存在于八角茴香中。已知莽草酸的结构简式为:
|
OH |
|
OH |
|
C |
|
O |
|
HO |
|
—OH |
 |
下列有关莽草酸的说法正确的是
A.该合物中含有苯环
B.该化合物的分子式是C7H6O5
C.该化合物在一定条件下可以与氢气发生加成反应
D.该化合物不能和
|
|
28.下列各反应达到化学平衡后,加压或降温都能使化学平衡向逆反应方向移动的是
A.2NO2 ![]() N2O2 (正反应为放热反应)
N2O2 (正反应为放热反应)
B.C(s) CO2 ![]() 2CO (正反应为吸热反应)
2CO (正反应为吸热反应)
C.N2 3H2 ![]() 2NH3 (正反应为放热反应)
2NH3 (正反应为放热反应)
D.H2S ![]() H2 S(s) (正反应为吸热反应)
H2 S(s) (正反应为吸热反应)
二.填空题(本题有3小题,共20分)
29.(3分)浓H2SO4具有①酸性,②强氧化性,③吸水性,④脱水性.根据题意填空(填序号):
(1)浓H2SO4常用作气体干燥剂,是因为它具有____________;
(2)加热乙醇和浓H2SO4的混合物可制得乙烯,是利用了浓硫酸的___________和催化作用;
(3)常温下可以用铁制容器贮运浓H2SO4,是因为浓H2SO4有_____________
30.(4分)请将下列物质或粒子相互关系的代号填入相应的空格内。
a.同分异构体 b.同位素 c.同系物 d.同素异形体
(1)正丁烷与异丁烷 。
(2)氧气与臭氧 。
(3)甲醇和乙醇 。
(4)1 H、2 H和3 H 。
31.(7分)A、B、C、D四种短周期元素,原子序数依次增大。A原子的最外电子层上有4个电子;B的阴离子和C的阳离子有相同的电子层结构,两元素的单质反应,生成一种淡黄色的固体E;D原子的L电子层上的电子数等于K、M两个电子层上的电子数之和。请回答下列问题:
(1)四种元素的元素符号为:A ,B ,C ,D 。
(2)画出C的离子结构示意图 ,写出D的最高价氧化物对应水化物的化学式 。
(3)写出A的最高价氧化物与E反应的化学方程式
|
A |
|
O2 |
|
催化剂 |
|
催化剂 |
|
H2 |
|
C |
|
B |
|
E |
|
D |
|
浓硫酸 |
|
170℃ |
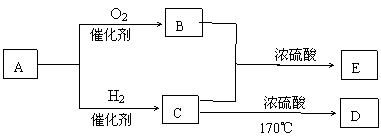 32.(6分)某有机物A为有刺激气味易挥发的液体,能与新制氢氧化铜悬浊液共热生成砖红色沉淀;有机物E的分式为C4H8O2,且具有芳香气味。A、B、C、D、E之间的转化关系如下图(图中部分产物和反应条件已略去)
32.(6分)某有机物A为有刺激气味易挥发的液体,能与新制氢氧化铜悬浊液共热生成砖红色沉淀;有机物E的分式为C4H8O2,且具有芳香气味。A、B、C、D、E之间的转化关系如下图(图中部分产物和反应条件已略去)
请回答下列问题:(1)写出A物质的结构简式
(2)写出A转化为B的化学反应类型
(3)写出B与C反应生成E的化学方程式
三.简答题(本题有2小题,共12分。)
|
A |
|
二氧化锰 |
|
B |
|
氯气 |
|
NaOH溶液 |
|
浓盐酸 |
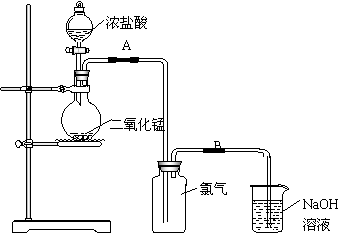 33.(6分)下图是一位学生设计的利用二氧化锰和浓盐酸制取氯气的实验装置图。
33.(6分)下图是一位学生设计的利用二氧化锰和浓盐酸制取氯气的实验装置图。
请回答下列问题:
(1)要制得氯气该装置还缺少的仪器是
(2)烧杯里NaOH溶液的作用是 写出在烧杯中发生反应的离子方程式
(3)实验开始前,某学生对装置进行了气密性检查。方法是:连接好装置后,用弹簧夹夹住 处(填“A”或“B”)橡胶管;向分液漏斗中加水,然后打开分液漏斗的活塞,当加到一定量时,停止加水,静置观察,当观察到分液漏斗中的液面 时,表明该装置不漏气。
 34(6分)右图为实验室制取乙酸乙酯的装置图。试回答:
34(6分)右图为实验室制取乙酸乙酯的装置图。试回答:
(1) B中所盛试剂是 ,其作用是 。伸入B中的导管不能插入叶面下的原因是:① 、② 。
(2) 反应结束后,将B管振荡、静置,待液体分层后,上层无色透明的油状液体具有 气味。酸和醇的酯化反应也属于 反应。
四.计算题(本题有2小题,共12分。)
35 .将13.44L(标准状况)乙烯和乙烷的混合气体通入足量的溴的四氯化碳溶液中,充分反应后,溴的四氯化碳溶液的质量增加了5.6g。求原气体混合物中乙烯与乙烷的物质的量之比。
36.(6分)取Na2CO3和NaHCO3混合物的样品4.42 g,加热至质量不再变化,剩余固体的质量为3.18 g。另取一定量该样品,向其中加入某物质的量浓度的盐酸240 mL,恰好完全反应,生成气体的体积在标准状况下为22.4 L。计算:
(1)样品中Na2CO3和NaHCO3的物质的量之比;
(2)加入盐酸的物质的量浓度。
参考答案
一、选择题
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
11 |
12 |
13 |
14 |
|
A |
B |
B |
A |
B |
C |
C |
B |
D |
A |
B |
B |
A |
A |
|
15 |
16 |
17 |
18 |
19 |
20 |
21 |
22 |
23 |
24 |
25 |
26 |
27 |
28 |
|
B |
C |
A |
C |
D |
B |
B |
D |
D |
A |
D |
B |
C |
B |
二、填空题
29: 3 (2) 4 (3) 2
30:(1) a (2) d (3) c (4)1 b
|
86 |
|
2 |
|
6 |
 31:: (1):A C ,B O ,C Na ,D S
31:: (1):A C ,B O ,C Na ,D S
(2) H2SO4
(3) 2CO2 2Na2O2===2Na2CO3 O2
32: (1) CH3CHO (2) 氧化反应
(3)CH3CH2OH CH3COOH SHAPE \* MERGEFORMAT
|
浓硫酸 |
|
△ |
三.简答题
33:(1)酒精灯 (2)吸收多余的氯气,防止污染环境
Cl2 2OH— == Cl- ClO-- H2O
(3) A; 保持不变
34 (1)饱和Na2CO3溶液,
除去乙酸乙酯中的少量乙酸和乙醇,
有利于乙酸乙酯的分离, 防止液体发生倒吸。
(2) 果香, 取代.
四.计算题
35 1:2
36 (1)1:4 (2)5mol/L
