|
�����ŵ�ʹ��
��������п��Ծ��жԱ����ŵĿ�����Ҫ��ʽ�����¼��ַ�ʽ�����ж������ļ����һ�λ��б�����ʹ�õ�����ѡ����ȷ��һ���ѡ��������������ñ����ŵ�һ��۸��ݱ������Ҫ��Ϊһ�λ�����ȥ�����ŵĵط�������ȷ�ı����ţ�����ԭ������ʹ�ò���ȷ�ı����ţ��ݽ�Ͼ����ᄈ�����ⳣ�ñ���������������õ���������ѡ���磺
2002 �㽭���ݾ�
���о����еı�����ʹ�ö���ȷ��һ����( )
A���ڲ���Ա�IJ����У��������������һ�������ǰѸö�ȥ�����ֶ���������
B���ɰ����Լ�����������ֱ�ӵĹ��������۵İ��Լ������ʧ���ߣ�������ʹ�㲻��ȡʤ���ֹ۵İ��Լ������ʤ���ߣ�����������������ijɹ���
C���γ����ֺ;���ӽ÷���䲻�٣��������˿ڵĵ�Ȼ�ǡ���Ӱ��бˮ��dz�����㸡���»ƻ衣��
D��ʫ����ע�ػ�����ɫ���������������ϣ��⾳�ȡ�����ˣ�����Ի��ʫ������������������ʫ��
������������Ҫ����ѧ����ð�š��ֺš��������ŵ����ü�ʡ�Ժŵȱ����ŵ�����������������������������һ����ѡ�⣬��������⣬����Ҫ�ι�
��ѧĿ�꣺
1 ��ѧ����һ���˽�����ƽ���ߵĺ��壬���ܽ�һ������ƽ�����������е�һЩʵ��
2�����������dzߵȹ�����ƽ���ߡ�
3���ܹ�ֱ��L��һ��P����һ��ƽ����L��ֱ��
��ѧ�ص���ѵ㣺
�ص㣺����ƽ���ߵĸ���
�ѵ㣺��һ�����ƽ���ߵĺ��塢����ƽ���ߡ��˽�ƽ���ߵ�һЩ����
��ѧý�壺��ѧƽ̨
��ǰѧ������������ϰ��
��ѧ���̣�
һ ��ϰ����
��ʾ��һЩ��ͬ��״���ĸ��ı��Σ�
�ʣ���Щ�����ۣ�Ϊʲô���Ǹ��ٹ�·������Ӧ����������λ�ù�ϵ��Ϊʲô����Ӧ�û���ƽ�У�����·��Խ��Խ����Խ��Խխ����
�ʣ����ܾټ��������б����õ�ƽ����Ƶ�������
����ͬ�߶ȡ����ż���ĵ��ߣ��������Եķ��֣�˫�ܵ�������˼��ĸ���ֱ�ĸ��ӵȡ���
�ʣ������˺�ϲ����ѩ��ѩ���ǻ�ѩ�е���Ҫ���ߣ�������ѩ�����ڻ�ѩ������Ӧ�ñ���ƽ�У�����֪��Ϊʲô�������Dz�ƽ�У��������أ�
�ʣ�������������������������ֱ����ƽ������
�� ���Ľ�
1 ʦ����ͬһƽ���ڣ����ཻ������ֱ�߽���ƽ���ߣ���ʾ����
��ͬһƽ���� �� �������ཻ������ֱ�� ������������ȱһ���ɡ�
ʦ����֪��Ϊʲô�����ܾ�һ������˵����
ʦ�������ڽ���������ƽ���ߣ���˭�ҵöࡣ
ʦ��ͬһ����·������������ʲôλ�ù�ϵ�����������������֮�� ����ľ �ij����кι�ϵ��������˵��ʲô��������ƽ����֮��Ŀ��ȱ��ֲ��䣩
2 �������ܻ�������ƽ�����أ��������Ǿ���ѧϰ���������ƽ���ߡ�
��ʦ��ѧ���ó����ǰ��ֱ�ߣ�������ʦһ����ƽ���ߡ�
������һ�����̶����ǰ壬��һ��ֱ�DZ�����һ��ֱ�ߡ�
��ʦ����ʾ���߹۲�ѧ����ͼ�������ע��ǿ����ʱֱ��һ�����ú����ǰ��Ȳ��ܶ���Ҫ�����ְ�ס���ǰ塣��ѧ����һ������Ϊʲô��
�����ڶ�������ֱ�߽������ǰ����һ��ֱ�DZߣ�Ȼ��̶�ֱ�ߣ�ƽ�����ǰ塣
ע��ǿ��ֱ�������ǰ��ֱ�DZ�Ҫ������Ȼ��סֱ�߲����ɶ����������ǰ�����ֱ�ߵķ���ƽ�ƣ�������ֱ�������ǰ��λ��Ҫ���ֽ���������Ϊʲô��
����������������һ��ֱ�DZ�������һ��ֱ�ߡ�
ע��ǿ������ʱ��Ҫ�����ֽ����ǰ�̶�ס��������λ������Ϊʲô��
ʾ����ɺ���ѧ�������ǰ��ֱ������ϰ���ϻ�����ƽ���ߡ���ʦѲ��ѧ����ͼ�ķ�������Ѳ�ӱ���ʾ��ͼ�IJ��衣Ҫע�⿴ѧ����ÿһ���������������δ����ȫ���յ�ѧ��Ҫ��ʱ���Ա�Ҫ��ָ����
����ѧ����ͼ����ָ�������ǻ�����������ƽ���ߵķ�����������ֱ���߶��Dz��ǻ���ƽ�С�
�� ������ϰ���������ϵ�56ҳ������
1�����һ��ƽ������
2 ��ֱ����һ����ֱ�ߵ�ƽ���ߡ�
3 �ֱ����p��q��ֱ�ߵ�ƽ����
ʦ��С� ����ֱ����һ�㣬����ֻ��һ��ֱ������ֱ֪��ƽ��
�������ֱ�߶��������ֱ��ƽ�У���ô������ֱ��Ҳ����ƽ��
�� ������ϰ
��֪ ������ABC������A��BC�ߵ�ƽ����
С���ڿ�ͬѧ��ѧ����Щ���ݣ��㻹����Щ���⣿���ƽ����������Щ�µ���ʶ��
�������
��ѧЧ���ķ�����
�ڶ���Ԫ ������Χ�Ŀ���
һ������
1�����ٶ���ǰ������ѧ�� ����ͨ��ʵ��ó��˿����� �� ��ɵĽ��ۣ����� Լռ�����������1/5�� Լռ�����������4/5��
2�������ɶ��ֳɷ���ɣ��� ������ijɷְ� ���㣬��Լ��
3�������������������� ��
4�����Ź�ҵ�ķ�չ���ŷŵ������е� �� �Կ����������Ⱦ����Ŀǰ���������Ⱦָ���������ĿΪ
��������
1��������һ�� ɫ ��ζ�����壬�����ܶȱȿ��� �� ����ˮ��Һ̬����̬������ɫ��
2����������ѧ���� ����������������Ӧ��������������Ӧ���ṩ ������ �ԡ�
3�����������ķ���
4��������֧���������ʷ���ȼ�գ���������ͬ����д����ѧ����ʽ��������
|
���� |
��ѧ����ʽ |
ʵ������ |
|
���� |
|
������ |
|
�� |
|
������ |
|
������ |
|
ľ̿ |
|
������ |
|
������ |
|
��˿ |
|
������ |
5��������Ӧ���� �����ݾ��ҳ̶Ȳ�ͬ�� ������
�������࣬���ǵ���Ҫ���� ����ͬ�� ����������ʵ���� ���ٳ�4�����ӣ� ��
[NextPage]
������ȡ����
1��ʵ���������������ַ�������1�� ����2��
��3�� ������ѧ����ʽ��ʾ����
2���ռ������� ��,��Ϊ ���������� ���ռ�������Ϊ ���� �ռ��������ϴ�����
3���������ʱ�Թܿڱ��� ��ԭ����
4���Թ���װ�������غ����Թܿڷ� ��Ϊ�˷�ֹ
5���ø������������������ˮ���ռ���������ȷ�IJ��������Ⱥ�˳��Ϊ
6��ʵ�����ֹͣ����ǰ���Ȱ� Ȼ�� ��������� �������ʹ�Թ����ѡ�www.xkb1.com
7�����������ķ������� ��ľ������ ����� ��֤�������Ѿ�������
8���������ص�
9������ȽϷֽⷴӦ�����Ϸ�Ӧ��
|
��Ӧ���� |
�μӷ�Ӧ���������� |
���ɵ��������� |
���� |
|
�ֽⷴӦ |
|
|
|
|
���Ϸ�Ӧ |
|
|
|
������Ԫ��Ȼ���ˮ
1����ˮ�ĵ��ʵ���У�ˮ������ ��Ӧ�������� �� ����Ӧ����ѧ����ʽ ����˵��ˮ���� ��ɵġ���������к��� Ԫ�ص����������� ����CO��Fe2O3���� ���� Ԫ����ɵĴ�������� ����H2��N2��O2���� ��
2��������һ�� ɫ�� ζ�� ����ˮ�����塣���п���������������������ʱ���ܷ��� ����˵�ȼ����ʱһ��Ҫ ������ȼ�յ���ѧ����ʽ ��������Ϊȼ�ϵ������ŵ� ��
3���������� �� �� ��С���ӹ��ɵģ����������� ���ɵģ�ˮ������ ���ɵģ����������� ���ɵģ�������������������� �α�� һ ��
4�����ӵĻ������ʣ���1�����ӵ� �� ����С����2�����������ڲ��� �ţ�����������£��������� ���˶����� ����3�����Ӽ��� ��
5�������DZ������� ����С���ӣ�ԭ���� �е���С���ӡ�����SO2��ѧ���ʵ���С������ ��ˮ����ѧ�仯�е���С������ ��
6������ѧ�仯�У� �ɷ֣� ���ɷ֡�
7��Ӳˮ�� ����ˮ�� ���������Ӳˮ����ˮ��Ӳˮ�����ķ��� ��
8������ˮ��Դ��һ����Ҫ ��һ����Ҫ ��
���ġ��嵥Ԫ ���ʹ��ɵİ��� ��ѧ����ʽ
һ�� ԭ�ӵĹ���
 1��̼Ԫ�ؿ�����ɲ�ͬ�ĵ��ʣ��� �� �� �ȡ����ǵ��������ʴ��ڲ����ԭ�� �� 1��̼Ԫ�ؿ�����ɲ�ͬ�ĵ��ʣ��� �� �� �ȡ����ǵ��������ʴ��ڲ����ԭ�� ��
2��������̼��һ����̼��ѧ���ʴ��ڲ����ԭ�� ��
3����1�����ʯ�������ò���������Ϊ������ ���������ʣ�
��2��ʯī�������Ƶ缫������Ϊ������ ���������ʣ�
��3������̿���� �Ľṹ����˿� ��ζ��ɫ�صȡ�
��4��C60���� ����ʡ����������Է�������= ��
4����1�����������̼�� �������� �����ʣ������� ��
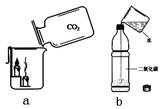
��2����ͼa����������̼���������ձ��У����� ��˵��������̼���� �� �����ʣ���˶�����̼������ ��
��3����ͼb����һ���ռ���������̼���ʵؽ���������ƿ�е���1/2�����ˮ����������ƿ�Dz������� ����˵��������̼���� �����ʡ�
��4��������̼��ʹ��ɫʯ����Һ��죬�������� ��Ե�ʣ���Ӧ����ѧ����ʽΪ ���¿�
[NextPage]
��� һ ��
��5��������̼��ʹ����ʯ��ˮ����ǣ�����Ϊ ��Ե�ʣ������Ӧ���������� ��ʯ��ɰ����שĨǽ���ι̾������������Ӧ���ɵ� ��һ�ּ�Ӳ�İ�ɫ���塣д���÷�Ӧ�ķ���ʽ ��
��6��������̼���ǹ�����õ�ԭ�ϣ����������ϴ������������Ӷ�����̼�ĺ������Դٽ� ���ã���� ������
5����1��һ����̼���� �ԣ���ȼ��ʱ����� ɫ��ͬʱ�ų������ȣ����CO������ ��
��ȼ���ж�����CO��
��2��CO��ԭ����ͭ���ֳ� �ԣ����CO������ұ����������������CO����������������Ҫ��Fe2O3��������ѧ����ʽ��ʾ ��
���������������Ͷ�����̼ʵ�����Ʒ��ıȽ�
1��ʵ��������ȡ����Ҫע��
��1��ͨ��ȷ����Ӧ��״̬�ͷ�Ӧ������ȷ�� װ�á�
��2��ѡ����ʵ���ȡװ�ã����� �� װ�á�
2�������������Ͷ�����̼ʵ�����Ʒ��ıȽ�
|
���� |
��Ӧԭ��������ʽ�� |
ʵ��װ��ͼ |
���鷽�� |
|
O2 |
|
�̹̼�����
��
��Һ������ |
|
|
CO2 |
|
��Һ������ |
|
|
H2 |
|
��Һ������ |
|
����������һ����̼��̼����ѧ���ʵ������ԵıȽϣ��÷���ʽ��ʾ��
|
���� |
��ѧ���ʵ����ƴ� |
|
���ƴ� |
�ٿ�ȼ�� |
�ڻ�ԭ�� |
|
���� |
|
|
|
̼ |
���ȼ�գ�
�����ȼ�գ� |
|
|
һ����̼ |
|
|
�ģ�����ЧӦ
��1����������ЧӦ������ , , , ��
��2����ֹ����ЧӦ�Ĵ�ʩ ��
��
��
���ߵ�Ԫ ȼ�ϼ�������
1��ȼ����ָ �� ������һ�� �� �ľ��ҵ� ��Ӧ��
2��ȼ�յ��������� ��
�� ��������������ͬʱ�߱���
3������ԭ������ ��
�� ����������ֻ��߱�һ����
4����ʯȼ�հ��� �� �� �������� ��Դ
���� ����������������
5�������� �� ����Ҫ�ɷ֣��ڿ�����ȼ�յ���ѧ����ʽ�� �������Ƿ��� ���ų� ������ ��ʹ����ʯ��ˮ����ǵ� ���塣
6��ʯ��Һ������̼�⻯����,������ѧʽΪC4H10,����ȼ�յ���ѧ����ʽ�� ��
7��úȼ��ʱ���ŷų� �� ����Ⱦ���Щ��������ˮ���γ� ��
8��CNG��ʾ ��LPG��ʾ ��
9���Ҵ��׳� �ڿ�����ȼ�յ���ѧ����ʽ�� ��
[NextPage]
10��������һ�� ��Դ��ȼ�յ���ѧ����ʽ�� ��ʵ������ȡ������ԭ���� ���ռ������� �� ��
�ڰ˵�Ԫ �����ͽ�������
1���������ϰ��� �� ��
2���������������ʣ�ͭΪ ɫ����Ϊ ɫ������������� ɫ�������£����� ΪҺ̬���������Ϊ��̬�����������Ϊ�Ⱥ͵���������壬����չ�ԣ��ܶȴ�ȡ�
3������֮��¿α��һ��
�ؿ��к�����ߵĽ���Ԫ�� �������к�����ߵĽ���Ԫ�� ��
�������ߵĽ����� �����硢������õĽ����� ��
�۵���ߵĽ����� ���۵���͵Ľ����� ��
4���Ͻ�ָ������ �м����ۺ�ijЩ �� ���Ƶõľ��� ������һЩ���ʣ����ĺϽ���� �� ���������� �������������������ߵ���Ҫ������ ��
5���Ͻ���������ǵĴ��������Ӳ�� ���۵� �� ����Ҳ���ã���˺Ͻ��и��㷺����;��21���͵���Ҫ���������� ��
6��������������Ӧ
��1����þ�������ķ�Ӧ�������£� ɫ��þ�ڿ����л��䰵������ ��������ȼʱ������ �⣬���� ����Ӧ����ѧ����ʽΪ ��
��2�������������ķ�Ӧ�����ڳ������ܺ�������Ӧ����һ�����ܵ� ������ѧʽ����Ĥ����ֹ����һ����������ˡ������кܺõ� ���䷴Ӧ����ѧ����ʽΪ ������������������� ����������������ϴ�� ����ܡ����ܡ�����ʱ��ʢ��ʳ���������ʡ�
��3�������������ķ�Ӧ�������£��� �Ŀ����У���������е� �� ��ͬ�������� ɫ�ıȽ����ɵ����ʡ������⣬����ѧʽΪ ���ڵ�ȼʱ�������� �о���ȼ�գ� ������ ɫ���壬�䷴Ӧ��ѧ����ʽΪ ��
��4����ͭ�������ķ�Ӧ�������£�ͭ�ڸ���Ŀ����м�������������Ӧ���ڼ���ʱͭ˿���������� ɫ���ʣ���Ӧ����ѧ����ʽΪ ��
��5����������»�����˵���� ����Ȼ����ڵĽ��������� �� ��
7������������Һ��Ӧ
|
���� |
��ϡ�ᷴӦ |
��ϡ�ᷴӦ |
|
þ |
|
|
|
п |
|
|
|
�� |
|
|
|
�� |
|
|
8������������Һ��Ӧ
|
ʵ����� |
���� |
��ѧ����ʽ |
|
Al+CuSO4 |
|
|
|
Cu+AgSO4 |
|
|
|
Fe+CuSO4 |
|
|
|
Cu+Al2(SO4)3 |
|
|
9���û���Ӧ�Ķ��� ��
10���������˳��
�ڽ������˳���������λ��Խ��ǰ���Ļ��Խ ��
�ڽ������˳���λ�� ǰ��Ľ��������û������ᡢϡ�����е� ��
�ڽ������˳���λ�� �����ܰ� ���������ǵĻ�������Һ���û�������
11������ԭ�������� �� ��Ӧ���� ����������ʯ�л�ԭ��������ʯ����ʽ ���Գ�����Ϊ������
12������������� ����ֹ��ʴ��ԭ�� �����巽���� �� �� ��
13������������Դ����Ч;�� �� ��
�� ��
|