| 黄冈市高三模拟考试理科综合 | ||||||||||||||
|
说明:本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分,满分300分。考试时间150分钟。 第Ⅰ卷 (选择题 共150分) 本卷共25题,每题6分,共150分。在下列各题的四个选项中,只有一个选项是符合题目要求的。 1.1998年,国家启动了天然林保护工程,天然林与人工林比较其最大的优势是 A.自动调节能力强 B.调节气候能力强 C.水土保持能力强 D.水源涵养能力强 2.生长素浓度对植物器官的影响有相同效果的一组是 A.根的向地性和茎的背地性 B.植物的向光性和顶端优势 C.茎的背地性和植物的向光性 D.根的向地性和带芽扦插生根 3.下列细胞结构中,有可能发生碱基配对行为的一组是 A.细胞核、线粒体、叶绿体、核糖体 B.线粒体、叶绿体、核糖体、高尔基体 C.细胞核、核糖体、中心体、高尔基体 D.细胞核、线粒体、核糖体、中心体 4.以美国为首的北约在1994至1995年对波黑的空袭以及1999年对南联盟的空袭中大量使用了贫铀弹。贫铀弹的使用,使生物体发生变异,导致人类癌症、白血病和新生儿畸形 的发生等。近几个月来,一些欧洲国家纷纷报道本国参加北约维和行动的士兵因患癌症等病死亡,并称之为“巴尔干综合症”。对以上现象的讨论,下列哪一项不合理 A.大多数基因突变是对生物体有害的 B.当射线作用于生殖细胞或发育的胚胎时,新生儿就可能产生畸形 C.射线引起的生物变异都将通过有性生殖遗传给下一代
5.有下列实验:①观察洋葱根尖细胞染色体 ②促进扦插枝条生根 ③使细胞失去活性,所用试剂依次是 A. 10%HCl溶液,10-4 mol/L秋水仙素,1.5%的NaCl溶液 B. 0.01g/mL醋酸洋红液,10-10 mol/L吲哚乙酸,10%HCl溶液 C. 0.01g/mL龙胆紫液,10-4 mol/L秋水仙素,0.5g/mL蔗糖溶液 D. 10%HCl溶液,10-10mol/L吲哚乙酸,10%的尿素溶液 6.吸烟有害身体健康,烟草中含有众多的对人体有害的物质,有一种称为尼古丁的剧毒物质,它的结构简式为:
A.结构中除H外的所有C、N原子同在一平面上 B.它的化学式为C10H13N2 C.它存在于植物细胞的液泡中 D.它存在于植物细胞的细胞核中 7.糖元是一种式量比淀粉更大的多糖,主要存在于肝脏和肌肉中,又被称为动物淀粉。下列有关糖元的叙述中正确的是 A.糖元与纤维素是同分异构体 B.糖元水解的最终产物是葡萄糖 C.糖元是还原性糖 D.糖元溶于水,有甜味 8.新华社1999年11月17日电,在兰州召开的一次能源地质国际研讨会上传出讯息:“可燃冰”是水与天然气相互作用形成的晶体物质,主要存在于冻土层和海底大陆架中;据测定每0.1 m3固体“可燃冰”要释放出20 m3的甲烷气体;由此可判断下列说法中不正确的是 A.“可燃冰”将成为人类新的后续能源 B.“可燃冰”是水变油,属于化学变化 C.“可燃冰”具有使用方便,清洁卫生等优点 D.我国青藏高原冻土层可能存在巨大体积的“可燃冰” 9.被称为“未来钢铁”的钛元素(Ti)有多种同位素,如 A.30 B.28 C.26 D.24 10.下列事实不能用勒沙特列原理解释的是 A.氨水应密闭保存,放置低温处 B.在硫酸亚铁溶液中,加入铁粉以防止氧化变质 C.生产硝酸的过程中使用过量空气以提高氨气的利用率 D.实验室常用排饱和食盐水的方法收集氯气 11.类推的思维方法在化学学习与研究中常会产生错误的结论。因此类推出的结论最终要经过实践的检验才能决定其正确与否。以下几种类推结论中,不正确的是 A.金属镁失火不能用二氧化碳灭火器扑灭;金属钠失火也不能用二氧化碳灭火 B. Fe3O4可以写成FeO·Fe2O3;Pb3O4也可以写成PbO·Pb2O3 C.不能用电解AlCl3溶液来制取金属铝;也不能用电解MgCl2溶液来制取金属镁 D.Fe与S直接化合可得到FeS;Al和S直接化合也可以得到Al2S3 12.能正确表示下列反应的离子方程式是
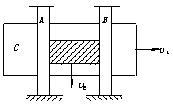
A.x=1 y=2 B.x=3 y=2 C.x=2y=3 D.x=2 y=4 14.有Na2CO3、AgNO3、BaCl2、HCl及NH4NO3五瓶无标签溶液,为鉴别它们,取四只试管分别装入一种溶液,再向上述四支试管中加入少许剩下的一种溶液,下列叙述错误的是 A.若三支试管出现沉淀时,则后加入的是AgNO3溶液 B.全部没有明显现象时,则后加的是NH4NO3溶液 C.一支试管出现气体,两支试管出现沉淀时,则后加入的是HCl溶液 D.若仅有两支试管出现沉淀时,则后加入的是BaCl2溶液 15.下列结构图中的大黑点代表原子序数从1到10的元素的原子实(原子实是原子除去最外层电子后剩余的部分),小黑点代表未用于形成共价键的最外层电子,短线代表价键。下列根据各图表示的结构特点,写出分子的化学式错误的是
A.①A为NH3 B.②为HCN C.③为C3H4O D.④为BF3 16.人体正常的血红蛋白中含有亚铁离子。若误食亚硝酸盐,则导致血红蛋白中亚铁离子转化为铁离子而中毒。服用维生素C可解除亚硝酸盐中毒。下列叙述中正确的是 A.亚硝酸盐是还原剂 B.维生素C是还原剂 C.维生素C能把亚铁离子氧化成三价铁离子 D.亚硝酸盐被氧化 17.正负电子对撞后湮灭成两个频率相同的光子。已知普朗克恒量是h,电子质量是m,电子电量为e,电磁波在真空中传播速度是c,则生成的光子在折射率为n的介质中传播时,其波长为 A. 18.构成等离子显示屏的等离子管发光,是通过高电压使低压氖氙气体原子的 A.自由电子周期性的运动而发光 B.外层电子受到激发而发光
19.将平面镜M斜放入一个装满清水的碗中,调整平面镜的倾斜角度,让一束太阳光斜射入水中经折射、反射、折射后射到PQ屏上,分为a、b、c三个光区,如图所示。现将三瓶相同的红藻放在三个光区,则(设其他光不进入这三个光区) A.在a光区的红藻生长得慢 B.在b光区的红藻生长得慢 C.在c光区的红藻生长得慢 D.在三个光区的红藻生长速度相同 20.为了测定某辆轿车在平直路上起动时的加速度(轿车起动时的运动可近似看作匀加速运动),某人拍摄了一张在同一底片上多次曝光的照片,如图所示。如果拍摄时每隔2 s曝光一次,轿车车身总长为4.5 m,那么这辆轿车的加速度约为 A. 1 m/s2 B. 2 m/s2 C. 3 m/s2 D.4 m/s2
21.如图所示,质量为m的物体放在水平放置的钢板C上,与钢板的动摩擦因数为μ,由 A.等于μmg B.大于μmg C.小于μmg D.不能确定 22.如图,在光滑的水平面上有一内、外壁都是光滑的气缸,
23.如图,两个面积足够大的金属板,平行竖直放置,间距为d,并接直流电压U。有一半径为R(2R<d)的绝缘金属球壳,放在两板中央,C、D为球壳水平直径上的两点,由于静电感应,关于金属球壳有以下说法: ①C、D两点电势相等,与球心O点电势差均为 ②C、D两点的场强相等,与球心O点场强均为零 ③球壳的感应电荷外壁带负电,内壁带正电 ④用手摸一下球壳,再移走金属板,球壳将带正电其中正确的说法是
24.如图所示为两列简谐横波在同一绳上传播时某时刻的波形图,则下列说法中正确的是 A.这两列波可能发生干涉现象 B.波甲的速度v1比波乙的速度v2大 C.波甲的速度v1与波乙的速度v2一样大 D.两列波波速的大小无法比较 25.在“用伏安法测干电池的电动势和内阻”实验中,通过改变滑线变阻器电阻大小,测量并记录多组端电压和相应电流值。某同学的实验数据如下表所示,与预想的实验结果不一致,由实验数据来分析,他所连接的电路可能是下列电路图中的
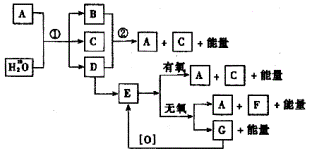
第Ⅱ卷 (非选择题 共150分) 本卷可能用到的相对原子质量有:H—1 O—16 C—12 S—32 P—31 F—19 Cu—63.5 26.(16分)A、B、C是人们熟悉的与生命运动密切相关的三种无机物,D、E、F、G是常见的有机物。七种物质间在一定条件下有如下关系:
(1)实现反应①的化学方程式为: (2)在工业上常用D作还原剂。其有关反应的离子方程式为: 。 (3)工业上用二种方法大规模生产F的化学方程式为: 。 (4)指出实现反应②的生物学意义是: 27.(20分)蚂蚁等群居性昆虫在找到食物后的归巢途中,用一种自身分泌物涂布在土地上,为其他的蚂蚁觅食引路,这种分泌物叫跟踪激素,其化学成分为拢牛儿醇,又称香叶醇,是一种液态的不饱和醇,其元素分析结果为:C 77.87%,H 11.75%,O 10.38%,分子量为154。将此激素先与臭氧反应,生成臭氧化物;再与水和金属锌反应,发生水解。结果得到下列三种水解产物(其物质的量之比为1∶1∶1):CH3COCH3、CH2OHCHO、 CH3CO(CH2)2CHO。
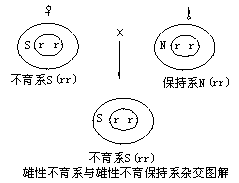
已知: (1)写出上述跟踪激素的分子式 ; (2)写出上述跟踪激素的结构简式: 或 ; (3)这种跟踪激素是蚂蚁体表腺体分泌的,是信息激素中的一种,信息激素的作用是 ; (4)昆虫体内天然激素的产量很微少,因此,目前已能人工合成昆虫激素的类似物,这些物质可以用于 和 。 (5)青菜种植过程中叶片易受到“菜青虫”的蚕食,农民常用喷洒农药的方法杀灭“菜青虫”。但这样的青菜农药残留高,有的在喷药后的三个月内食用还可引起中毒,甚至危及生命。 请用所学知识给出解决“菜青虫”问题的两种方法,并说明理由: 方法一: 优点: 方法二: 优点: 28.(14分)袁隆平被称为“杂交水稻之父”,他研究成功的水稻杂交技术为我国水稻产量的提高,做出了巨大的贡献,被誉为农业上的一次绿色革命。他因此而获得了我国的最高科学技术奖。 水稻杂交技术利用了植物的“雄性不育”。植物为什么会发生雄性不育现象呢?研究表明,小麦、水稻和玉米等作物,它们的雄蕊是否可育,是由细胞核和细胞质中的基因共同决定的。在细胞核和细胞质中,都含有决定雄蕊是否可育的基因。其中,细胞核的不育基因用r表示,可育基因用R表示,并且R对r为显性;细胞质的不育基因用S表示,可育基因用N表示。在上述四种基因的关系中,细胞核可育基因(R)能够抑制细胞质不育基因(S)的表达。因此,当细胞核可育基因(R)存在时,植株都表现为雄性可育。当细胞质基因为可育基因(N)时,无论细胞核具有可育基因还是不育基因,植株都表现为雄性可育。只有当细胞核不育基因(rr)与细胞质不育基因(S)同时存在时,植株才能表现为雄性不育。用基因型为N(rr)的品种作为父本,与基因型为S(rr)的雄性不育系杂交,杂交后代的基因型就是S(rr),表现为雄性不育。这里,基因型为N(rr)的品种,既能使母本结实,又使后代保持了不育的特性,因此叫做雄性不育保持系(简称保持系)。见图解。
用基因型为N(RR)的品种作父本,基因型为S(rr)的雄性不育系杂交,才能使后代恢复可育性。这种能够使雄性不育系的后代恢复可育性的品种,叫做雄性不育恢复系(简称恢复系)。用这样的种子在田间大面积播种,长成的植株既可以通过传粉而结实,又可以在各方面表现出较强的优势。在杂交育种中,雄性不育系、雄性不育保持系和雄性不育恢复系必须配套使用。这就是人们常说的三系配套。 袁隆平成功了,但他没有止步,在“三系法”的基础上,又研究成功了“二系法”,最后向“一系法”冲击。…… 阅读以上资料,分析回答下列问题: (1)画出水稻雄性可育的三种以上基因图解。
(2)画出雄性不育系和雄性不育恢复系的杂交图解。 (3)生产上使用的杂交水稻其基因组成是 29.(16分)铜与浓硝酸反应和铜与稀硝酸反应,产物不同,实验现象也不 (1)某课外活动小组为了证明并观察到铜与稀硝酸反应的产物为NO,设计了如图所示的实验装置。请你根据他们的思路,选择下列药品,完成该实验,并叙述实验步骤。 药品:稀硝酸、稀盐酸、Zn粒、CaCO3固体 步骤:①检查装置的气密性; ② ③ ④ ⑤ ⑥用注射器向广口瓶内推入氧气(或空气) (2)推入氧气或空气的目的是 (3)分别将等质量的铜片与等体积均过量的浓硝酸、稀硝酸反应,所得到的溶液前者呈绿色,后者呈蓝色,某同学提出这可能是Cu2+浓度差异反应的,你同意这种看法吗? (填“同意”或“不同意”),原因是 ;另一同学提出溶液呈“绿色”是Cu2+与NO2混合的结果,请你设计一个实验证明之(简述实验方案和实验现象) 。 30.(14分)白色粉末A由Na2S、Na2S2O3、Na2SO3、NaCl物质中的三种混合而成,取一定量的A样品投入100 mL2.2 mol/L的盐酸中,充分反应后过滤,最终得到100 mL pH=0的溶液,将此溶液蒸干,可得到8.19 g纯净物B。 (1)B的化学式为 。 (2)原混合物A中是否含有NaCl 。 (3)粉末A的组成可能是(有几种写几种) Ⅰ: Ⅱ: Ⅲ: Ⅳ: (4)生成沉淀最多的组合是(填序号) 。 31.(16分)关于卤族元素的碘及碘化氢 (1)碘化氢不稳定,怎样用简单的方法证明碘化氢的分解产物碘的存在?
(3)如果将结构简单的碘化氢(HI)分子想象为键的两端有两个离子,如同将两个不同质量的物体在弹簧两端振动的情况一样(如图所示)。假若在此模型中能够忽略碘离子的运动。 a.设氢离子的质量为M(H+),键的劲度系数为k,氢离子偏离平衡位置的位移为x,则氢离子运动的加速度a= 。 b.在振动过程中,氢离子能量 ,碘化氢分子能量 (选填“守恒”或“不守恒”) c.当电磁波通过碘化氢气体时,发现一平均波长为4.6×10-6 m吸收带,试计算被吸收的电磁波的平均频率 32.(本题包括两小题,共19分) (1)(9分)科学家发现太空中的γ射线都是从很远的星球发射出现的。当γ射线爆发时,在数秒钟内所产生的能量,相当于太阳在过去一百亿年内所发出的能量的总和的一千倍左右,大致相当于太阳质量全部亏损得到的能量。科学家利用超级计算机对γ射线的爆发状态进行了模拟,发现γ射线爆发是起源于一个垂死的星球“坍塌”过程,只有星球“坍塌”时,才能释放这么巨大的能量。已知太阳光照射到地球所需时间为t,地球公转周期为T,真空中的光速为c,万有引力恒量为G,试推算出一次γ射线爆发所产生的能量。 (2)(10分)要测出一个未知电阻的阻值Rx,现有如下器材:读数不准的电流计A、定值电阻R0、电阻箱R1、滑动变阻器R2、单刀单掷开关S1、单刀双掷开关S2、电源和若干根导线。①在图中画出实验电路图,并在图上标出所选用器材的代码。②写出主要的实验操作步骤及Rx的表达式。
(1)导体棒做匀速运动时的速度,要求用两种方法求解,并说明两种解法所依据的主要理由。 (2)导体棒从开始下滑到刚开始匀速运动这一过程中,导体棒的有效电阻消耗的电功。 (sin37°=0.6,cos37°=0.8,g=10 m/s2) |
教育最重要的是使人变得更聪明。教育就是要开启人的心智,使人身体好,更主动、积极,行动能力强,更能干。
中文域名: 古今中外.com
英文域名: www.1-123.com
丰富实用的教育教学资料
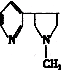 是一种
是一种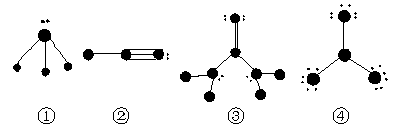
 C.内层电子受到激发而发光 D.原子核受到激发而发光
C.内层电子受到激发而发光 D.原子核受到激发而发光
 于光滑导槽A、B控制,物体只能沿水平导轨运动,现使钢板以速度v1向右运动,同时用力F拉动物体(F的方向沿导槽的方向)使物体以速度v2沿导槽运动,则F的大小为
于光滑导槽A、B控制,物体只能沿水平导轨运动,现使钢板以速度v1向右运动,同时用力F拉动物体(F的方向沿导槽的方向)使物体以速度v2沿导槽运动,则F的大小为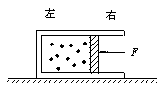 气缸的质量为M,气缸内有一质量为m(m<M)的活塞,密封一部分
气缸的质量为M,气缸内有一质量为m(m<M)的活塞,密封一部分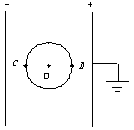 A.p1=p2 B.p1<p2 C.V1>V2 D.V1<V2
A.p1=p2 B.p1<p2 C.V1>V2 D.V1<V2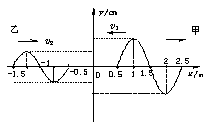 A.①②③ B.②④ C.② D.④
A.①②③ B.②④ C.② D.④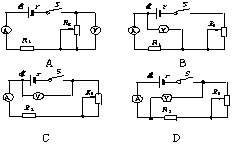
 已知:
已知: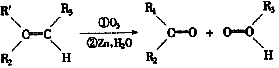

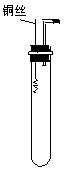 同。
同。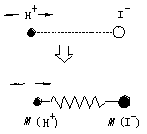 (2)碘化氢与硝酸银溶液反应的产物之一具有感光性,试写出其见光分解的
(2)碘化氢与硝酸银溶液反应的产物之一具有感光性,试写出其见光分解的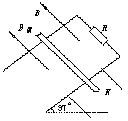
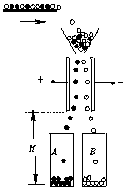 33.(16分)如图所示是静电分选器的原理示意图,将磷酸盐和石英的混合颗粒由传送带送至两个竖直的带电平行板上方,颗粒经漏斗从电场区域中央处开始下落,经分选后的颗粒分别装入A、B桶中,混合颗粒离开漏斗进入电场时磷酸盐颗粒带正电,石英颗粒带负电,所有颗粒所带的电量与质量之比均为10-5C/kg。若已知两板间的距离为10cm,两板的竖直高度为50 cm。设颗粒进入电场时的初速度为零,颗粒间相互作用不计。如果要求两种颗粒离开两极板间的电场区域时有最大的偏转量且又恰好不接触到极板。(1)两极板间所加的电压应多大?(2)若带电平行板的下端距A、B桶底高度为H=1.3m,求颗粒落至桶底时速度的大小。(g=10 m/s2)
33.(16分)如图所示是静电分选器的原理示意图,将磷酸盐和石英的混合颗粒由传送带送至两个竖直的带电平行板上方,颗粒经漏斗从电场区域中央处开始下落,经分选后的颗粒分别装入A、B桶中,混合颗粒离开漏斗进入电场时磷酸盐颗粒带正电,石英颗粒带负电,所有颗粒所带的电量与质量之比均为10-5C/kg。若已知两板间的距离为10cm,两板的竖直高度为50 cm。设颗粒进入电场时的初速度为零,颗粒间相互作用不计。如果要求两种颗粒离开两极板间的电场区域时有最大的偏转量且又恰好不接触到极板。(1)两极板间所加的电压应多大?(2)若带电平行板的下端距A、B桶底高度为H=1.3m,求颗粒落至桶底时速度的大小。(g=10 m/s2) 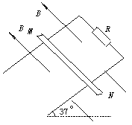 34.(19分)如图所示,足够长的U形导体框架的宽度L=1.0 m,电阻忽略不计,其所在平面与水平面成α=37°角,磁感强度B=1.0T的匀强磁场方向垂直于导体框平面,一根质量为m=1.0kg,有效电阻r=1.0Ω的导体棒MN垂直跨放在U形框架上,框架上端接有一阻值R=1.0Ω的定值电阻。该导体棒与框架间的动摩擦因数μ=0.5,导体棒由静止开始沿框架下滑到刚开始匀速运动时(导体棒运动时始终与框架紧密接触),通过导体棒截面的电量共为Q=3.0 C,求:
34.(19分)如图所示,足够长的U形导体框架的宽度L=1.0 m,电阻忽略不计,其所在平面与水平面成α=37°角,磁感强度B=1.0T的匀强磁场方向垂直于导体框平面,一根质量为m=1.0kg,有效电阻r=1.0Ω的导体棒MN垂直跨放在U形框架上,框架上端接有一阻值R=1.0Ω的定值电阻。该导体棒与框架间的动摩擦因数μ=0.5,导体棒由静止开始沿框架下滑到刚开始匀速运动时(导体棒运动时始终与框架紧密接触),通过导体棒截面的电量共为Q=3.0 C,求: