理科综合能力测试(十四)
本试卷分第Ⅰ卷(选择题)和第Ⅱ卷两部分,共300分,考试用时150分钟。
相对原子质量: H1 C12 016 Na23 P 31
第Ⅰ卷
(选择题共21题每题6分共126分)
注重事项:
1.答第Ⅰ卷前,考生务必将自己的姓名、准考号、科目涂写在答题卡上,并在规定位置粘贴考试用条形码。
2.每小题选出答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡皮擦干净后,再选涂其他答案标号。答在试卷上的无效。
在下列各题的四个选项中,只有一个选项是最符合题目要求的。
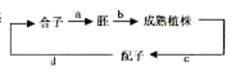 1.右图是自然界豌豆的生殖周期示意图,下列有关叙述正确的是
1.右图是自然界豌豆的生殖周期示意图,下列有关叙述正确的是
A.a过程需要的营养物质由子叶提供
B.b过程中有机物的重量一直持续增加
C.基因重组过程可以发生在c过程
D.在d过程中来自精子和卵细胞的同源染色体联会配对
2.下面对体液免疫和细胞免疫异同的表述,不正确的是
A.体液免疫中抗体和抗原发生特异性结合,发挥免疫效应
B.效应淋巴细胞都来自骨髓造血干细胞,都在骨髓中分化、发育成熟
C.体液免疫和细胞免疫的效应淋巴细胞中遗传物质一般未改变,而mRNA种类不同
D.细胞免疫中,效应 T细胞的攻击目标是已经被抗原入侵了的宿主细胞
3.下图为脉孢霉体内精氨酸的合成途径示意图。从图中不可能得出
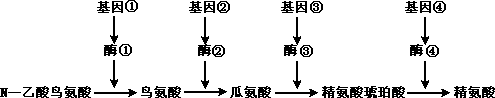
A.精氨酸的合成是由多对基因共同控制的 B.基因可通过控制酶的合成来控制代谢
C.若产生的鸟氨酸依靠突变型脉孢霉,则可能是基因①发生突变
D.若基因②不表达,则基因③和④也不表达
4.突变和基因重组产生了生物进化的原始材料,现代生物技术是利用这一原理来改变生物遗传性状,以达到人们所期望的目的。下列有关叙述中,错误的是
A.转基因技术造成的变异,实质上相当于人为的基因重组,但却导致了自然界没有的定向变异产生东烟台 孙芸廷 整理
B.体细胞杂交技术是人为造成染色体变异的方法,它突破了自然生殖隔离的限制
C.人工诱变没有改变突变的本质,但却因突变率的提高而实现了定向变异
D.经过现代生物技术的改造和人工选择的作用,许多生物变得更适合人们的需要
5.下列实例中涉及DNA分子杂交原理的是
①用DNA分子探针诊断疾病 ②利用植物体细胞杂交技术培育出杂种植株
③快速灵敏地检测饮用水中病毒的含量 ④利用大肠杆菌发酵生产人体胰岛素
A.①②③④ B.①③ C.①③④ D.①②④
6.一个患血友病的女子和一个正常男子结婚,生了一个性染色体组成为XXY的无血友病儿子,这种情况的出现是由于以下哪一过程不正常所造成的
A.精子形成、减数第一次分裂 B.精子形成、减数第二次分裂
C.卵细胞形成、减数第一次分裂 D.卵细胞形成、减数第二次分裂
7.有编号为1、2、3、4的四瓶无色液体,仅知道是1%酚酞、0.1mol/LNaOH溶液、0.1mol/L盐酸和0.1mol/LNaCl溶液,现要求甲、乙、丙、丁四位学生进行鉴别,而且每人只鉴别两瓶溶液,告诉学生鉴别两瓶溶液都正确得满分,只有一瓶正确可以及格。四位学生的鉴别结果如下:正确的结论是
甲
1号为0.1mol/L盐酸
4号为0.1mol/LNaCl溶液
老师评价:四位学生都及格,但是没有一个得满分。
乙
1号为0.1mol/LNaOH溶液
3号为0.1mol/L盐酸
丙
1号为1%酚酞
2号为0.1mol/L盐酸
丁
4号为0.1mol/L盐酸
2号为NaOH溶液
A.3号为0.1mol/LNaOH溶液 B.2号为0.1mol/LNaCl溶液
C.1号为1%酚酞 D.4号为0.1mol/L盐酸
8.一定条件下,体积为10L的密闭容器中,1molX和1molY进行反应:
2X(g)+Y(g)错误!嵌入对象无效。Z(g),经60s达到平衡,生成0.3molZ。下列说法正确的是
A.以X浓度变化表示的反应速率为0.001mol/(L·S)
B.将容器体积变为20L,Z的平衡浓度变为原来的 ![]()
C.若增大压强,则物质Y的转化率减小
D.若升高温度,X的体积分数增大,则该反应的△H>0
9.常温下,0.1mol·L-1某一元酸(HA)溶液中c(OH-)/c(H+)=1×10-8,下列叙述正确的是
A.该溶液中由水电离出的c(H+)=1×10-12mol·L-1
B.由pH=3的HA与pH=11的NaOH溶液等体积混合,溶液中c(Na+)>c(Ac—)>c(OH―)>c(H+)
C.浓度均为0.1mol/L的HA和NaA溶液等体积混合后,若溶液呈酸性,则
c(A-)>c(HA)>c(Na+)>c(H+)>c(OH-)
D.0.1mol·L-1HA溶液与0.05mol·L-1NaOH溶液等体积混合后所得溶液2c(H+)+c(HA)=c(A-)+2c(OH-)
10.下列有关叙述中正确的是
A.液态氟化氢中存在氢键,所以其分子比氯化氢更稳定
B.由碳、氮原子形成的化合物比金刚石坚硬,其主要原因是碳氮键比碳碳键更短
C.HD和NO2都是共价化合物,NH4Cl和CaC2都是离子化合物
D.若ⅡA某元素的原子序数为m,则同周期ⅢA元素的原子序数有可能为m 10
11.NA代表阿伏加德罗常数的值,下列叙述不合理的是
A.常温常压下,22.4 L N2所含的分子数小于NA
B.在含有1mol CH3COO-的醋酸钠溶液中, Na+数目略大于NA
C.8.0 g Cu2S和CuO的混合物中含有铜原子数为0.1NA
D.0.1mol Fe 与0.1mol Cl2充分反应,转移的电子数为0.3 NA
|
20 |
|
22 |
|
24 |
|
26 |
|
28 |
|
30 |
|
0 |
|
10 |
|
20 |
|
30 |
|
40 |
|
50 |
|
V1 / mL |
|
温度 / ℃ |
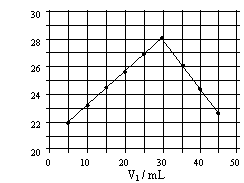 12.将V1mL1.0mol/L HCl溶液和V2mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如右图所示(实验中始终保持V1+V2=50mL)。下列叙述正确的是
12.将V1mL1.0mol/L HCl溶液和V2mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如右图所示(实验中始终保持V1+V2=50mL)。下列叙述正确的是
A 做该实验时环境温度为22℃
B 该实验表明化学能可能转化为热能
C NaOH溶液的浓度约为1.0mol/L
D 该实验表明有水生成的反应都是放热反应
13.三氧化二镍(Ni2O3)可用于制造高能电池,其电解法制备过程如下:用NaOH调NiCl2溶液pH至7.5,加放适量硫酸钠后进行电解。电解过程中产生的Cl2在弱碱性条件下生成ClO-,把二价镍氧化为三价镍。以下说法正确的是
A 可用铁作阳极材料 B 电解过程中阳极四周溶液的pH升高
C 阳极反应方程式为:2Cl--2e-=Cl2
D 1mol二价镍全部转化为三价镍时,外电路中通过了2mol电子。
14.2005年2月16日《京都议定书》正式生效,这是人类历史上首次依法规定限制温室气体排放,地球的大气层中,基本不变的成分为氧气、氮气、氢气等,占大气总量的99.96%,可变气体成分主要有二氧化碳(CO2)、水蒸气和臭氧等,这些气体的含量很少,但对大气物理状况影响却很大,据研究:人类燃烧矿物燃料放出大量CO2,使大气中的CO2浓度不断增大,是导致“温室效应”的主要原因,即使大气平均温度上升,从而导致一系列生态环境问题,由此可判定:CO2比大气中的氧气、氮气、氢气等基本不变的气体成分
 A、对可见光的吸收作用强 B、对无线电波的吸收作用强
A、对可见光的吸收作用强 B、对无线电波的吸收作用强
C、对紫外线的吸收作用强 D、对红外线的吸收作用强
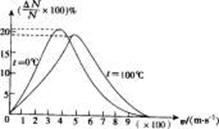
15.如图是氧气分子在不同温度(0℃和100℃)下的速率分布,由图可得信息( )
A、同一温度下氧分子呈现出“中间多两头少”的分布规律
B、随着温度的升高,每一个氧气分子的速率都增大
C、随着温度的升高,氧气分子中速率小的分子所占的比例高
D、随着温度的升高,氧气分子的平均速率变小
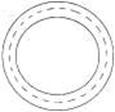 16.为了科学研究的需要,经常将质子(
16.为了科学研究的需要,经常将质子( ![]() )和α粒子(
)和α粒子( ![]() )等带电粒子贮存在圆环状空腔中,圆环状空腔置于一个与圆环平面垂直的匀强磁场(偏转磁场)中,磁感应强度为 B、假如质子和α粒子在空腔中做圆周运动的轨迹相同(如图中虚线所示),偏转磁场也相同.比较质子和α粒子在圆环状空腔中运动的动能EH和Eα,运动的周期TH和Tα的大小,有
)等带电粒子贮存在圆环状空腔中,圆环状空腔置于一个与圆环平面垂直的匀强磁场(偏转磁场)中,磁感应强度为 B、假如质子和α粒子在空腔中做圆周运动的轨迹相同(如图中虚线所示),偏转磁场也相同.比较质子和α粒子在圆环状空腔中运动的动能EH和Eα,运动的周期TH和Tα的大小,有
A.EH=Eα,TH≠Tα B.EH=Eα,TH=Tα
C.EH≠Eα,TH≠Tα D.EH≠Eα,TH=Tα
17.如图所示,真空中一半径为R、质量分布均匀的玻璃球,频率为v的细激光束在真空中沿直线BC传播,于玻璃球表面的C点经折射进入小球,并在玻璃球表面的D点又经折射进入真空中,已知∠COD=120°,玻璃球对该激光的折射率为 ![]() ,则下列说法中正确的是( )
,则下列说法中正确的是( )
A.激光束在C点的入射角α=30°
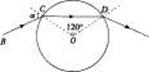 B.此激光束在玻璃中穿越的时间为t=
B.此激光束在玻璃中穿越的时间为t= ![]() (其中c为光在真空中的传播速度)
(其中c为光在真空中的传播速度)
C.一个光子在穿过玻璃球的过程中能量逐渐变小
D.改变入射角α的大小,细激光束可能在球表面C处发生全反射
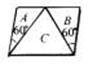 18.如图所示,某长方形板状物体被锯成A、B、C三块,然后再拼在一起,放在光滑的水平面上,各块质量分别为MA=MB=1kg,MC=2kg,现以10N的水平推力F沿对称轴方向推C,使A、B、C三块保持矩形整体沿力的方向平动,在运动过程中,C对A作用的摩擦力大小为( )
18.如图所示,某长方形板状物体被锯成A、B、C三块,然后再拼在一起,放在光滑的水平面上,各块质量分别为MA=MB=1kg,MC=2kg,现以10N的水平推力F沿对称轴方向推C,使A、B、C三块保持矩形整体沿力的方向平动,在运动过程中,C对A作用的摩擦力大小为( )
A.10N B.2.17N C.2.5N D.1.25N
19.原子核自发地放出电子的现象称为β衰变.开始时科学家曾认为β衰变中只放出电子(即β粒子),后来发现,这个过程中除了放出电子外,还放出一种叫作“反中微子”的粒子.反中微子不带电,与其他物质的相互作用极弱.下面关于β衰变的说法正确的是
 A、静止的原子核发生β衰变时,β粒子与衰变后的核的运动速度方向一定相反
A、静止的原子核发生β衰变时,β粒子与衰变后的核的运动速度方向一定相反
B、原子核发生β衰变时,放出的能量等于β粒子与衰变后的核的动能之和
C、原子核能发生β衰变,说明原子核内含有电子
D、发生β衰变后的原子核的核子数不变,但带电量增加
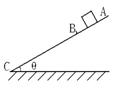
20.如图斜面ABC,AB段是光滑的,BC段有摩擦.某物体从A点由静止开始下滑,当滑至C点时恰好停止,则下列说法正确的是:
A.BC段的长度总大于AB段,但BC段的摩擦系数越大时,BC段的长度越接近AB段的长度
B.BC段的长度总大于AB段,但BC段的摩擦系数越小时,BC段的长度越接近AB段的长度
C.在θ角小到一定值时,只要BC段的摩擦系数适当,AB段的长度可以大于BC段的长度
D.θ=30°时,选择适当的摩擦因数,可使得AB的长度大于BC段的长度
21.如图所示,空间有一垂直纸面的磁感应强度为0.5T的匀强磁场,一质量为0.2kg且足够长的绝缘木板静止在光滑水平面上,在木板左端无初速放置一质量为0.1kg、电荷量q= 0.2C的滑块,滑块与绝缘木板之间动摩擦因数为0.5,滑块受到的最大静摩擦力可认为等于滑动摩擦力。现对木板施加方向水平向左,大小为0.6N恒力,g取10m/s2.则( )
A.木板和滑块一直做加速度为2m/s2的匀加速运动
B.滑块开始做匀加速直线运动,然后做加速度减小的变加速运动,最后做匀速运动
C.最终木板做加速度为2 m/s2的匀加速运动,滑块做速度为10m/s的匀速运动
D.最终木板做加速度为3 m/s2的匀加速运动,滑块做速度为10m/s的匀速运动
|
班级________________________姓名_____________________________准考证号______________________________________ |

 绝密★启用前
绝密★启用前
 2009年普通高等学校招生全国统一考试(南开中学模拟卷)
2009年普通高等学校招生全国统一考试(南开中学模拟卷)
理科综合能力测试(十四)
第Ⅱ卷
(共10题共174分)
注重事项:
1.答卷前将密封线内的项目填写清楚。
2.用钢笔或圆珠笔直接答在试卷上。
22.(1)物体因绕轴转动而具有的动能叫转动动能,转动动能的大小 与物体转动的角速度有关.为了研究某一砂轮的转动动能Ek与角速度ω的关系,某同学采用了下述实验方法进行探索:先让砂轮由动力带动匀速旋转测得其角速度ω,然后让砂轮脱离动力,由于克服转轴间摩擦力做功,砂轮最后停下,测出砂轮脱离动力到停止转动的圈数n,通过分析实验数据,得出结论.经实验测得的几组ω和n如下表所示:另外已测得砂轮转轴的直径为1cm,转轴间的摩擦力为10/π N.
①计算出砂轮每次脱离动力的转动动能,并填入上表中.
②由上述数据推导出该砂轮的转动动能Ek与角速度ω的关系式为 。
③若测得脱离动力后砂轮的角速度为2.5rad/s,则它转过45圈时的角速度为 rad/s.
 |
(2)(4分)以下是一些有关高中物理力学实验的描述,其中正确的是 。(填写正确的序号)
A.在“研究匀变速直线运动”实验中,应该先释放小车,让其运动稳定后,再接通电源,让打点计时器在纸带上打下一系列的点。
B.在“验证力的平行四边形定则”实验中拉橡皮筋的细绳要稍长,并且实验时要使弹簧与木板平面平行。
C.在“用单摆测定重力加速度”实验中,假如摆长测量无误,但测得的g 值偏小,其原因可能是将全振动的次数n误计为n-1。
D.在“验证机械守恒定律”的实验中,需要用天平测物体(重锤)的质量。
E.在“验证动量守恒定律”的实验中,入射小球的质量应该大于被碰小球的质量。
F.在“研究平抛物体的运动”的实验中,每次应使小球从斜槽的不同位置自由滚下。
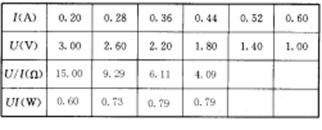
(3)(12分)电源的输出功率P跟外电路的电阻R有关。下左图是研究它们的关系的实验电路。为了便于进行实验和保护蓄电地,给蓄电池串联了一个定值电阻R0,把它们一起看作电源(图中虚线框内部分)。于是电源的内电阻就是蓄电池的内电阻和定值电阻R0之和,用r表示。电源的电动势用E表示。
= 1 \* GB3 ①写出电源的输出功率P跟E、r、R的关系式: 。(电流表与电压表都看作理想电表)
= 2 \* GB3 ②在下右图的实物图中按照下左图画出连线,组成实验电路。
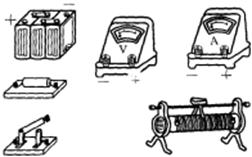
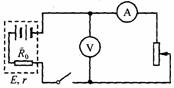
= 3 \* GB3 ③下表中给出了6组实验数据,根据这些数据。在图中的方格纸中画出P-R关系图线.根据图线可知,电源输出功率的最大值是_____________W,当时对应 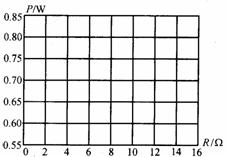 的外电阻是__________Ω。
的外电阻是__________Ω。
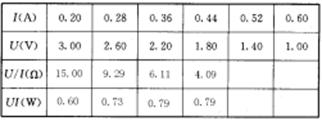
= 4 \* GB3 ④由表中所给出的数据,若已知跟电源串联的定值电阻的阻值为R0=4.5Ω,还可以求得该电源的电动势E = _________V,内电阻r0 = __________Ω.
23.(16分)计划发射一颗距离地面高度为地球半径R0的圆形轨道地球卫星,卫星轨道平面与赤道片面重合,已知地球表面重力加速度为g,
(1)求出卫星绕地心运动周期T.
(2)设地球自转周期T0,该卫星绕地旋转方向与地球自转方向相同,则在赤道上一点的人能连续看到该卫星的时间是多少?
24.(19分)如图所示,光滑水平面上有一质量M=4.0kg的平板车,车的上表面是一段长L=1.0m的粗糙水平轨道,水平轨道左侧连一半径R=0.25m的1/4光滑圆弧轨道,圆弧轨道与水平轨道在0’点相切.车右端固定一个尺寸可以忽略、处于锁定状态的压缩弹簧,一质量m=1.0kg的小物块紧靠弹簧放置,小物块与水平轨道间的动摩擦因数μ=0.5.整个装置处于静止状态.现将弹簧解除锁定,小物块被弹出,恰能到达圆弧轨道的最高点A.取g=10m/s2.求:
(1)解除锁定前弹簧的弹性势能;(6分)
(2)小物块第二次经过0’点时的速度大小;(6分)
(3)小物块与车最终相对静止时距O,点的距离.(7分)

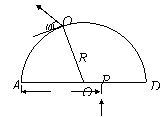
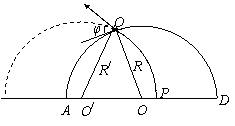
25.在半径为R的半圆形区域中有一匀强磁场,磁场的方向垂直于纸面,磁感应强度为B。一质量为m,带有电量q的粒子以一定的速度沿垂直于半圆直径AD方向经P点(AP=d)射入磁场(不计重力影响)。⑴假如粒子恰好从A点射出磁场,求入射粒子的速度。
⑵假如粒子经纸面内Q点从磁场中射出,出射方向与半圆在Q点切线方向的夹角为φ(如图)。求入射粒子的速度。
|
R |
|
A |
|
O |
|
P |
|
D |
|
Q |
|
φ |
|
加热 |
|
Y溶液 |
|
G↑ |
|
④+NaOH溶液 |
|
D↑ |
|
E↑ |
|
高温 |
|
水 |
|
F |
|
⑤+D |
|
G↑ |
|
D↑ |
|
J↑ |
|
J↑ |
|
② |
|
O2↑ |
|
M |
|
R |
|
E↑ |
|
① |
|
B |
|
C |
|
A↑ |
|
1400~1800℃ |
|
冰晶石 |
|
1000℃熔融电解 |
|
⑧+E↑ |
|
高温、催化剂 |
|
⑥+水 |
|
高温高压催化剂 |
|
⑦ |
|
适宜 条件 |
|
③+水 |
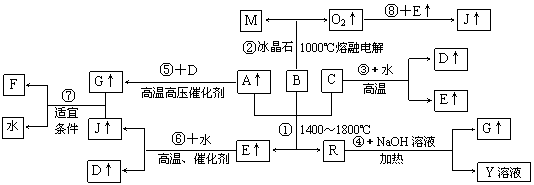 |
26.(16分)下图涉及多种无机化工反应,其中R是一种新型无机材料,M是一种应用广泛的金属材料,F为尿素[CO(NH2)2],A、C、D、M均为常见元素的单质,“↑”表示该物质常温下是气体,反应G+J→F+H2O中G与J的最佳配比为2∶1,向Y溶液中通入足量的J气体时可得到一种白色胶状沉淀,将该白色胶状沉淀滤出洗净后加热分解可以得到B。
⑴试写出B的化学式:_________________,J的电子式_____________。
⑵反应①的化学方程式为___________________________________________。
⑶反应④的离子方程式为___________________________________________。
⑷上述反应中属于非氧化还原反应的有_____________(填写相应反应的序号)。
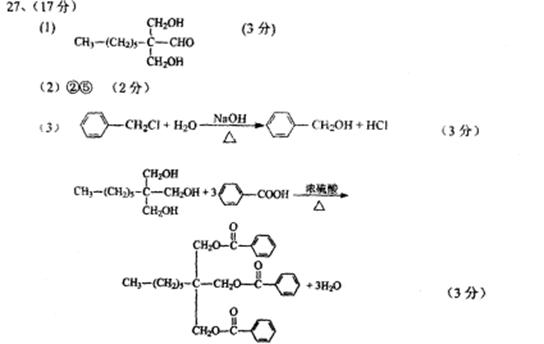
27.(17分)一种用于治疗高血脂的新药灭脂灵是按如下路线合成的:
已知:
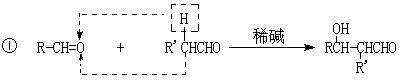
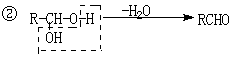
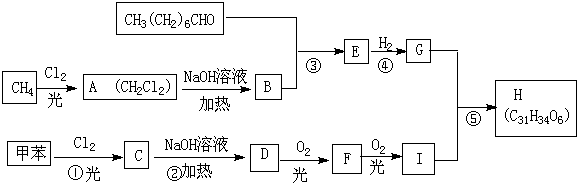
已知G的分子式为C10H22O3,试回答:
(1)写出结构简式:B E ;
(2)上述反应中属于取代反应的是 (填序号);
(3)写出反应方程式:
Ⅰ、反应② ;
Ⅱ、反应⑤ ;
Ⅲ、F与银氨溶液反应: 。
28.(18分)如图是某研究性学习小组设计制取氯气并以氯气为原料进行待定反应的装置
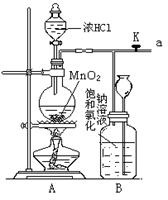
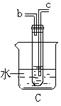
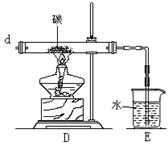
(1) 要将C装置接入B和D之间,正确的接法是:a → → → d ;
(2) 实验开始先点燃A处的酒精灯,打开旋塞K,让Cl2布满整个装置,再点燃D处的酒精灯。Cl2通过C装置后进入D,D装置内盛有碳粉,发生氧化还原反应,生成CO2和HCl(g),发生反应的化学方程式为____________________________________________。
(3) D处反应完毕后,关闭旋塞K,移去酒精灯,由于余热的作用,A处仍有少量Cl2产生,此时B中的现象是______________________________________________________,B的作用是__________________________________________________________________。
(4)用量筒取20mL E中溶液,倒入已检查完好的分液漏斗中,然后再注入10mL CCl4,盖好玻璃塞,振荡,静置于铁架台上(如图),等分层后取上层液和下层液,呈黄绿色的是_______________(填“上层液”或“下层液”),再装入如图所示的烧杯中,能使有色布条褪色的是__________(填“上层液”或“下层液”)
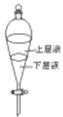
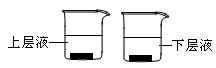
(5)在A、B、C、D、E装置中有一个需要改进,说明
需要改进的理由并画出改进后的装置图。
29.(15分)碱式氯化铝[Al2(OH)nCl6-n]m (1≤n≤6,m≤10) (商业代号BAC),是一种比Al2(SO4)3效果更好的净水药剂。以下是用煤矸石(主要含Al2O3,SiO2及少量铁的氧化物)为原料生产碱式氯化铝过程中碰到的情况:
(1)在反应器中加入16%的硫酸和16%的盐酸,在不断搅拌过程中再加入经过焙烧后的煤矸石粉,反应器上部有一条长管子作为反应时气体的排放管。加热至沸腾(102℃)并保持一段时间,期间不断用精密pH试纸在排气管口上方检查排出气体的pH,记录如下:
时间
起始
14min后
30min后
75min后
pH
<2.0
=2.5
<3.5
=3.5
试解释排气管中放出气体的pH变化的原因___________________________________假如把排气管加长一倍,排气的pH_________(回答“增大”“减小”或“不变化”),解释原因__________________________
(2)上述反应结束后,冷却,过滤弃渣,然后再加热至100℃,并在不断搅拌的条件下,向溶液慢慢地添加Ca(OH)2至适量,生成大量沉淀。过滤上述溶液,弃渣,得到澄清的BAC稀溶液。将此稀溶液加热蒸发浓缩,又产生白色细晶状沉淀,经化验分析,知此沉淀不是BAC固体,也不是AlCl3晶体或Al(OH)3。问:这种物质是__________________,为什么此时会有沉淀析出_____________________________________
30、(一)11分下图甲是某种动物体细胞的亚显微结构示意图,乙是该动物产生的一个卵细胞示意图。请据图回答:
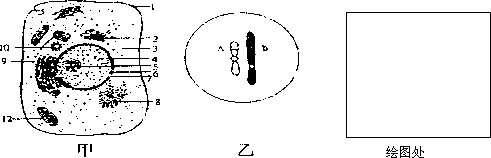
①在甲图中,能发生碱基互补配对现象的细胞器有_____________(填序号)。
②假如乙是甲细胞经过减数分裂形成的,则参与这一过程的非膜结构的细胞器有:[ ]_______________和[ ]____________________。东烟台 孙芸廷 整理
③根据乙图推断,该动物的基因型可能有______________________种。请在方框中绘出形成该细胞的次级卵母细胞(着丝点分裂以前)示意图,并注明染色体上的基因。
(二)10分
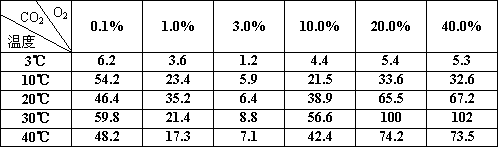 某校生物爱好小组的同学为了探究植物体呼吸强度的变化规律,选用新鲜菠菜作实验材料测定了在不同温度和不同氧浓度下,一定大小的菠菜叶的二氧化碳释放量(表中为相对值),测定数据如下表。请据表分析回答
某校生物爱好小组的同学为了探究植物体呼吸强度的变化规律,选用新鲜菠菜作实验材料测定了在不同温度和不同氧浓度下,一定大小的菠菜叶的二氧化碳释放量(表中为相对值),测定数据如下表。请据表分析回答
①为了使实验数据更能真实反映呼吸强度的变化,在实验环境条件上应非凡注重什么?
____________________________________________________________________________为什么? ____________________________________________________________________________
②表中数据反映出在氧浓度为20%的条件下,当温度从 3℃上升到 30℃时,植物的呼吸强度__________________________。其原因______________________________;
当氧含量从20%上升到40%时,植物的呼吸强度一般________________________。其原因____________________________________________________________。
③从表中数据分析可以得出,新鲜菠菜贮藏的最佳环境控制条件是:温度__________;氧浓度_____________。此条件下植物细胞内二氧化碳产生的场所是___________________________________________________。
31、15分果蝇是遗传学研究的好材料,遗传学家摩尔根曾因对果蝇的研究而获得“诺贝尔奖”。请回答下列有关问题:
(1)现有三试管果蝇,每支试管中均有红眼和白眼(相关基因为B、b),且雌雄各一半。各支试管内雌雄果蝇交配后,子代的情况如下:A管:雌雄果蝇均为红眼;B管:雌果蝇均为红眼,雄果蝇均为白眼;C管:雌雄果蝇均为一半红眼,一半白眼。根据上述结果可以判定出:果蝇的红眼和白眼与性别有关。
三支试管中亲代白眼果蝇的性别依次是_____________________________,C试管中亲本果蝇的基因型为______________________________。
(2)果蝇的长翅(A)对残翅(a)为显性,但是,即使是纯合长翅品种的幼虫,在35℃温度条件下培养(正常培养温度为 25℃),长成的成体果蝇却为残翅。这种现象称为“表型模拟”。山东烟台 孙芸廷 整理
这种模拟的表现性状能否遗传?为什么? ________________ _________________
________________ _________________。
(3)现有一只残翅果蝇,你能通过实验来确定它是纯合 aa,还是“表型模拟”吗?请你设计实验方案,并对结果进行分析。
方法步骤:____________________________________________________________
__________________________________________________________________________________。
结果分析:
____________________________________________________________________________
__。
(4)假设这只残翅果蝇(雌性)是由于遗传物质改变引起的。现有一定数量的长翅和残翅果蝇(正常温度下培养),请以最简捷的实验设计思路确定该性状是否为伴性遗传?并对可能出现的结果进行分析。
方法步骤:
__。
结果分析:
_____________________________________。
 2009年普通高等学校招生全国统一考试(南开中学模拟卷)
2009年普通高等学校招生全国统一考试(南开中学模拟卷)
理科综合能力测试(14)参考答案
第Ⅰ卷
题号
1
2
3
4
5
6
7
8
9
10
11
答案
C
B
D
C
B
A
C
A
D
B
D
题号
12
13
14
15
16
17
18
19
20
21
答案
B
C
D
A
A
B
D
D
C
D
22.①0.5 2.0 8.0 18.0 32.0 ②Ek=2ω2③2.0
(2)BCE(4分)
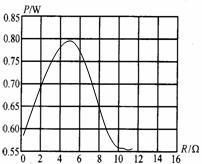 (3) eq \o\ac(○,1)1P = E2R / (R r)2 = 2 \* GB3 ②图略 = 3 \* GB3 ③0.80 5.0 = 4 \* GB3 ④ 4.0、0.5
(3) eq \o\ac(○,1)1P = E2R / (R r)2 = 2 \* GB3 ②图略 = 3 \* GB3 ③0.80 5.0 = 4 \* GB3 ④ 4.0、0.5
23.(1)
|
A1 |
|
A2 |
|
B1 |
|
B2 |
|
O |
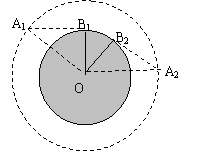
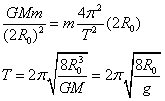
(2)设人在B1位置刚好看见卫星出现在A1位置,最后
在B2位置看到卫星从A2位置消失,
OA1=2OB1
有 ![]() ∠A1OB1=∠A2OB2=π/3
∠A1OB1=∠A2OB2=π/3
从B1到B2时间为t
则有 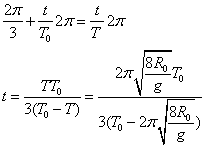
24.解:(1)平板车和小物块组成的系统水平方向动量守恒,故小物块到达圆弧最高点A时,二者的共同速度 ![]() (1分)设弹簧解除锁定前的弹性势能为
(1分)设弹簧解除锁定前的弹性势能为 ![]() ,上述过程中系统能量守恒,则有
,上述过程中系统能量守恒,则有 ![]() (4分)
(4分)
代入数据解得 ![]() (1分)
(1分)
(2)设小物块第二次经过 ![]() 时的速度大小为
时的速度大小为 ![]() ,此时平板车的速度大小为
,此时平板车的速度大小为 ![]() ,研究小物块在平板车圆弧面上的下滑过程,由系统动量守恒和机械能守恒有
,研究小物块在平板车圆弧面上的下滑过程,由系统动量守恒和机械能守恒有
![]() (2分)
(2分) ![]() (3分)
(3分)
由式代入数据解得 ![]() (1分)
(1分)
(3)最终平板车和小物块相对静止时,二者的共同速度为0.(1分)
设小物块相对平板车滑动的路程为S,对系统由能量守恒有 ![]() (4分)
(4分)
代入数据解得 ![]() (1分)
(1分)
则距 ![]() 点的距离
点的距离 ![]() (1分)
(1分)
25.⑴由于粒子在P点垂直射入磁场,故圆弧轨道的圆心在AP上,AP是直径。
设入射粒子的速度为v1,由洛伦兹力的表达式和牛顿第二定律得:
|
R |
|
A |
|
O |
|
P |
|
D |
|
Q |
|
φ |
|
O/ |
|
R/ |
解得: ![]()
⑵设O/是粒子在磁场中圆弧轨道的圆心,连接O/Q,设O/Q=R/。
由几何关系得: ![]()
![]()
由余弦定理得: ![]()
解得: ![]()
设入射粒子的速度为v,由 ![]()
解出: ![]()
26.⑴Al2O3(3分) CO2的电子式 (3分)
⑵N2+Al2O3+3C SHAPE \* MERGEFORMAT
|
1400~1800℃ |
⑶AlN+OH-+H2O=AlO ![]() +NH3↑(3分)
+NH3↑(3分)
⑷④⑦(4分,少一个正确答案扣2分、错选一个倒扣2分扣完为止)
28.(1) a→c→b→ d (2) (2) 2Cl2 C 2H2O ![]() 4HCl CO2 (2)
4HCl CO2 (2)
(3) 瓶中液面下降,长颈漏斗内液面上升 (2) 贮存少量Cl2避免Cl2对环境的污染 (2)
 (4)下层液 (2) 上层液(2)
(4)下层液 (2) 上层液(2)
(5) D中反应生成HCl极易溶于水,易发生倒吸 (2) (2)
或其它合理答案
29. (1)由于盐酸受热蒸发出HCl气体所致,随着反应的进行,盐酸逐渐与煤矸石中的物质反应而被消耗,因此,排气的pH从小逐渐变大。 增大。 假如排气管加长一倍,意味着排气被冷却的程度更高,HCl更多被冷凝回流,故排气的pH有所增大。
(2)沉淀物是水合硫酸钙(或硫酸钙)。由于硫酸钙是微溶的,在稀BAC溶液中达到饱和,浓缩蒸发过程中变为过饱和,故形成细晶状析出。 (每空3分)
30(一)、①9 12 ②[9]核糖体 [10]中心体 ③4(1分) 见右图 
(二)、①遮光使之处于黑暗状态。 防止叶片进行光合作用而影响呼吸强度的测定
②逐渐增大 随温度升高呼吸酶的活性增强 保持相对稳定 酶的数量限制(或线粒体数量限制)
③ 3℃ 3.0% 细胞质基质、线粒体
31、(1)雄、雌、雄 XbY和XBXb
(2)不能遗传 因为,这种残翅性状仅仅由环境条件的改变而引起的,遗传物质(基因)并没有改变,所以,不能遗传。
以下每空2分
(3)方法步骤:
让这只残翅果蝇与正常温度条件下发育成的异性残翅果蝇(基因型为aa)交配,并让其后代在正常温度条件下发育。
结果分析:
①若后代均为残翅果蝇,则这只果蝇为纯合体(aa);
②若后代中有长翅果蝇出现,则说明这只果蝇为“表型模拟”。
(4)方法步骤:
选择多个长翅果蝇与这只残翅果蝇杂交 ,在正常温度条件下培养观察
结果分析:
①若子代雌雄果蝇中均出现长翅和残翅,或均为长翅,则不是伴性遗传
②若子代果蝇中雌果蝇均表现为长翅,雄果蝇均表现为残翅,则为伴性遗传
