| ��������: �Ž�����.com������������
Ӣ��������www.1-123.com�����������ḻʵ�õĽ�����ѧ���� |
| |
| |
| |
|
|
7����NAΪ�����ӵ�������ֵ�����������в���ȷ���� A��12.4g�������к��е�P��P������0.6NA B��2.9g 2CaSO4��H2O���еĽᾧˮ������Ϊ0.01NA C��100g��98%��ŨH2SO4����������ԭ����Ϊ4NA D��2mol SO2��1 mol O2�����V2O5���ڵ����������ܱ������м��ȷ�Ӧ�����������ʷ���������2NA 8��Ŀǰ�����Ѿ����ֵ��ǽ���Ԫ�س�ϡ������Ԫ�����16�֣����ж���16���ǽ���Ԫ�ص��ж�����ȷ���� �ٶ�������Ԫ�أ�ԭ�ӵ�����������������3 �ڵ����ڷ�Ӧ�ж�ֻ���������� �۶�Ӧ�ĺ����ᶼ��ǿ�� ���⻯�ﳣ���¶�����̬�������ֽ���̬�⻯�� ����̬��������ˮ��Ӧ���������������� A��ȫ�� B��ֻ�Т٢� C��ֻ�Т٢ڢۢ� D��ֻ�Т٢ڢܢ� 9������˵��������� A��������Һ��K ��Fe3����I�D��SO42�����Դ������� B��ͬ�����ͬ���ʵ���Ũ�ȵ�NaOH��Һ��CH3COOH��Һ��ϣ�������Һ�У� c(Na��) c(H��)=c(CH3COO-) c(OH�D) C��pH=3��Na2SO4�������Ļ����Һ�У�c(Na��)=2c(SO42��) D����0.1mol/L��Na2S��Һ�У�c(OH�D)=c(H��) c(HS��) 2c(H2S) 10��������������ȷ���� A���������Һ���Ĺ����У���ֵ��С��ͬʱ���ͷ����� B���Ͼɵ�ر�����մ�������ֹ����к��еĹ���Ǧ���ӵȽ�����Ⱦ���� C��pH=5��������ϡ��1000������ҺpHԼΪ8 D�����ӻ�������һ���������Ӽ������ܻ����й��ۼ� 11����ѧ����S2O32�����ӷ���֮һ��ʹ��AgNO3��Һ��Ϊ�Լ�����AgNO3��Һ���뺬��S2O32�����ӵ���Һ�У��������·�Ӧ������Ag����2S2O32����[Ag(S2O3)2]3����3Ag����[Ag(S2O3)2]3����2Ag2S2O3���ף�����Ag2S2O3��H2O��Ag2S���ڣ�����H2SO4������S2O32�����Ӽ�����������������ȷ���� A���ü����������Ի������Һ�н��� B��ֻ����������Һ�н��� C��AgNO3������� D��S2�����ӶԸü����и��� 12�������йرȽ��У���С˳�����д������ A�����ȶ��ԣ�PH3<H2S<HCl<HF B�����ʵ��۵㣺ʯӢ��ʳ�Σ��ɱ���ˮ�� C��������ӵ�������CO32->CH3COO->SO42- D����ɢϵ�з�ɢ�����ӵ�ֱ����Fe(OH)3����Һ>Fe(OH)3����>FeCl3��Һ 13������ʵ���������������� A����Ũ��ˮ�м�����ʯ�ҿ�����ȡ������NH3
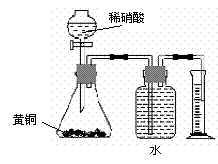 B����ˮ��һ���Լ����屽������������������ B����ˮ��һ���Լ����屽������������������
C��������ͼ��ʾ��װ�òⶨ��ͭ��Cu��Zn�Ͻ� ��Zn�ĺ��� D����ȥ�����е�Ca2����Mg2����SO42�������μ����������H2O��Ba(OH)2��Na2CO3��HCl 14. ��ͼ��ʾ�İ��β�����б�������»����ֽ�һ�������������У���
 A���п���ʹ���β۾�ֹ A���п���ʹ���β۾�ֹ
B���п��ܰ��βۼ����»� C�������������������»����������������»� D�������������أ����������»�
A���ò������������20cm B���ò��IJ���������8.4m C���ò��IJ��ٿ�����10.5 m/s D���ò���a������b������ʱ7s
A�� 17. ƽ�а�����ͼ����ʾ���ڱ仯�ĵ�ѹ���������ƵĴ������Ӿ�ֹ��ƽ�а����ģ���t=0ʱ�̿�ʼ�����ͷţ��˶����������������ͼ4���У��ܶ������������˶����ٶ�ͼ����ȷ����
����ѡ���⣨�������4С�⡣ÿС��������ĸ�ѡ���У��е�ֻ��һ��ѡ����ȷ���е��ж��ѡ����ȷ��ȫ��ѡ�Եĵ�6�֣�ѡ�Ե�ѡ��ȫ�ĵ�3�֣���ѡ���ĵ�0�֣�
A��I1���I2��� B��I1��С��I2��С C��P0���P��� D��P0��С��P��С
A��0~t1ʱ���ڣ�������ǣ���������ٶ������ʲ��� B��0~t1ʱ���ڣ�������ǣ�������䣬���ٶȲ��䣬�������� C��t1~t2ʱ���ڣ�������ǣ������С�����ٶȼ�С D��t1~t2ʱ���ڣ�������ǣ�������䣬���ٶȲ��� 20���������ǰѷǵ�ѧ��ת���ɵ�ѧ����һ��Ԫ������ͼ��ʾ���ҡ��������ֳ����ĵ���ʽ���������ֽ��ҡ������ִ������ֱ�ӵ�ͼ�ĵ�·�н���ʵ�飨�����ӵ�����������������ʱָ������ƫ��������ʵ����������ȷ���� A�����Ҵ����������·ʵ��ʱ����F��С���������ָ������ƫת B�����Ҵ����������·ʵ��ʱ����F����������ָ������ƫת C�����������������·ʵ��ʱ����������Һ���h����������ָ������ƫת D�����������������·ʵ��ʱ����������Һ���h��С���������ָ������ƫת
21.����̫��ϵ��������ܶȲ��䣬����ֱ��������֮����붼��С��ԭ����һ�룬������̫����ת����Ϊ����Բ���˶����������������仯��ȷ���� A���������������Ϊ��Сǰ��һ�� B���������������Ϊ��Сǰ�� C��������̫����ת��������Сǰ����ͬ D��������̫����ת���ڱ�Ϊ��Сǰ��һ��
�ڢ����174�֣� 22����18�֣� I��3�֣������в������ȵ��������ܹ���ȷ��0.01 mm����________ A���׳߶� B��10�ֶ��α꿨�� C��20�ֶ��α꿨�� D��50�ֶ��α꿨�� E���������� II��15�֣�ijͬѧ�����ij������Һ�ĵ����ʣ�����һ�����ȵij����������˸�װ��һ���缫���Ӵ����費�ƣ������缫��� �����������Ľ��в�������ѹ��������l5 V������Լ30 ��1��������ͨ�����е���Һ���ĵ��������˵�ѹ��ʵ�����ݣ�ʵ����������20�ֶȵ��α꿨�߲����˲����ܵ��ھ��������ͼ2��ʾ
��������������ش���������⣺ ��1���������ھ�d�IJ���ֵΪ����������cm�� ��2�����ݱ�1������ͼ3����������㣬������ ��3�����㵼����Һ�ĵ����ʱ���ʽ��
��ͼ��ʾ����һ��������ϰ�У�����Ϊ60kg��������Ա���������¥��l=90m���ķ��䡣����һ����ֱ�����������Ӿ�ֹ��ʼ�ȼ����»������������÷���Ĵ���A��ʱ����Ȼֹͣ�»���ͬʱ�ýŽ������߿����Լ�������һ�£�Ȼ����봰�ڡ���֪����Ա�ӿ�ʼ�»����ս��봰�ڹ�����ʱ��t=15s���Թ������������»�ʱ�ܵ���Ħ����F��С��ȡ1λ��Ч���֣�������ʾ��gȡ10 m��s2��
��ͼ��ʾ�������⻬�ij�ֱ�������� MN��PQƽ������ͬһˮƽ���ڣ�������L=0.2m��������˽��С�0.8V��0.8W������С���ݣ����촦�ڴŸ�Ӧǿ��ΪB��1T��������ֱ���µ���ǿ�ų��С�����ҲΪL�Ľ��������ab��ֱ�ڵ�����ã������뵼���ÿ�׳��ȵĵ����ΪR0=0.5�������ർ�ߵ��費�ơ���ʹ������������������뵼�����ýӴ����һ��������綯�ƣ�ʹС�����ܳ����������⡣ ��1��д��ab���ٶ�v���������MP�ľ���x�Ĺ�ϵʽ�������������С�ٶ�vmin�� ��2������v��x�Ĺ�ϵʽ������������x��ֵ��Ӧ��v����ֵ������У�Ȼ������v-xͼ�ߡ�
25����20�֣� �ڳ�Ϊ2L�ľ�Ե����ϸ�˵����˸�����һ��������Ϊm�Ĵ���С��A��B������Ϊ�ʵ㣬Ҳ�����Ƕ���������������A������硢�����Ϊ 2q��B������硣�����Ϊ��3q���ְ�A��B��ɵĴ���ϵͳ�����ڹ⻬��Ե��ˮƽ���ϣ�����A������ͼ��ʾ���н���ǿ�糡����MPQN�ڡ���֪����MP��ϸ�˵��д��ߣ�MP��NQ�ľ���Ϊ4L����ǿ�糡�ij�ǿ��СΪE������ˮƽ���ҡ���ȡ����A��B�������������ǴӾ�ֹ��ʼ�˶���������С���˶����������Ĵų���ɵ�Ӱ�죩 ��1����С��A��B�˶������е�����ٶȣ� ��2��С��A��B�ܷ�ص�ԭ�����㣿�����ܣ���˵�����ɣ����ܣ�����������ʱ�����ϵͳ�ֻص�ԭ�ط��㡣 ��3�����˶������д���С��B���������ӵ����ֵ��

26����10�֣�һ�֡��˹��̵������·������ڳ��¡���ѹ�����������£�N2�ڴ���������ˮ������Ӧ����NH3��N2 3H2O ��һ���о�NH3���������¶ȵĹ�ϵ������ʵ�����ݼ��±�����Ӧʱ��3 h����
��ش��������⣺ ��1��50��ʱ�ӿ�ʼ��3 h����O2���ʵ����仯��ʾ��ƽ����Ӧ����Ϊ mol��min��
��3����Ŀǰ�㷺Ӧ�õĹ�ҵ�ϳɰ�������ȣ��÷����й̵���Ӧ�������������������䷴Ӧ����������NH3�������Ľ��飺 �� ��4����ҵ�ϳɰ��ķ�ӦΪN2��g�� 3 H2��g�� �� �������·�Ӧ2NH3��g�� �� ��ͬ�����£�����һ��ͬ�����г���a mol N2��g����b mo1 H2��g�����ﵽƽ��ʱ�����������NH3Ϊ0��8 mo1��H2Ϊ2��0 mol���� 27����14�֣�A��B��C��D�Ƕ���������Ԫ�أ�ԭ��������������������������Ҫ�� �ٶ���������Ԫ����Aԭ�Ӱ뾶��С��Dԭ�Ӱ뾶��� ��Bԭ�������������Ǵ�����������������Cԭ�ӵ������������Ǻ������������3/4�� ��B��C���γɷǼ��Է���Y����Z�Ļ�ѧʽΪ ��ش��������⣺ ��1�� ��2�� ��3��������Zȼ�ϵ�صĹ���ԭ������ͼ��ʾ��
��ʯī��II���ĵ缫������______________������������������� ��д��ʯī��I���缫�Ϸ����ĵ缫��Ӧʽ______________�� ��4����ʯīΪ�缫����������Zȼ�ϵ�ص��һ��Ũ�ȵ� 28��(17��)����֮���ת����ϵ����ͼ��ʾ��A����Ϊ��ҵ����J��ԭ�ϣ�B��C��H��IΪ�ǽ������ʡ������£�X��һ��Һ̬����� FΪ�����ĺ���ɫ�����������ϵ���Ҫ�ɷ֣�O�dz�����������ߵĵ��ʣ� A��E��J��N�к���ͬһ��Ԫ�ء�
�ش��������⣺ (1)X�Ļ�ѧʽΪ__________________��X�ķ�������__________________ (����ԡ����Ǽ���)���ӣ�д����Ӧ�ݵ����ӷ�Ӧ����ʽ____________________________________�� (2)C D�ķ�Ӧ��ѧ����ʽΪ__________________ ���ڸ��µ������£���һ���ܱ�������Ͷ��1molC��2molD����Ӧһ��ʱ����C��ת����Ϊ50������D��ת����Ϊ________________����ʱ��������ƽ����Է�������Ϊ________________ �� (3)K��D��һ�������·�ӦҲ������H��д���仯ѧ����ʽ________________��д����Ӧ�Ļ�ѧ����ʽ________________________________________________�� (4)����1mol A�μӷ�Ӧ�����������Ӧ����ȫ������N������Ϊ1165g������K������Ϊ224g����Ӧ�ٵĻ�ѧ����ʽΪ___________________________________________�� 29����17�֣�ijѧϰС�����SO2���Ʊ�������̽��ʵ�顣 ��1�����ݷ�ӦNa2SO3���̣� H2SO4��Ũ��=Na2SO4 SO2�� H2O���Ʊ�SO2���塣 �������м�ͼ���ڴ���ֽ�ķ����������Ʊ����ռ�SO2��ʵ��װ�ã����Լ���ʾ��ͼ��
��ʵ������У�ʹ�÷�Һ©���μ�Ũ����IJ����ǣ�
��2����SO2����ֱ�ͨ��������Һ�У� ����ˮ��Һ�����ӷ���ʽΪ �� ��������Һ�������� �� ��3����һС����ʵ���з��֣�SO2����������������º���ʵ������ܲ����ԣ����ֲ��������������⡣�����Ʋ���ܵ�ԭ��˵����Ӧ����֤���������Բ��������� ��ԭ�� ����֤���� �� ��ԭ�� ����֤���� �� ��ԭ�� ����֤���� �� 30��16�֣�����ͼΪijһ���Զ����ϸ��ʾͼ��������ش�
��ͼ�и�ϸ�����ڸö���� �ṹ���ҵ�������ϸ��Ϊ��Ӭ��ϸ����ͼ��������һ��Ⱦɫ��ӦΪ �� �Ƽ�ϸ���γ���ϸ���ķ��ѷ�ʽΪ ����ϸ���е��ķ�����ĿΪ �������ղ�������ϸ���Ļ�����Ϊ �� �DZ�ϸ������ ��Ⱦɫ���飬����Ѳ�������ϸ��������Ϊ ��������ɿ����� �� 31����28�֣���.��������������£�Ѫ�Ǻ�����80��120 mg/dL�ķ�Χ�ڱ�������ȶ������ڱ�֤���������֯�����ٵ�����������������������Ľ��������ŷdz���Ҫ�����塣��ش������й��Ǵ�л�����⣺ ��1�������Ѫ�ǵ�ȥ·��________________________________________________________ ________________________________________________________________________�� ��2�������������ȵ������û��Ƶ��о���һ�����룬�������õ��ź�ͨ·�ѱȽ������A��B��ʾϸ��ͨѶ��ʽΪ�����ڳ��������ֲ�ͬ���͵��źŷ��Ӽ����źŴ�����ʽ��C��D��ʾ��ͬ���źŷ��Ӷ�ϸ�����õķ�ʽ������ͼ�����������ȵ��������ź�ͨ·��ͼ�е�_____________________
(3)����ij�˵��ȵ��غ��������ͣ���ȴ�����˵��͵�������֢״��������ͼ������Ϊ���ܵ�ԭ����_____________________________________________________�� ��4����ѧ����������ȡ���鶯����ȵ��أ���������������Ƴ���ĥҺ��ȴ����ֱ�ӷ�����ȵ��ص�����ܵ�ԭ����________________________________________________�� ��5����������ѧ֪ʶ����ִ��Ƽ��ɹ������������������������������д��˼·���ɣ� ��_____________________________________________________________________________ ��_____________________________________________________________________________ ��.�������ҹ��Ϸ���һ����Ҫ�ľ�������ݴ˻ش� ��1��������Ҷ��ϸ�����ԭ�������,��Ҫ����������м��,��������ʵ�����ʺ�?________�� A.�۲�ԭ������Ľṹ�Ƿ����� B.�۲�ϸ�������� C.�۲�ϸ������˿���� D.�۲�Ҷ�������̬����Ŀ
��3���ӱ�֤����������������������������̬ϵͳ������ѭ�������������ⲿ��Ĥ���˹���Ƥ��Ӧ���� �� ���ص㡣 ��4���ڸ����˹������б�����ľ���ͨ���� �� |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |