高三理科综合能力测试试题卷
一.单选
 1.右图的分类依据不可能是下列哪一项:
1.右图的分类依据不可能是下列哪一项:
A、是否为生物体 HIV 噬菌体
B、是否为组成细胞的结构
C、是否含DNA 核糖体 染色体
D、是否含遗传物质
2. 豌豆的黄子叶(Y)对绿子叶(y)为显性,灰种皮(B)对白种皮(b)为显性。现有基因型为YYBB和yybb的豌豆杂交,所得F1自交得F2,下列叙述正确的是:
①F1植株所结种子的子叶颜色出现性状分离;②F1植株所结种子的种皮颜色出现性状分离;③子叶颜色出现性状分离的现象可在同一植株体现④种皮颜色出现性状分离的现象可在同一植株体现⑤子叶颜色出现性状分离的现象可在同一豆荚体现⑥种皮颜色出现性状分离的现象可在同一豆荚体现
A、①③⑤ B、②④⑥ C、①③④ D、①②③
3. 赫尔希和蔡斯分别用35S和32P标记T2噬菌体的不同的有机物。下列被标记的部位组合正确的是

A.① = 2 \* GB3 ② B.①③ C.①④ D. = 2 \* GB3 ②④
4. 有丝分裂过程异常会发生多种染色体变异,其中不易发生的是:
A. 染色体结构改变 B.个别染色体增减
C.染色体组成倍增加 D. 染色体组成倍减少
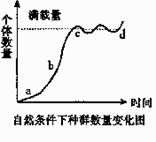 5.右图所示为自然环境中生物种群数量变化曲线,下列有关叙述错误的
5.右图所示为自然环境中生物种群数量变化曲线,下列有关叙述错误的
A.d处波动主要是因为出生率和死亡率
变动所致
B.“竭泽而渔”会使鱼虾数量下降至b以
下,使生态系统发展停滞甚至崩溃
C.灭鼠时假如仅杀死一半老鼠,可能
效果适得其反
D.微生物初级代谢产物在a 阶段大量
合成,因此,生产上发酵必须在a时停止
6.“绿色化学”是指从技术.经济上设计可行的化学反应,尽可能减少对环境的负作用。下列化学反应,不符合绿色化学概念的是 ( )
A.消除硫酸厂尾气排放 SO2+NH3+H2O==(NH4)2SO3
B.消除制硝酸工业尾气的氮氧化物污染 NO2+NO+NaOH==2NaNO2+H2O
C.制CuSO4 Cu+2H2SO4(浓)==CuSO4+SO2↑+2H2O
D.制CuSO4 2Cu+O2==2CuO CuO+H2SO4(稀)==CuSO4+H2O
D.矿质元素在植物体内的运输不需要消耗ATP
7.下列事实不能作为实验判定依据的是
A.钠和镁分别与冷水反应,判定金属活动性强弱
B.在MgCl2与AlCl3溶液中分别加入过量的氨水,判定镁与铝的金属活动性强弱
C.碳酸钠溶液显碱性,硫酸钠溶液显中性,判定硫与碳的非金属活动性强弱
D.Br2与I2分别与足量的H2反应,判定溴与碘的非金属活动性强弱
8.下列有关溶液中各种离子浓度的关系错误的是
A.0.1mol·L-1NH4Cl溶液中:c(Cl-) c(OH-) =c(NH4 ) c(H )
B.0.1mol·L-1NaHSO3溶液中:c(SO32-) c(HSO3-) c(H2SO3)=0.1mol·L-1
C.0.1mol·L-1KAl(SO4)2溶液中:c(SO42-)=c(Al3 ) c(K )
D.足量铁屑溶于稀硝酸所得溶液中:c(NO3-)>c(Fe2 )>c(H )>c(OH-)
9.LiFePO4新型锂离子动力电池以其独特的优势成为奥运会绿色能源的新宠.已知该电池放电时的电极反应式为:正极 FePO4 Li e-==LiFePO4 ,负极 Li-e-== Li .下列说法中正确的是
A.充电时电池反应为FePO4 Li = LiFePO4
B.充电时动力电池上标注“ ”的电极应与外接电源的正极相连
C.放电时电池内部Li 向负极移动
D.放电时,在正极上是Li+得电子被还原
10.下列离子方程式书写正确的是
A.硝酸银溶液中滴加过量氨水:Ag NH3·H2O=AgOH↓ NH4
B.硫化钠的水解反应:S2-+H3O ![]() HS-+H2O
HS-+H2O
C.4mol/L的KAl(SO4)2溶液与7mol/L的Ba(OH)2溶液等体积混合:
Al3 2SO42— 2Ba2 4OH—=AlO2— 2BaSO4↓ 2H2O
D.向KI与稀硫酸的混合溶液中通入氧气:4H +O2+4I-=2I2 2H2O
11.奶粉中添加三聚氰胺事件再次敲响我国食品安全的警钟。三聚氰胺是一种常用化工原料,其结构简式如图所示。下列有关三聚氰胺的说法正确的是 ( )
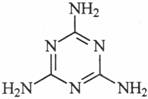 A.奶粉中添加三聚氰胺能提高蛋白质的含量
A.奶粉中添加三聚氰胺能提高蛋白质的含量
B.三聚氰胺是一种白色结晶粉末,熔点高,硬度大
C.三聚氰胺属于非极性分子,在水中可形成悬浊液
D.三聚氰胺分子中含有氨基,氨基的电子式为 ![]()
12.下列结论正确的是( )
①微粒半径: ![]() ; ②氢化物的稳定性:
; ②氢化物的稳定性: ![]() ;
;
③离子的还原性: ![]() ;④氧化性:
;④氧化性: ![]() ;
;
⑤酸性: ![]() ;⑥非金属性:
;⑥非金属性: ![]() 。
。
A.②④⑥ B.①③④ C.只有① D.⑥
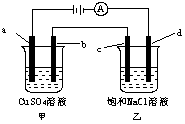 13.如图所示,a、b、c均为石墨电极,d为碳钢电极,通电进行
13.如图所示,a、b、c均为石墨电极,d为碳钢电极,通电进行
电解。假设在电解过程中产生的气体全部逸出,下列说法正
确的是
A.甲、乙两烧杯中溶液的pH均保持不变
B.甲烧杯中a的电极反应式为4OH――4e-=O2↑+2H2O
C.当电解一段时间后,将甲、乙两溶液混合,一定会产生蓝
色沉淀
D.当b极增重3.2g时,d极产生的气体为2.24L(标准状况)
二、选择题(本题共8小题.在每小题给出的四个选项中,有的只有一个选项正确,有的有多个选项正确,全部选对的得6分,选对但不全的得3分,有选错的得0分)
14.我国探月的“嫦娥工程”已启动,在不久的将来,我国宇航员将登上月球。假如宇航员在月球上测得摆长为L的单摆做小振幅振动的周期为T,将月球视为密度均匀、半径为r的球体,则月球的密度为
A. ![]() \* MERGEFORMAT B.
\* MERGEFORMAT B. ![]() \* MERGEFORMAT C.
\* MERGEFORMAT C. ![]() \* MERGEFORMAT D.
\* MERGEFORMAT D. ![]() \* MERGEFORMAT
\* MERGEFORMAT
|
甲 |
|
A |
|
乙 |
|
B |
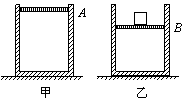 15.如图甲所示,内壁光滑的绝热气缸竖竖立于地面上,绝热活塞将一定质量的气体封闭在气缸中,活塞静止时处于A位置。现将一重物轻轻地放在活塞上,活塞最终静止在如图乙所示的B位置。设分子之间除相互碰撞以外的作用力可忽略不计,则活塞在B位置时与活塞在A位置时相比较
15.如图甲所示,内壁光滑的绝热气缸竖竖立于地面上,绝热活塞将一定质量的气体封闭在气缸中,活塞静止时处于A位置。现将一重物轻轻地放在活塞上,活塞最终静止在如图乙所示的B位置。设分子之间除相互碰撞以外的作用力可忽略不计,则活塞在B位置时与活塞在A位置时相比较
A.气体的压强可能相同
B.气体的内能可能相同
C.单位体积内的气体分子数一定增多
D.单位时间内气体分子撞击活塞的次数一定增多
|
\* MERGEFORMAT R S |
|
0 |
|
0.2 |
|
-0.2 |
|
2 |
|
4 |
|
· |
|
· |
|
P |
|
\* MERGEFORMAT R S |
|
图甲 |
|
0.2 |
|
-0.2 |
|
0.5 |
|
1.0 |
|
· |
|
· |
|
0 |
|
\* MERGEFORMAT |
|
图乙 |
|
\* MERGEFORMAT |
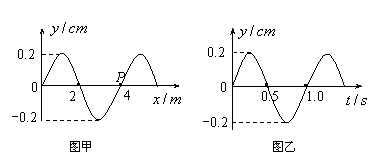 |
16.如图所示,图甲为一列横波在t=0.5s时的波动图象,图乙为质点P的振动图象,下列说法正确的是
A.波沿x轴正方向传播
B.波沿x轴负方向传播
C.波速为6 m/s
D.波速为4m/s
17.如图甲所示,一轻弹簧的两端与质量分别为 ![]() \* MERGEFORMAT 、
\* MERGEFORMAT 、 ![]() \* MERGEFORMAT 的两物块
\* MERGEFORMAT 的两物块 ![]() \* MERGEFORMAT 、
\* MERGEFORMAT 、 ![]() \* MERGEFORMAT 相连接,并静止在光滑水平面上.现使B获得水平向右、大小为3m/s的瞬时速度,从此刻开始计时,两物块的速度随时间变化的规律如图乙所示,从图像提供的信息可得:
\* MERGEFORMAT 相连接,并静止在光滑水平面上.现使B获得水平向右、大小为3m/s的瞬时速度,从此刻开始计时,两物块的速度随时间变化的规律如图乙所示,从图像提供的信息可得:
A.在 ![]() \* MERGEFORMAT 、
\* MERGEFORMAT 、 ![]() \* MERGEFORMAT 时刻两物块达到共同速度1m/s,且弹簧都处于伸长状态
\* MERGEFORMAT 时刻两物块达到共同速度1m/s,且弹簧都处于伸长状态
B.从 ![]() \* MERGEFORMAT 到
\* MERGEFORMAT 到 ![]() \* MERGEFORMAT 时刻间弹簧由压缩状态恢复到原长
\* MERGEFORMAT 时刻间弹簧由压缩状态恢复到原长
C.两物体的质量之比为 ![]() \* MERGEFORMAT
\* MERGEFORMAT
\* MERGEFORMAT
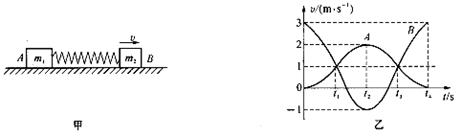 |
D.在 ![]() \* MERGEFORMAT 时刻
\* MERGEFORMAT 时刻 ![]() \* MERGEFORMAT 、
\* MERGEFORMAT 、 ![]() \* MERGEFORMAT 两物块的动能之比为
\* MERGEFORMAT 两物块的动能之比为 ![]() \* MERGEFORMAT ∶1
\* MERGEFORMAT ∶1
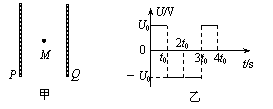
18.如图甲所示,两个平行金属板P、Q正对竖直放置,两板间加上如图(乙)所示的交变电压。t=0时,Q板比P板电势高U0,在两板的正中心M点有一电子在电场力作用下由静止开始运动(电子所受重力可忽略不计),已知电子在0~4t0时间内未与两板相碰。则电子速度方向向左且速度大小逐渐增大的时间是
A.0<t<t0
B.t0<t<2t0
|
P |
|
Q |
|
甲 |
|
M |
|
乙 |
|
0 |
|
U0 |
|
-U0 |
|
t0 |
|
2t0 |
|
3t0 |
|
4t0 |
|
t/s |
|
U/V |
 C.2t0<t<3t0
C.2t0<t<3t0
D.3t0<t<4t0
|
O |
 19.如图所示,过空间O点,可放倾角不同的光滑斜面。从O点无初速度地释放物体,记下它们沿这些斜面滑下速率为
19.如图所示,过空间O点,可放倾角不同的光滑斜面。从O点无初速度地释放物体,记下它们沿这些斜面滑下速率为 ![]() \* MERGEFORMAT 的位置,把这些位置连接起来,它们应该在同一个
\* MERGEFORMAT 的位置,把这些位置连接起来,它们应该在同一个
A.球面 B.抛物面
C.水平面 D.椭圆面
![]() 20.如图所示,q1和q2是两个位置固定的正、负点电荷,在它们直线延长线上的a点,电场强度恰好为零。现将一个正电荷q从a点左边的b点沿bac直线移到右边的c点,该电荷的电势能将
20.如图所示,q1和q2是两个位置固定的正、负点电荷,在它们直线延长线上的a点,电场强度恰好为零。现将一个正电荷q从a点左边的b点沿bac直线移到右边的c点,该电荷的电势能将
A.不断增大 B.不断减小
C.先减小后增大 D.先增大后减小
21.空间某区域内存在着电场,电场线在竖直平面上的分布如图所示,一个质量为m、电量为q的小球在该电场中运动,小球经过A点时的速度大小为v1,方向水平向右,运动至B点时的速度大小为v2,运动方向与水平方向之间的夹角为α,A、B两点之间的高度差与水平距离均为H,则以下判定中正确的是
A.若v2>v1,则电场力一定做正功
B.A、B两点间的电势差 ![]() \* MERGEFORMAT
\* MERGEFORMAT
C.小球由A点运动至B点,电场力做的功 ![]() \* MERGEFORMAT
\* MERGEFORMAT
D.小球运动到B点时,所受重力的瞬时功率P=mgv2sinα
三填空
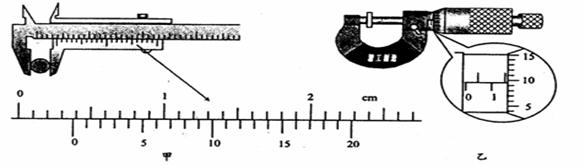
22、(4分)(1)、图甲所示20分度的游标卡尺的读数是 mm;图乙所示的螺旋测微器的读数是 mm。
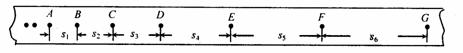 (2)、(8分)如图所示,某同学在做“研究匀变速直线运动”实验中,由打点计时器得到了表示小车运动过程的一条清楚纸带,纸带上两个相邻计数点的时间间隔为T=0.1s,其中s1=5.25cm、s2=5.74cm、s3=6.25cm、s4=6.75cm、s5=7.26cm、s6=7.75cm。由此可以得到小车运动的加速度大小是 m/s2,打点计时器打D点时小车的速度是 m/s。(结果保留到小数点后两位)
(2)、(8分)如图所示,某同学在做“研究匀变速直线运动”实验中,由打点计时器得到了表示小车运动过程的一条清楚纸带,纸带上两个相邻计数点的时间间隔为T=0.1s,其中s1=5.25cm、s2=5.74cm、s3=6.25cm、s4=6.75cm、s5=7.26cm、s6=7.75cm。由此可以得到小车运动的加速度大小是 m/s2,打点计时器打D点时小车的速度是 m/s。(结果保留到小数点后两位)
|
37° |
|
B |
|
A |
|
v0 |
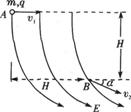
 23.(18分)跳台滑雪是一种极为壮观的运动,它是在依山势建造的跳台上进行的运动。运动员穿着专用滑雪板,不带雪杖在助滑路上获得较大速度后从跳台水平飞出,在空中飞行一段距离后着陆。如图所示,设某运动员从倾角为θ=37°的坡顶A点以速度v0=20m/s沿水平方向飞出,到山坡上的B点着陆,山坡可以看成一个斜面。(g=10m/s2,sin37º=0.6,cos37º=0.8)求:
23.(18分)跳台滑雪是一种极为壮观的运动,它是在依山势建造的跳台上进行的运动。运动员穿着专用滑雪板,不带雪杖在助滑路上获得较大速度后从跳台水平飞出,在空中飞行一段距离后着陆。如图所示,设某运动员从倾角为θ=37°的坡顶A点以速度v0=20m/s沿水平方向飞出,到山坡上的B点着陆,山坡可以看成一个斜面。(g=10m/s2,sin37º=0.6,cos37º=0.8)求:
(1)运动员在空中飞行的时间t;
(2)AB间的距离s。
24.(20分)李明同学进行一次跳高测试,测量他的身高为1.70 m,质量为60 kg,他先弯曲两腿向下蹲,再用力蹬地起跳,从蹬地开始经0.40 s竖直跳离地面。设他蹬地的力大小恒为1050 N,其重心上升可视为匀变速直线运动。求小明从蹬地开始到最大高度过程中机械能的增加量。(不计空气阻力,取g=10 m/s2。)
25.(22分)如图所示,光滑的 ![]() \* MERGEFORMAT 圆弧轨道AB、EF,半径AO、O′F均为R且水平。质量为m、长度也为R的小车静止在光滑水平面CD上,小车上表面与轨道AB、EF的末端B、E相切。一质量为m的物体(可视为质点)从轨道AB的A点由静止开始下滑,由末端B滑上小车,小车立即向右运动。当小车右端与壁DE刚接触时,物体m恰好滑动到小车右端且相对于小车静止,同时小车与壁DE相碰后立即停止运动但不粘连,物体继续运动滑上圆弧轨道EF,以后又滑下来冲上小车。求:
\* MERGEFORMAT 圆弧轨道AB、EF,半径AO、O′F均为R且水平。质量为m、长度也为R的小车静止在光滑水平面CD上,小车上表面与轨道AB、EF的末端B、E相切。一质量为m的物体(可视为质点)从轨道AB的A点由静止开始下滑,由末端B滑上小车,小车立即向右运动。当小车右端与壁DE刚接触时,物体m恰好滑动到小车右端且相对于小车静止,同时小车与壁DE相碰后立即停止运动但不粘连,物体继续运动滑上圆弧轨道EF,以后又滑下来冲上小车。求:
(1)水平面CD的长度;
(2)物体m滑上轨道EF的最高点相对于E点的高度h;
(3)当物体再从轨道EF滑下并滑上小车后,小车立即向左运动。假如小车与壁BC相碰后速度也立即变为零,最后物体m停在小车上的Q点,则Q点距小车右端多远?
|
R |
|
R |
|
A |
|
B |
|
C |
|
O |
|
h |
|
D |
|
O′ |
|
R |
|
E |
|
F |

26. (16分) (1).化学实验设计和操作中必须十分重视安全问题和环境保护问题.下列实验问题处理方法不正确的是_________________.
①.制氧气时排水法收集氧气后出现倒吸现象,立即松开试管上的橡皮塞
②.在气体发生装置上直接点燃一氧化碳气体时,必须要先检验一氧化碳气体的纯度.最简单的方法是用排空气的方法先收集一试管气体,点燃气体,听爆鸣声
③.实验结束后将所有的废液倒入下水道排出实验室,以免污染实验室
④.给试管中的液体加热时,不时移动试管或加入碎瓷片,以免暴沸伤人
⑤.不慎将酸溅到眼中,应立即用水冲洗,边洗边眨眼睛
⑥.配制硫酸时,可先在烧杯中加入一定体积的水,再边搅拌边加入浓硫酸
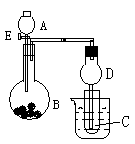 (2).用如右图所示装置进行实验,将A逐滴加入B中:
(2).用如右图所示装置进行实验,将A逐滴加入B中:
a.若B为Na2CO3粉末,C为C6H5ONa溶液,实验中观察到小试管内溶液由澄清变浑浊,则试管C中化学反应的离子方程式________________ .然后往烧杯中加入沸水,可观察到试管C中的现象 .
b.若B是生石灰,观察到C溶液中先形成沉淀,然后沉淀溶解.当沉淀完全溶解,恰好变澄清时,关闭E.然后往小试管中加入少量葡萄糖溶液,再往烧杯中加入热水,静置片刻,观察到试管壁出现光亮的银镜,则A是 (填名称),C是 (填化学式).与葡萄糖溶液混合后,该溶液中反应的化学方程式_________.仪器D在此实验中的作用是 .
(3).某固体混合物中含有Na 、K 、Mg2 和Cl-、Br-五种微粒.
Ⅰ.欲将钠、钾、镁三元素大致分离开来,并将氯、溴两元素大致分离开来,有以下方法和操作步骤可供选择(其中有的步骤可选两次).
= 1 \* GB3 ①.溶于水制成稀溶液; = 2 \* GB3 ②.溶于水制成浓溶液; = 3 \* GB3 ③.通入足量CO2; = 4 \* GB3 ④.加入足量氯水; = 5 \* GB3 ⑤.通入足量氨气; = 6 \* GB3 ⑥.过滤; = 7 \* GB3 ⑦.用四氯化碳萃取.
选取最合理的方法和步骤:(按顺序先后填写编号) .
Ⅱ.分离后剩余的水溶液中所含的主要物质是 .
Ⅲ.在上述分离过程中分离出一种化合物晶体.欲得到干燥的该化合物固体,有两种方法可供选择: = 1 \* GB3 ①.加热蒸发掉水分; = 2 \* GB3 ②.将过滤得到的固体物质自然风干.正确的方法应选择_____.
27.(10分)物质之间的转化关系如下图所示,A可作为工业生产J的原料,B、C、H、I为非金属单质,H是密度最小的气体,X的水溶液为一种常见的无色医用消毒液,F为常见的红棕色防锈油漆颜料的主要成分,O是常见氮肥,且反应⑦中L与M的物质的量之比为1∶2,A、E、J、N中含有同一种元素.
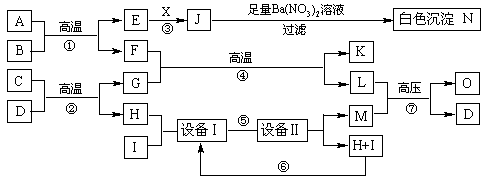
回答下列问题:
(1).X的化学式为_______________,C D的反应方程式为___________________.
(2).设备Ⅰ的名称_______________.工业生产中为了节约资源、降低成本和保护环境,经常对某些物质进行循环利用.上述转化关系中能达到该目的的是___________(填序号).
(3).写出反应⑦的化学方程式________________________________________________.
28(12分)2008年我国南方地区遭受了历史上罕见的特大的冰雪,交通堵塞,电网中断,给群众的生活带来很多困难。化学试剂氯化钙作为融雪剂在抗雪灾中起了一定的作用。氯化钙是用途广泛的化学试剂,可作干燥剂、冷冻剂、防冻剂等。为了测定某氯化钙样品中钙的含量,进行如下实验:
= 1 \* GB3 ①准确称取氯化钙样品0.2312 g,放入烧杯中,加入适量6 mol/L的盐酸和适量蒸馏水使样品完全溶解,再滴加35.00 mL 0.25 mol/L (NH4)2C2O4溶液,水浴加热,逐渐生成CaC2O4沉淀,经检验,Ca2+已沉淀完全。
= 2 \* GB3 ②过滤并洗涤 = 1 \* GB3 ①所得沉淀。
= 3 \* GB3 ③加入足量的10% H2SO4和适量的蒸馏水, = 2 \* GB3 ②中沉淀完全溶解,溶液呈酸性,加热至75℃,趁热加入0.05 mol/L KMnO4溶液16 .00mL,恰好完全反应。
回答下列问题:
(1)配平: MnO4-+ H2C2O4+ H+― Mn2++ CO2↑+ H2O
(2)0.05mol·L-1KMnO4标准溶液应置于 (选填“酸式”或“碱式”)滴定管中;判定滴定终点的现象为 。
(3)计算该氯化钙样品中钙元素的质量分数为 (精确到0.01%)。
|
[ CH2-C ]n |
|
COOCH3 |
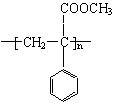 |
29.
|
是一种重要的高分子材料,可通过如下路线进行合成:
|
① 溴水 |
|
A |
|
B |
|
C |
|
② NaOH溶液 |
|
③ O2 |
|
④ 新制的Cu(OH)2 |
|
△ |
|
Cu△ |
|
悬浊液△ |
|
D |
|
E |
|
F |
|
浓硫酸 △ |
|
⑤ |
|
浓硫酸△ |
|
⑥ CH3OH |
|
⑦ |
|
W |
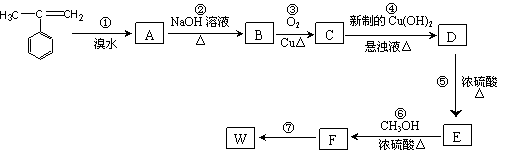 |
按要求填空:
(1)属于取代反应的有 (填写反应编号);
(2)写出C和F结构简式:C ;F ;
(3)写出反应②和⑤的化学方程式:
② ,
⑤ 。
⑥
30.回答以下两个问题
Ⅰ.下图I、Ⅱ、Ⅲ表示高等动植物细胞的部分代谢过程,请据图回答问题:
|
ADP |
|
ATP |
|
(CH2O) |
|
① |
|
② |
|
NADP |
|
NADPH |
|
③ |
|
H2O |
|
H |
|
O2 |
|
光 |
|
葡萄糖 |
|
脂肪 |
|
B |
|
CO2 H2O |
|
④ |
|
A |
|
⑤ |
|
⑥ |
|
⑦ |
|
⑧ |
|
内环境 |
|
CO2 |
|
肝细胞 |
|
Ⅰ |
|
Ⅱ |
|
Ⅲ |
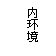  |
(1)I阶段中生成NADPH的过程用一反应式表示为 ,其反应场所为___ ___。I阶段中发生的能量变化是 。
(2)CO2从细胞外到细胞内并参与过程Ⅱ的第一步骤,这一步骤叫做 。假如CO2的供给忽然停止,过程Ⅱ中 (物质)会增多。
(3)肝脏是人体非常重要的器官,I、Ⅱ过程生成的糖通过摄食并消化吸收进入肝细胞后,既可被氧化分解,也可通过⑥形成物质[A] (填名称)。
(4)当膳食糖分过高后,还可发生⑦⑧过程,该过程需要肝细胞合成 (填物质名称)参与方可生成[B] (填名称),运出肝脏,否则会造成脂肪肝。
Ⅱ.二倍体植物柴油树的种子榨出的油稍加提炼就可成为柴油。为了实现大规模生产,科学家在“神州六号飞船”上搭载了四株珍贵的试管苗。
(1)为了获得高产柴油品系,以幼苗作为实验材料的理由是 。
(2)试管苗返回地面后,为了在短时间内扩大幼苗数量,应该运用 技术,所获得的植株中大部分植物的产油量 (填“增加”、“减少”或“基本不变”)。
|
前体物质 |
|
酶I |
|
酶II |
|
中间物质X |
|
油 |
|
A基因 |
|
B基因 |
 |
(3)科学研究发现,某些种类的细菌能将“前体物质”转化为柴油。已知产油的代谢途径如下:
①从来源看,“油”可以来源于微生物,也可以来源于植物,从遗传学的性状和基因的关系分析,由上图可以得出 。
②若通过生物工程,利用枯草杆菌来大量获得这种“柴油”,请简述其操作方法
(4)现有AaBb的个体,为尽快获得高产稳产植物,选用的育种方法是 。
31.牛的黑色(B)对红色(b)为显性,良种场现有两栏种牛,A栏全是黑色,B栏既有黑
色又有红色。AB两栏牛是亲子代关系,来场参观的生物爱好小组同学,有的说B栏是A栏
的亲代,有的说B栏是A栏的子代。请你根据所学的生物学知识,分析回答下列问题:
(1)若B栏种牛是A栏种牛的杂交后代,则A栏种牛的基因型为___________,B栏种牛
的基因型为___________。
(2)若A栏种牛是B栏种牛的杂交后代,则B栏种牛的基因型为___________,A栏种牛的基因型___________。
(3)若B栏是A栏的亲本时,B栏种牛除必须具有相对性状(黑色与红色)外,还应具备的两个条件是:①______________________,②______________________。
(4)若B栏是A栏的亲本,且B栏中黑色也有杂合体,A栏中没有红色种牛的原因是__________________________ _______。
