| ��������: �Ž�����.com������������
Ӣ��������www.1-123.com�����������ḻʵ�õĽ�����ѧ���� |
| |
| |
| |
|
|
��2��ȡ��Һ������ɫ��Ӧ������ʻ�ɫ��
| �϶����ڵ�����
| �϶������ڵ�����
| ����
|
|
| |
��3��ȡ��ɫ��������ϡ������������ȫ�ܽⲢ�ų����塣
�϶����ڵ�����
�϶������ڵ�����
����
��4��ͨ������ʵ������ȷ����������______________��
27����15�֣�
D��E��X��Y��Z�����ڱ��е�ǰ20��Ԫ�أ���ԭ���������������ǵ�����⻯����ӵĿռ乹���������������塢�����Ρ��������塢���Σ�V�Σ���ֱ���Ρ��ش��������⣺
��1��Y�������������Ļ�ѧʽΪ__________��
��2������5��Ԫ���У����γ�������ǿ�ĺ������Ԫ����___________��д����Ԫ�ص�����3�ֺ�����Ļ�ѧʽ��__________________________________��
��3��D��Y�γɵĻ��������ӵĿռ乹��Ϊ____________��
��4��D ��X�γɵĻ�����仯ѧ��������___________���侧��������__________��
��5������þ��E�ĵ����ڸ����·�Ӧ�õ��IJ�����___________���˲�����ˮ��Ӧ�������ּ�÷�Ӧ�Ļ�ѧ����ʽ��____________________��
��6���ԱȽ�D��X�������������۵�ĸߵͲ�˵�����ɣ� ____________________________________________ _____________
28����15�֣�
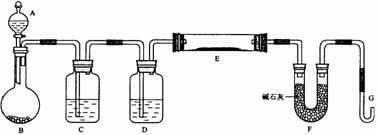 ij����С������H2��ԭ��ɫ��WO3��ĩ�ⶨW�����ԭ����������ͼ�Dzⶨװ�õ�ʾ��ͼ��A�е��Լ���������
ij����С������H2��ԭ��ɫ��WO3��ĩ�ⶨW�����ԭ����������ͼ�Dzⶨװ�õ�ʾ��ͼ��A�е��Լ���������
��ش��������⡣
��1��������װ����Լ���B_________ ��C________��D___________��
��2�����Ӻ�װ�ú�Ӧ����_________________________���䷽����________________
��3�������ȷ�Ӧ��E���͡���Aƿ��εμ�Һ�塱����������Ӧ���Ƚ��е��� _______________����������֮�仹Ӧ���еIJ�����____________________________��
��4����Ӧ������G���ݳ���������________________���䴦��������_____
��5����ʵ���в������������
�ٿ�E�ܵ�����a �� ��E�ܺ�WO3��������b ���۷�Ӧ��E�ܺ�W�۵�������c����ȴ�����³��������ܷ�ӦǰF�ܼ���ʢ���������d ���ݷ�Ӧ��F�ܼ���ʢ���������e
���������ݿ����г�����W�����ԭ��������������ͬ����ʽ����W�⣬�����漰��Ԫ�ص����ԭ��������Ϊ��֪����
����ʽ1��Ar(W)��____________������ʽ2��Ar(W)��____________��
29����16�֣�
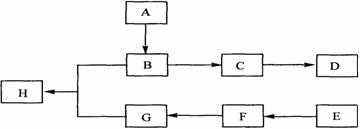
��ͼ��A��B��C��D��E��F��G��H��Ϊ�л������
�ش��������⣺
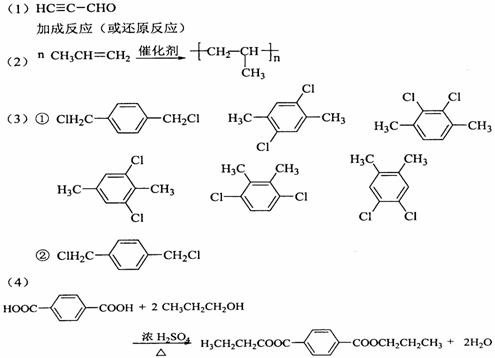
��1���л������� A����Է�������С��60��A�ܷ���������Ӧ��1molA�ڴ�������������3 mol H2��Ӧ����B����A�Ľṹ��ʽ��___________________����A����B�ķ�Ӧ������ ��
��2��B��Ũ�����м��ȿ�����C��C�ڴ��������¿ɾۺ����ɸ߷��ӻ�����D����C����D�Ļ�ѧ����ʽ��__________________________��
��3���ٷ��㻯����E�ķ���ʽ��C8H8Cl2��E�ı����ϵ�һ��ȡ����ֻ��һ�֣���E�����п��ܵĽṹ��ʽ��_______________________________________________
��E��NaOH��Һ�п�ת��ΪF��F�ø������������Һ��������G��C8H6O4����1 mol G�������� NaHCO3��Һ��Ӧ�ɷų� 44.8 L CO2����״�������ɴ�ȷ��E�Ľṹ��ʽ��________________
��4��G��������B��Ũ������¼��ȷ�Ӧ������H������G��B����H�Ļ�ѧ����ʽ��____________________________���÷�Ӧ�ķ�Ӧ������_______________________��
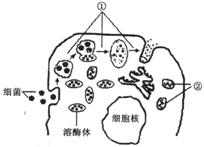 30����.(12��)��ͼΪ����ϸ��ɱ��ϸ����ʾ��ͼ��ͼ
30����.(12��)��ͼΪ����ϸ��ɱ��ϸ����ʾ��ͼ��ͼ
�е���ø���ں��ж���ˮ��ø����ͼ�ش�
(1)ͼ�Тٹ��̽��е�����ø���ͷ�ˮ��ø����
ϸ���ֽ⣬�ù������� ���ߡ�
(2)��Щ���Ժ�ǿ��ϸ����������������Ȼ����
�ܱ�����������ڲ����ص� ���Ա���¶��
�����ʵݸ���Ӧ������ϸ����ʹ֮Ѹ����ֳ�ֻ�
�� ������ϸ������Һ�лʱ���ᱻ��Ӧ�Ŀ������������������������е� ��
(3)ͼ�Т�Ϊ�����壬���д���������ڷ�������ϸ�������йص���Ҫ��ѧ�仯����(��ͼ���ʾ)��
�� ��
 |
��1��������Ҷ��ϸ���У��ܹ����иù��̵�ϸ���ṹ��Ҫ��________��
��2��ת¼�����У�DNA������[ ]___________�Ĵ������£���DNA�����м�����ڵ�___________�Ͽ����ù��̳�Ϊ___________��
��3��Ȼ����[4] RNA�ۺ�ø�Ĵ������£������еļ���Ϊģ�壬��[ ] __________Ϊԭ�ϣ���_________�ṩ����������_________________ԭ�ϳɳ�[ ] __________��
��4�������ϸ����ϸ�����У�ת¼�IJ���ͨ��________���뵽ϸ�����У���__________�����һ��ָ�������ʵ�����ϳɡ�
31����20�֣�������Ժʿ�����2006��ȹ�����߿Ƽ���������Ҫ�ɾ���ʵ����С��ͬ��������ԶԵ�ӽ����������˶��С����Ʒ�֣���ش������й�С���Ŵ����ֵ����⣺
1����С�������죨A�������죨a�������ԣ������ȣ�B���Բ������ȣ�b�������ԣ����Ի���������ϣ������о������������״���ӽ������У���ij�ױ���˫���ʹ������ӽ���F1����״�����Ϊ1��1����д�����ױ����ܵĻ����ͣ�___________________________��
2���������С�����벻������һ�Ի�����Ҷ����DNA�ϣ����Կ��������벻��������Ĵ����ױ��ӽ���Ҫ�õ�����������壬���ñ�����Ϊ____________�ĸ�����ĸ�����ô��ϵĿ�������������������________����
3��С����������Ʒ�֣�������һ����С��������꣬������Ϊ����������飬��ϸ��ȱ��һ��Ⱦɫ�壬������Ⱦɫ������е�__________���죬���罫��һ����С����ͬ����С�����ӽ����õ���F1���Խ�����ֱ����F2���г���Ⱦɫ����Ŀ�����벻���������ԭ��
_________________________________________________________________________��
4����С�����⣬�ҹ�Ҳʵ������ͨС��������ԶԵ�ӽ���
����ͨС�������壩�����е�Ⱦɫ����Ϊ21�������γ�ʱ���ڼ����ڶ��η��Ѻ��ڵ�ÿ��ϸ���е�Ⱦɫ����Ϊ__________;
�ں��������е�Ⱦɫ������Ⱦɫ�������ֱ�Ϊ7��1�����������________����ֲ�
����ͨС��������ӽ���F1����ϸ���е�Ⱦɫ������Ϊ_______�� F1���ɽ�һ������С�������ַ����� ������ԭ���� ��
![]() �ʹ�һ��2008��2009ѧ��ȵ�һѧ�ڸ�������һ��
�ʹ�һ��2008��2009ѧ��ȵ�һѧ�ڸ�������һ��
![]() �����ۺ���������Ծ�
�����ۺ���������Ծ�
�����ڢ����72�֣� ��λ�ţ�
|
�� �� |
22 |
23 |
24 |
25 |
�ڢ���ܷ� |
|
�� �� |
|
|
|
|
|
22��ʵ���⣺�����2С�⣬��17�֣��Ѵ��������еĺ����ϻ���ĿҪ������
��1�� cm ��3�֣� mm��4�֣�
��2����________��_________��4�֣�
����©�����ݷֱ��ǣ� _____________________
��_ _ ________________________ ��6�֣�
�����⣨���3С�⣬����55�֣�������������Ҫ�Ĺ�ʽ�������Լ�����˵����ֻд������ܵ÷���
23. ��16�֣���1��ˮƽǣ�����Ĵ�С��(6��) ��2����������ʣ�(6��)
��3��ˮƽǣ�����Ĺ���. (4��)

24����19�֣���1�����߿��в����ĸ�Ӧ�綯�ƴ�С; (6��)
��2����cd�����ĵ��Ʋ��С; (6)
��3������ʱ�߿���ٶ�ǡ��Ϊ�㣬���߿�����ĸ߶�h��Ӧ�����������(7��)
|
P |
|
E |
|
B |
|
X |
|
Y |
|
. |
|
V0 |
|
O |
|
d |
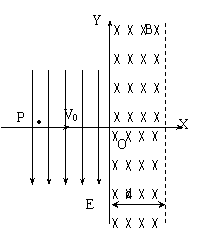
25��(20��) ��1�����������˶���Y����ʱ���ٶȵĴ�С������(10��)
��2��Ҫʹ���������ܴ�Խ�ų���������ٷ��ص��糡�У�
�ų��Ŀ������Ϊ���٣����ƴ������ӵ�������(10��)
![]() �ʹ�һ��2008��2009ѧ��ȵ�һѧ�ڸ�������һ��
�ʹ�һ��2008��2009ѧ��ȵ�һѧ�ڸ�������һ��
![]() �����ۺϻ�ѧ����Ծ�
�����ۺϻ�ѧ����Ծ�
��ѧ�ڢ����60�֣� ��λ�ţ�
|
�� �� |
26 |
27 |
28 |
29 |
�ڢ���ܷ� |
|
�� �� |
|
|
|
|
|
26����14�֣�
��1����������������ˮ�еõ���ɫ��Һ�Ͱ�ɫ������
�϶����ڵ�����
�϶������ڵ�����
����
��2��ȡ��Һ������ɫ��Ӧ������ʻ�ɫ��
�϶����ڵ�����
�϶������ڵ�����
����
��3��ȡ��ɫ��������ϡ������������ȫ�ܽⲢ�ų����塣
�϶����ڵ�����
�϶������ڵ�����
����
��4��ͨ������ʵ������ȷ����������______________��
27����15�֣�
��1��Y�������������Ļ�ѧʽΪ__________ ��
��2������5��Ԫ���У����γ�������ǿ�ĺ������Ԫ����___________��д����Ԫ�ص�����3�ֺ�
����Ļ�ѧʽ��__________________________________��
��3��D��Y�γɵĻ��������ӵĿռ乹��Ϊ____________��
��4��D ��X�γɵĻ�����仯ѧ��������___________���侧��������__________��
��5������þ��E�ĵ����ڸ����·�Ӧ�õ��IJ�����___________���˲�����ˮ��Ӧ�������ּ�÷�Ӧ�Ļ�ѧ����ʽ��____________________ ��
��6���ԱȽ�D��X�������������۵�ĸߵͲ�˵�����ɣ�
____________________________________________ _____________
28����15�֣�
��1��������װ����Լ���B_______ __ ��C____ ____��D________ ___��
��2�����Ӻ�װ�ú�Ӧ����_________________________���䷽����________________
��3�������ȷ�Ӧ��E���͡���Aƿ��εμ�Һ�塱����������Ӧ���Ƚ��е���
_________ ______����������֮�仹Ӧ���еIJ�����____________________________��
��4����Ӧ������G���ݳ���������________________��
�䴦��������____ _
��5������ʽ1��Ar(W)��____________������ʽ2��Ar(W)��____________��
29����16�֣�
��1��A�Ľṹ��ʽ��___________________����A����B�ķ�Ӧ������ ��
��2����C����D�Ļ�ѧ����ʽ��_________________________ _��
��3����E�����п��ܵĽṹ��ʽ�ǡ�___________ ____
_______________
_______________ _
��E��NaOH��Һ�п�ת��ΪF��F�ø������������Һ��������G��C8H6O4����1 mol G�������� NaHCO3��Һ��Ӧ�ɷų� 44.8 L CO2����״�������ɴ�ȷ��E�Ľṹ��ʽ��
______________ __
��4��G��������B��Ũ������¼��ȷ�Ӧ������H������G��B����H�Ļ�ѧ����ʽ��
_________________________ ��
�÷�Ӧ�ķ�Ӧ������__________________________��
�����ۺ���������Ծ� ![]()
![]()
����ڢ����42�֣� ��λ�ţ�
|
�� �� |
30 |
31 |
�ڢ���ܷ� |
|
�� �� |
|
|
|
 30.�ش��������⣮
30.�ش��������⣮
��(12��)��ͼΪ����ϸ��ɱ��ϸ����ʾ��ͼ��ͼ
�е���ø���ں��ж���ˮ��ø����ͼ�ش�
(1)ͼ�Тٹ��̽��е�����ø���ͷ�ˮ��ø����
ϸ���ֽ⣬�ù������� ���ߡ�
(2)��Щ���Ժ�ǿ��ϸ����������������Ȼ����
�ܱ�����������ڲ����ص� ���Ա���¶��
�����ʵݸ���Ӧ������ϸ����ʹ֮Ѹ����ֳ�ֻ�
�� ������ϸ������Һ�лʱ���ᱻ��Ӧ�Ŀ������������������������е� ��
(3)ͼ�Т�Ϊ�����壬���д���������ڷ�������ϸ�������йص���Ҫ��ѧ�仯����(��ͼ���ʾ)��
�� ��
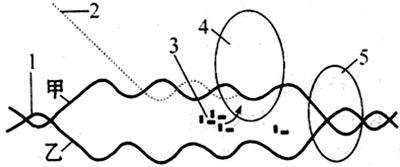
��10�֣���ͼ��ʾ��DNAΪģ��ת¼RNA�Ĺ���ͼ�⡣ͼ��4��5��ʾ���ֹ��ܲ�ͬ��ø�����ͼ�����ش��������⣺
��1��������Ҷ��ϸ���У��ܹ����иù��̵�ϸ���ṹ��Ҫ��________��
��2��ת¼�����У�DNA������[ ]___________�Ĵ������£���DNA�����м�����ڵ�___________�Ͽ����ù��̳�Ϊ___________��
��3��Ȼ����[4] RNA�ۺ�ø�Ĵ������£������еļ���Ϊģ�壬��[ ] __________Ϊԭ�ϣ���_________�ṩ����������_________________ԭ�ϳɳ�[ ] __________��
��4�������ϸ����ϸ�����У�ת¼�IJ���ͨ��________���뵽ϸ�����У���__________�����һ��ָ�������ʵ�����ϳɡ�
31.��20�֣�������Ժʿ�����2006��ȹ�����߿Ƽ���������Ҫ�ɾ���ʵ����С��ͬ��������ԶԵ�ӽ����������˶��С����Ʒ�֣���ش������й�С���Ŵ����ֵ����⣺
1.����С�������죨A�������죨a�������ԣ������ȣ�B���Բ������ȣ�b�������ԣ����Ի���������ϣ������о������������״���ӽ������У���ij�ױ���˫���ʹ������ӽ���F1����״�����Ϊ1��1����д�����ױ����ܵĻ����ͣ�___________________________��
2.�������С�����벻������һ�Ի�����Ҷ����DNA�ϣ����Կ��������벻������
��Ĵ����ױ��ӽ���Ҫ�õ�����������壬���ñ�����Ϊ____________�ĸ�����ĸ�����ô��ϵĿ�������������������________����
3.С����������Ʒ�֣�������һ����С��������꣬������Ϊ����������飬��ϸ��ȱ��һ��Ⱦɫ�壬������Ⱦɫ������е�__________���죬���罫��һ����С����ͬ����С�����ӽ����õ���F1���Խ�����ֱ����F2���г���Ⱦɫ����Ŀ�����벻���������ԭ��
_________________________________________________________________________��
4.��С�����⣬�ҹ�Ҳʵ������ͨС��������ԶԵ�ӽ���
����ͨС�������壩�����е�Ⱦɫ����Ϊ21�������γ�ʱ���ڼ����ڶ��η��Ѻ��ڵ�ÿ��ϸ���е�Ⱦɫ����Ϊ__________;
�ں��������е�Ⱦɫ������Ⱦɫ�������ֱ�Ϊ7��1�����������________����ֲ�
����ͨС��������ӽ���F1����ϸ���е�Ⱦɫ������Ϊ_______�� F1���ɽ�һ������С�������ַ����� ������ԭ���� ��
�����ۺ������ο���
ѡ������� 8С�⣬ÿС�� 6 �֣��� 48 �֡���ÿС��������ĸ�ѡ���У��е�С��ֻ��һ��ѡ����ȷ���е�С���ж��ѡ����ȷ��ȫ��ѡ�Եĵ� 6 �֣�ѡ��ȫ�ĵ� 3 �֣��д�ѡ��ĵ� 0 ��
����. D 15. C 16. B 17. ABD 18. A 19. B 20. AD 21. BC
ʵ��������17�֣�
��1 ��2.06cm��3�֣� 2.948mm��2.950mm��4�֣�
( 2 ) ��C��E (ÿ�� 2��,��4��)
��C��δ��������ϸ���ķ���
E��δ˵���Ƿ����Ƥ���Ľ��������Oλ��(ÿ�� 3�֣���6��)
�����⣨���3С�⣬����55�֣�������������Ҫ�Ĺ�ʽ�������Լ�����˵����ֻд������ܵ÷���
23. ��16�֣�����������1���Ի�����˶�ԱΪ�о�������������ͼ��ʾ
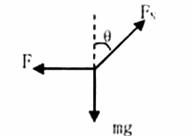 �ɹ�����ƽ�������ɵ�
�ɹ�����ƽ�������ɵ�
![]() ��(2��)
��(2��)
![]() ��(2��)
��(2��)
�ɢ١�����������F =810N (2��)
(2) ![]() (2��)
(2��)
![]() (2��)
(2��)
�� ![]() m/s (2��)
m/s (2��)
(3)ˮƽǣ�����Ĺ���
P=Fv=4050 W (4��)
24����19�֣�����������1��cd�߸ս���ų�ʱ���߿��ٶ�v= ![]() (3��)
(3��)
�߿��в����ĸ�Ӧ�綯��E=BLv��BL ![]() (3��)
(3��)
(2) ![]() ��ʱ�߿��е��� I=
��ʱ�߿��е��� I= ![]()
![]() (2��)
(2��)
cd�����ĵ��Ʋ�U=I( ![]() )=
)= ![]() (4��)
(4��)
(3)������ F=BIL= ![]() (3��)
(3��)
����ţ���ڶ�����mg-F=ma,��a=0 (2��)
�������߶����� h= ![]() (2��)
(2��)
25��(20��)�⣺�����ڵ糡������ƽ���˶�����ֱ�ٶ�Vy=at��(2��)
���ٶ� ![]() (2��)
(2��)
ˮƽλ��L=V0t�� (2��)
�����ϸ�ʽ�ý���糡ʱ�ĺ��ٶ�Ϊ ![]() �� (2��)
�� (2��)
������y���450�� (2��)
��2�����������ڴų���������Բ���˶�
![]() (3��)
(3��)
![]() �� (2��)
�� (2��)
���ұ߽�����ʱ���ɼ��ι�ϵ��Rsin450 R=d, (3��)
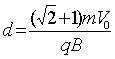
��ã�
![]()
�ʴų��Ŀ������Ϊ (2��)
�����ۺϻ�ѧ�ο���
�𰸣�6 C. 7 B. 8 D. 9 C. 10 D. 11 A. 12 B. 13 C.
26 (14��)
��l����ÿ�ո�1�֣���3�֣�
��
CuSO4
��Һ��ɫ����CuSO4��ҺΪ��ɫ
��2����ÿ�ո�1�֣���3�֣�
Na2SO4
��
�Ƶ���ɫ��Ӧ�ʻ�ɫ
��3������6�֣�ÿ�ʶ�Ӧ1�֣�
MgCO3
Ba(NO3)2 AgNO3
MgCO3��������������������ų�������Ba(NO3)2�����ɵ�BaSO4��������������������AgNO3�����ɵij����������в���ʧ��
��4����2�֣�Al2(SO4)3
27��ÿ��1�֣������ո�3�֣���15�֣�
��1��SO3 ����2��Cl��HClO HClO2 HClO3 HClO4����д 3���ᣩ
��3��ֱ���Σ���4�����ۼ� ԭ�Ӿ��壻��5��Mg3N2 ��Mg3N2ʮ8H2O = 3Mg(OH)2����2NH3��H2O
��Mg3N2ʮ6H2O = 3Mg(OH)2����2NH3��������6��D��������������CO2��X��������������SiO2��ǰ�߱Ⱥ��ߵ��۵�͡���Ϊǰ��Ϊ���Ӿ��壬�ɷ��Ӽ�����ϣ�������Ϊԭ�Ӿ��壬�ɹ��ۼ���ϣ����ۼ�ǿ�ȴ��ڷ��Ӽ�����
28 (ÿС��3�֣���15��)
��1��п���� ˮ��Ũ�����2����������ԣ�1�֣�����G��ܽ�û��ʢ��ˮ���ձ��У�������ƿB���۲�G�ܿڣ����������ݳ���˵��װ�õ����������ã���2�֣���3���ȴ�Aƿ��εμ�Һ�壨1�֣��� ����H2�Ĵ��ȣ�2�֣�
��4��������1�֣�����G�ܳ��ڴ���ȼ��2�֣���
��5�� ![]()
![]() (��1��2�֣�ȫ��3��)
(��1��2�֣�ȫ��3��)
29 ����16 �֣�
��1��2�֣�1�� ��2��2�� (3) �١�6�֣���ռ1�֡��ڡ�2��
��4��2�֣�1��
������Ӧ����ȡ����Ӧ��
�����ۺ������ο���
һ��ѡ����
1.D 2.A 3.D 4.C 5.A
������ѡ����
30����12�֣�
��1��������������
��2����ԭ������ ЧӦBϸ����ЧӦTϸ��������ϸ�� ��Һ����
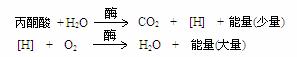 ��3����ÿ����Ӧʽ2�֣�
��3����ÿ����Ӧʽ2�֣�
��10�֣�
��1��ϸ���ˣ�
��2��5����ø�����������
��3��3��������ĺ��Ǻ����ATP�����������ԣ�2��ʹRNA
��4���˿ף�������
31��20��ÿ��2��
1��AaBB��Aabb��AABb��aaBb
2���������죻F2�����Ӷ�����
3����Ŀ ԭ��F1��ͨ�����������ܲ��������벻�������������ӣ�
�����������ϲ���������F2�����������������ϡ�����������
���������ӽ�ϲ�����������F2��
4���� 42 �� 2 ��4 ������� Ⱦɫ�����
| |