|
���Ծ��ֵڢ��(ѡ����)�͵ڢ�����ڢ����Ϊ�ؿ��⣬�ڢ�������ؿ���ѡ���������֡�ȫ������300�֣����ʱ��150���ӡ�
���ԭ������(ԭ����)��H 1 C 12 N 14 O 16 K 39 Cl 35.5
������(�ؿ�)
һ��ѡ����(���12С�⡣��ÿС��������ĸ�ѡ����ֻ��һ��ѡ�������ĿҪ��)
1�����й���ϸ���ڵ�������֬�ʵ���������ȷ���ǣ� ��
A���̴���������ϸ����Ӫ�������ںʹ�л�о�����Ҫ����
B��֬���е���֬�ǹ���ϸ��Ĥ����Ҫ���ʣ�����ϸ����������֬
C������������ά�����������Ҫ�������ʣ�Ҳ����������Ҫ�Ľṹ����
D��ֲ��ϸ���еĶ�����Ҫ�ǵ��ۺ���ά�أ�����ϸ���еĶ�����Ҫ�����Ǻ���Ԫ
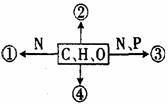 2����ͼΪϸ���ڲ�ͬ��ѧԪ����ɵĻ�����ʾ��ͼ������˵����ȷ���ǣ� �� 2����ͼΪϸ���ڲ�ͬ��ѧԪ����ɵĻ�����ʾ��ͼ������˵����ȷ���ǣ� ��
A������Ϊ�������ӣ����䳹��ˮ��IJ�����4��
B�����ڴ���������Ƥ�º������������ܣ��������֬
C��������Ҫ���������ͼ����ںϳɣ�������������Ԫ
D����ͼ�Т�Ϊij�ֻ�����Ļ�����λ�����������Ǻ�����
3�����й����������������ڵ�������ȷ���ǣ� ��
A��һ��Ũ�ȵ�2��4��D���Դٽ�Ǥ���֦������
B��һ��Ũ�ȵ���������������Һ���Դٽ���ʵ����
C��������Ԫ����Ϣ�Ĵ�����ͨ���������ʽ��ɵ�
D��è����Ĺ����У��˷����˶�����ά�ϵĴ�����˫���
4�����й�������Ĥ�ṹ���ܵ�������ȷ���ǣ� ��
A��ϸ���ˡ������塢Ҷ���嶼����˫��Ĥ���������ǵ�ͨ������ͬ��
B������Ĥ���������ԣ�ʹĤ���ѱ�������Ľṹ�����������ʽ���
C����������Ĥ�Ľṹ������������DZ��������ʡ���֬˫���Ӳ����
D������Ĥ�ڽṹ�����ϵĽ�����ϵ����ϸ����Ϊ�л�����ı�Ҫ����
   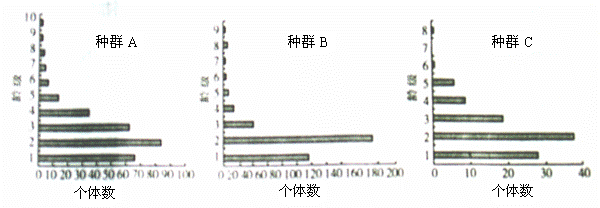 5���о���Ա���ݻ�ɼ�ؾ��Ĵ�С�����˲�ͬ�伶������ȺA(��Ȼ״̬)����ȺB��C(��ͬ��Ϊ����ǿ��)������ȡ�����飬�������ͼ���ɴ˵ó��Ľ�������ȷ����( ) 5���о���Ա���ݻ�ɼ�ؾ��Ĵ�С�����˲�ͬ�伶������ȺA(��Ȼ״̬)����ȺB��C(��ͬ��Ϊ����ǿ��)������ȡ�����飬�������ͼ���ɴ˵ó��Ľ�������ȷ����( )
A���ʶȵ���Ϊ���ŶԵ����ɼ��������Ϊ����
B����ȺA�и��伶�������У�Ӫ������������������ȶ�
C����ͬ��Ϊ���������£���ɼ��Ⱥ������Ϊ������
D����ȺC�и��伶��ɼ��Ŀ�������ʱ���������ڶ�����������
6��2005��4��22���ǵ�36������������ա����ҹ�������Դ��ȷ�����ꡰ��������ա�������Ϊ���ƴ�����ѧ��չ��������г��������Ϊ������Ϊ�в�������һ�������( )
A������̫���ܡ�ˮ�ܡ����ܡ���ȼ��������Դ������ʹ��ú��ʯ�͵Ȼ�ʯȼ��
B�����ƺ�����������ʹ�ã���ֹˮ�帻Ӫ����������ˮ��Դ
C���о���ú�������¼�����������߲��������㹤ҵ�����Ŀ��ٷ�չ
D��ʵ����Դ�ġ�3R�����ùۣ�����������Դ���ģ�Reduce����������Դ���ظ�ʹ�ã�Reuse������Դ��ѭ��������Recycle��
7�����и����Լ�����Һ�з�Ӧ���������Լ����������ı�ʱ��������ͬһ���ӷ���ʽ��ʾ����( )
A���Ȼ�þ���������� B�������ơ��������� C���Ȼ�������ˮ D���廯��������ˮ
8��20��ʱ����KCl��Һ���ܶ�Ϊ1.174 g/cm3�����ʵ���Ũ��Ϊ4.0 mol/L��������˵���д������( )
A��25��ʱ������KCl��Һ��Ũ�ȴ���4.0 mol/L B������Һ��KCl����������Ϊ 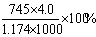
C��20��ʱ���ܶ�С��1.174 g��cm��3��KCl��Һ�Dz�������Һ
D��������Һ��������ˮ���ٻָ���20��ʱ����Һ�ܶ�һ������1.174 g/cm3
9����������AlN���������¡�������������Ժõ��������ʣ����㷺Ӧ���ڵ��ӹ�ҵ���մɹ�ҵ��������һ�������£���������ͨ�����·�Ӧ�ϳɣ�Al2O3 N2 3 C 2 AlN 3 CO ����������ȷ����( )
A���ڵ������ĺϳɷ�Ӧ�У�N2�ǻ�ԭ����Al2O3��������
B��������Ӧ��ÿ����2 mol AlN��N2�õ�3 mol����
C���������е�Ԫ�صĻ��ϼ�Ϊ��3
D���������������ڷ��Ӿ���
10�����и��������У�һ���ܴ����������( )
A������������������������Һ�У�H ��K ��NO3����C1��
B��pH = 0����ɫ��Һ�У�Na ��K ��MnO4����NO3��
C����0.1mol��L�Ĵ�����Һ�У�Fe2 ��Na ��ClO����Ca2
D��ij��ɫ������Һ�У�Cl����SO42����Na ��Mg
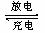 11�����������һ�����Ϳɳ���أ�����ͨ���ܵ����ȣ��õ���ܳ�ʱ�䱣���ȶ��ķŵ��ѹ��������ص��ܷ�ӦΪ�� 11�����������һ�����Ϳɳ���أ�����ͨ���ܵ����ȣ��õ���ܳ�ʱ�䱣���ȶ��ķŵ��ѹ��������ص��ܷ�ӦΪ��
3Zn 2K2FeO4 8H2O 3Zn(OH)2 2Fe(OH)3 4KOH
������������ȷ����( )
A���ŵ�ʱ������ӦΪ��Zn �� 2e�� 2OH�� == Zn(OH)2
B�����ʱ������ӦΪ��Fe(OH)3 �� 3e�� 5OH�� == FeO42�� 4H2O
C���ŵ�ʱÿת��3moL���ӣ�������1 mol K2FeO4������
D���ŵ�ʱ����������Һ�ļ�����ǿ
12����0.1mol/L CH3COOH��Һ�м���CH3COONa�����ӵ����ˮϡ��ʱ���������� ��
A����Һ��pH���� B��CH3COOH�ĵ��������
C����Һ�ĵ���������С D����Һ��c (OH �C )��С
����ѡ����(���6С�⡣��ÿС��������ĸ�ѡ���У��е�ֻ��һ��ѡ����ȷ���е��ж��ѡ����ȷ��ȫ��ѡ�Եĵ�6�֣�ѡ�Ե���ȫ�ĵ�3�֣��д�ѡ�ĵ�0�֡�)
13������˵����ȷ����( )
A��ţ��֧�ֹ�IJ���˵ B�����ƫ������˵������һ�ֺᲨ
C�����������ǹ�ĸ��������γɵ� D���������ϵIJ�ɫ�ǹ��ɫɢ�����γɵ�
14��������ѹ��ԭ������Ȧ����һ����ͬ���������ǣ��� ��
 A��������Ƶ�ʡ��� B�������Ĺ��� A��������Ƶ�ʡ��� B�������Ĺ���
C����ͨ���ı仯�ʡ� D�����������ֵ
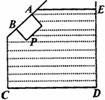
15����ͼ��ʾ������ʢ��ˮ������AB����б״����һ��С���P����ͼʾλ�ã������־�ֹ״̬������������������ȷ���ǣ��� ��
A��P����ֻ��һ���� B��P������������
C��P������ֻ�ܶ����� D��P�����ܵ������������ܵ��ĸ���
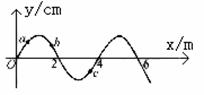 16����ͼ��ʾΪһ��г����tʱ�̵�ͼ����֪�ʵ�a�����ʵ�b�Ȼص�ƽ��λ�ã�������˵����ȷ���ǣ� �� 16����ͼ��ʾΪһ��г����tʱ�̵�ͼ����֪�ʵ�a�����ʵ�b�Ȼص�ƽ��λ�ã�������˵����ȷ���ǣ� ��
A������x������ B���ʵ�a�ļ��ٶ���������
C���ʵ�b�ٶ��������� D���ʵ�c�ļ��ٶ���������
17������Ϊm�����壬��F�����´Ӿ�ֹ������ 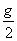 �ļ��ٶ���ֱ����h���ڸù����У�AC �� �ļ��ٶ���ֱ����h���ڸù����У�AC ��
A������Ļ�е�ܼ�С 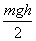 B������Ļ�е������ B������Ļ�е������ 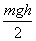
C������Ķ������� 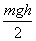 D��F���������� D��F���������� 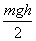
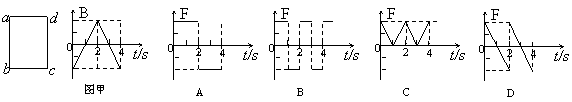 18�����ε��߿�abcd������ǿ�ų��У������������¾�ֹ�������Ÿ��߷�������Ȧƽ�洹ֱ���Ÿ�Ӧǿ��B��ʱ��仯��ͼ����ͼ����ʾ.t=0ʱ�̣��Ÿ�Ӧǿ�ȵķ���ֱֽ�������0��4sʱ���ڣ��߿�ab������ǿ�ų�����������ʱ��仯��ͼ��(���ķ���涨������Ϊ������)��ͼ�еģ� �� 18�����ε��߿�abcd������ǿ�ų��У������������¾�ֹ�������Ÿ��߷�������Ȧƽ�洹ֱ���Ÿ�Ӧǿ��B��ʱ��仯��ͼ����ͼ����ʾ.t=0ʱ�̣��Ÿ�Ӧǿ�ȵķ���ֱֽ�������0��4sʱ���ڣ��߿�ab������ǿ�ų�����������ʱ��仯��ͼ��(���ķ���涨������Ϊ������)��ͼ�еģ� ��
������
�ؿ�����(�ڢ���ؿ����ֹ�9�⣬��157�֡�)
19��(����ж�С�⣬��18��)
(1)(6��)��ͼ��ʾ�ļס�����ͼ��ʾ��ͬһ�����IJ�������P�볤�������Ķ�Ħ�����������ֲ�ͬ��������ͼʹ�����徲ֹ��ˮƽ�����ϣ�����ͨ�����ɳ���������F��P��ʹP�����˶�����ͼ�ѵ��ɳӵ�һ�˹̶���ǽ�ϣ�����Fˮƽ�����������壬ʹ�����������˶���
= 1 \* GB3 �������ֲ�������Ħ�����ķ�����һ�ָ���һЩ���� (ѡ��ס����ҡ�)��
= 2 \* GB3 ��ͼ���Ѱѣ��ף������ң����ַ����е��ɳӵ�ʾ������Ŵ�������������P������Ϊ50N��������P�������Q��Ķ�Ħ�������Ĵ�С�� ��
(2)(12��) ��һ��ϸ�����ȵĵ��������Ʒ������Ϊͬ��Բ������ͼ��ʾ������Ʒ��LԼΪ3 cm������ԼΪ100������֪���ֲ��ϵĵ�����Ϊ 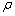 ����Ҫ��������Ʒ���ھ��������Ʒ���ھ�̫С����ֱ�Ӳ��������ṩ����ʵ�����ģ�ͨ����Ӳ����õ�����Ʒ�ھ�d�� ����Ҫ��������Ʒ���ھ��������Ʒ���ھ�̫С����ֱ�Ӳ��������ṩ����ʵ�����ģ�ͨ����Ӳ����õ�����Ʒ�ھ�d��
 A��20�ȷ̶ֿȵ��α꿨�� B���������� A��20�ȷ̶ֿȵ��α꿨�� B����������
C��������A1������50 mA�������ȷֵr1Ϊ100����
D��������A2������100 mA������r2��ԼΪ40����
E������������R1��0 ~ 10���������2 A��
F��ֱ������E��12 V�������С��
G�����������ƷR2����LԼΪ3 cm������R2ԼΪ100����
H�����Sһֻ����������
����������������һ�������ܾ�ȷ�ز�������Ʒ�ھ�d��ʵ�鷽�����ش��������⣺
�����α꿨�߲�ø���Ʒ�ij�����ͼ����ʾ����ʾ��L = ________cm��������������ø���Ʒ���⾶��ͼ����ʾ����ʾ��D = _________mm��
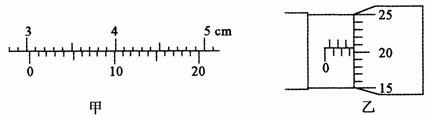
�������Ϸ��ķ����������������������Ʒ��ֵR2�ĵ�·ͼ��������صĵ�·Ԫ���ϻ��Ա߱�����ѡ���ĵ���ĸ����(�磺A1��A2��R1��R2��E��)��
�������������Ʒ��ֵΪR2������ΪL���⾶ΪD��������Ϊ 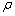 �����⼸���������ķ��ű�ʾ��Ʒ���ھ�d�ı���ʽΪd= �� �����⼸���������ķ��ű�ʾ��Ʒ���ھ�d�ı���ʽΪd= ��
20��(16��)�ҹ�����ġ����ۡ�ϵ�к���ɴ�����־�ҹ����켼���ﵽ�µ�ˮƽ�����е�һ�ҷɴ�����ΪM���Ƶ������е�����ΪT����֪����İ뾶ΪR��������������ٶ�Ϊg��������������ΪG��ɴ��Ƶ���������Բ���˶����������ṩ����Ϣ������������⣺
(1)�÷ɴ������ĸ߶�Ϊ����?
(2)�÷ɴ��Ƶ�����е��ٶ��Ƕ��
(3)���˲��ڽ�Ҫ��½֮ǰ�����ڿ�������������һ������������̣��������������ٶ�ƽ�������ȣ�����ϵ��Ϊk�����˲յ�����Ϊm���������������������˲յ��ٶȶ��
 21��(18��)��ͼ��ʾ����ֱ���õİ�Բ�ξ�Ե����뾶ΪR���¶����Եˮƽ��ƽ�����ӣ�����װ�ô��ڷ�����ֱ���ϵ���ǿ�糡��E�У�һ����Ϊm��������Ϊ q����飨����Ϊ�ʵ㣩����ˮƽ���ϵ�A���Գ��ٶ�v0ˮƽ�����˶����ذ�Բ�ι���˶�ǡ 21��(18��)��ͼ��ʾ����ֱ���õİ�Բ�ξ�Ե����뾶ΪR���¶����Եˮƽ��ƽ�����ӣ�����װ�ô��ڷ�����ֱ���ϵ���ǿ�糡��E�У�һ����Ϊm��������Ϊ q����飨����Ϊ�ʵ㣩����ˮƽ���ϵ�A���Գ��ٶ�v0ˮƽ�����˶����ذ�Բ�ι���˶�ǡ
��ͨ����ߵ�C�������Ĵ���������Ħ�����仯����ǿ��СΪE
��E<mg/q������
(1)�����C���ļ��ٶȴ�С��
(2)����ڴ�A��C�˶������п˷�Ħ�������Ĺ���
(3)����뿪������ˮƽ����̵�ˮƽ���еľ��롣
22��(20��)ij��������Ϊ������Դ�Ļ���������������(��������Ա)m=3��103kg��������ˮƽ·������V=36km/h���ٶ�������ʻʱ������������������I=50A����ѹU=300V���ڴ���ʻ״̬�£���
(1)��������������빦��P�磻
(2)����������ܹ������빦�ʵ�90%ת��Ϊ����ǣ������ǰ���Ļ�е����P�������������������복�صı�ֵk��gȡ10m/s2����
(3)���һ�������������������ʹ��Ч�ʵĺ��������飻
(4)�������̫���ܵ�ظ��ó����磬�����������䣬�������̫���ܵ�ذ����С�������ϼ�������������Ը���������Ե�˼����
��֪̫��������ܹ��� 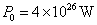 ��̫��������ľ��� ��̫��������ľ��� 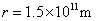 ��̫���������������Ĺ����д�Լ��30%��������ģ��ó�����̫���ܵ�ص�����ת��Ч��ԼΪ15%�� ��̫���������������Ĺ����д�Լ��30%��������ģ��ó�����̫���ܵ�ص�����ת��Ч��ԼΪ15%��
23��(14��)��A��B��C��D���ֶ�����Ԫ�أ�A��B��CΪͬһ�����������ڵ�3��Ԫ�أ�A��C��ԭ������֮��Ϊ3��4����A��B��C�ֱ���D�γ����ֻ�������������ĵ�������ȣ���ش�
��X��Y��Z��W����������Ԫ���е�������ɵĻ������X���ӵĿռ乹��Ϊ�����ͣ���X�ĵ���ʽΪ ����֪Y����Ϊ��ɫ��������Z��Y������ͬ�ĵ�������������Һ̬ʱ��һ����Ϊ����ƽ�����ȼ�ϣ�����֪0.8gZ��Y��Ϊ����ƽ���ʱ���ܷų�20.44KJ�������������Ϊ��̬������д���÷�Ӧ���Ȼ�ѧ����ʽ��
W����ѧ��ѧ�г��������ʣ�����ӵĿռ乹��Ϊֱ���ͣ��������е�ԭ��������2��������ܵĻ�ѧʽΪ �� ��ֻҪд��2������
�Ƽס��Ҷ���������Ԫ���е�������ɵ����ʣ���ΪʳƷ�г�������Ȼ�߷��ӻ������ʾ����ɵĻ�ѧʽΪ �������������࣬��ˮ��Һ���������ԣ����ҵĻ�ѧʽΪ ��
24����16�֣��ش����Т���С��
������ʵ��������ʵ����ʵ��������ȷ���� (�����)
�ٽ�������ˮ�ɼ�������ǡ�����ͭ��̼������ַ�ĩ��
��ʵ���������Ȼ�������Һʱ�����Ȼ��������ܽ��������У�Ȼ��������ˮϡ�Ͳ������������ۣ�
������һ��Ũ�ȵ���Һʱ����������ƿ�Ŀ��ߣ���ʹ���Ƶ�Ũ��ƫ�ͣ�
���ô������ۻ������ƵĻ����
�ݷ�Һʱ���ȴӷ�Һ©���е����ϲ�Һ�壬��ų��²�Һ�壻
����Һ���µ�pH���ò�����պȡ��Һ����ʪ���pH��ֽ�ϣ������ɫ�����գ�
�� ��ˮ�еμ�Al2(SO4)3��Һ����Al2(SO4)3��Һ�еμӰ�ˮ������ͬ��
��ֱ��������pH����ͬ�������ʹ����еμӵ�Ũ�ȵ�����������Һ����ȫ�к�ʱ���ĵ�����������Һ�����ǰ���٣����߶ࡣ
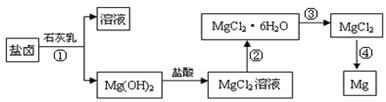 ��þ����Ͻ���һ����;�ܹ�Ľ������ϣ�Ŀǰ������60%��þ�ǴӺ�ˮ����ȡ�ġ�ijѧУ���Ⱞ��С��Ӻ�ˮɹ�κ����±(��Ҫ��Na ��Mg2 ��Cl����Br����)��ģ�ҵ��������ȡþ����Ҫ�������£� ��þ����Ͻ���һ����;�ܹ�Ľ������ϣ�Ŀǰ������60%��þ�ǴӺ�ˮ����ȡ�ġ�ijѧУ���Ⱞ��С��Ӻ�ˮɹ�κ����±(��Ҫ��Na ��Mg2 ��Cl����Br����)��ģ�ҵ��������ȡþ����Ҫ�������£�
�ش��������⣺
(1) ��ҵ�ϴ���±�л�ȡMg(OH)2��ʯ���������NaOH��Һ��ԭ����
��
(2) �ӹ��̢ٵõ���Mg(OH)2�����л���������Ca(OH)2 ����ȥ����Ca(OH)2�ķ������Ƚ��������뵽ʢ�� ��Һ���ձ��У���ֽ���� �� (���������)�ɳ�ȥCa(OH)2��
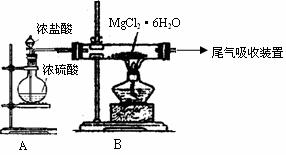 (3)��ͼ�Ǹð���С����ƽ��й��̢۵�ʵ��װ��ͼ�� (3)��ͼ�Ǹð���С����ƽ��й��̢۵�ʵ��װ��ͼ��
����װ��A�������ǣ� ��
(4)д�����̢��з�����Ӧ�Ļ�ѧ����ʽ ��
25����15�֣���֪2A2(g) B2(g)  2C3(g)����H=-a kJ/mol��a ��0������һ���д����Ĺ̶��ݻ��������м���2mol A2��1mol B2����500��ʱ��ַ�Ӧ��ƽ���C3��Ũ��Ϊw mol/L���ų�����b kJ�� 2C3(g)����H=-a kJ/mol��a ��0������һ���д����Ĺ̶��ݻ��������м���2mol A2��1mol B2����500��ʱ��ַ�Ӧ��ƽ���C3��Ũ��Ϊw mol/L���ų�����b kJ��
(1)�Ƚ�a____________b���������������
(2)�˷�Ӧ��ƽ�ⳣ������ʽΪ________________________��������Ӧ�¶����ߵ�700�棬��Ӧ��ƽ�ⳣ����_____________������С�䣩
(3)����ԭ���������У�ֻ����2mol C3��500��ʱ��ַ�Ӧ��ƽ�����������ckJ��C3Ũ��________�������������w mol/L��a��b��c֮��������ֹ�ϵ__________________���ô���ʽ��ʾ��
(4)Ϊʹ�÷�Ӧ�ķ�Ӧ����������ƽ��������Ӧ�����ƶ�����__________��
a����ʱ�����C3���� ��b���ʵ������¶ȣ�c������B2��Ũ�� ��d��ѡ���Ч�Ĵ���
(5)��������������Ϊ��ѹ��������Ӧǰ�����ͬ������ʼʱ����2mol A2��1mol B2��500��ʱ��ַ�Ӧ��ƽ��ų�����dkJ����d___b���������������������_________________��
26���ش����Т��⣨25�֣���
���Ķ����в��ϲ��ش����⣺��10�֣�
��ʳ��ƻ����������У����ῴ�����۵Ĺ���ܿ�ͱ�ɰ���ɫ��������Щֲ��ϸ������ڵķ������ʷ����˻�ѧ�仯������ֲ��ϸ���������ø���������Ƿֿ���ŵģ�������֯ϸ�������˥�ϣ��ṹ����ʱ��������ø���л�����������Ӵ���ʹ�����������غ�ɫ�����ʡ�
��1����������������ֲ��ϸ���������ø���������Ƿֿ���ŵġ���һ����������ϸ���ھ��� ��Ե�ʡ����֡��ֿ���š�������Ҳ����ϸ�������ֽṹ�������ʵ�ͨ������ �����ԣ���������������ϸ���ڵ� �����ġ�
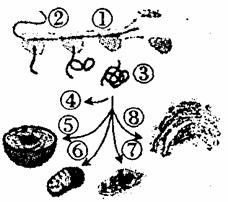 ��2��ϸ�����з�����ø���������÷�����ø�����Կɼӹ�������Ʒ�����磬�����ȡ�����б����С���ϸ�����ơ���Ҫ�����̣������ɫΪ��ɫ��������ϸ���Ŀ���Ŀ���� ���̲���ȡ�����б������ȹ����Ƶ�Ҫ�����̣��̲���ɫΪ��ɫ�����ȹ����ƵĿ���Ŀ���� �� ��2��ϸ�����з�����ø���������÷�����ø�����Կɼӹ�������Ʒ�����磬�����ȡ�����б����С���ϸ�����ơ���Ҫ�����̣������ɫΪ��ɫ��������ϸ���Ŀ���Ŀ���� ���̲���ȡ�����б������ȹ����Ƶ�Ҫ�����̣��̲���ɫΪ��ɫ�����ȹ����ƵĿ���Ŀ���� ��
������ͼΪһϵ�з�����������ϸ���е���������ʾ��ͼ�����ͼ�ش𣺣�15�֣�
(1)�㶹Ҷ��ϸ���ϳɢ�mRNA�ij����� �Ƚṹ�У����п����������κ;��߶ȵĻ���λ�� �С�
(2)ֱ�Ӿ������а����������˳����� ����ͬһֲ����IJ�ͬ��λ��ϸ���У��۵����ͬ��ԭ���� ������Ϊ�������Ƿֽ�Ϊ��ͪ���ø����ܵ����ó����� �С�
(3)Ҷ�����дֵ����ʵĺϳɳ����� ��������мӹ��ij����� ��
27.��15�֣��������״������һ�Ի��Ի�����ơ��о���������ɫ�Ŵ����ü����������ӽ���F1ȫΪ���磬F1�Խ������в��������Խ���������������ı������ӽ�9:7
�� ��������ɫ���Ŵ��Ƿ�����ϵ¶����Ŵ����ɣ� ���������A��a ��B��b����ĸ�ֱ��ʾ��λ����������F1��������Ļ�����Ϊ ��
�����������ӽ�9:7��ԭ�����������Ľ��͡�
 ���������ڣ�������ԭ��Ӱ�촫�۵��¼�������ͨ��������������������������ʧ���ⷽ���Ƿ���У��Լ������ɡ� ���������ڣ�������ԭ��Ӱ�촫�۵��¼�������ͨ��������������������������ʧ���ⷽ���Ƿ���У��Լ������ɡ�
ѡ������
�ڢ��ѡ�����ֹ�5�⣬��35�֡����У���28��29��Ϊ�����⣬��30��31��Ϊ��ѧ�⣬���������������⡢������ѧ���и�ѡһ����������28��29�ⶼ������28��Ʒ֣�����30��31�ⶼ������30��Ʒ֣���32��Ϊ�����⣬�DZش��⡣�뽫�𰸶���д�ڴ��ѡ�������ָ��λ���ϡ�
28�������� ѡ��3-3�� (��С�����С�⣬ÿС��6�֣���12�֡�ÿС��ֻ��һ��ѡ��������⡣)
(1) ���Ӽ�����������ܣ��涨�������������Զʱ�����Ӽ������Ϊ�㡣�����a�̶�����������b��ijһ���ٶȴ�����Զ����a�˶���ֱ������֮��ľ�����С���ڴ˹����У�a��b֮������� ��
���ȼ�С�����������С���� ���ȼ�С����������������
������������������ �������������������
(2) ��ͼ��ʾ�����ȸ���K�Ѿ��ȵ����ָ��������ȵ������֣�K�����ױڵĽӴ��ǹ⻬�ġ��������зֱ�ʢ����ͬ��������ͬ�¶ȵ�ͬ������a��b���������֮����������ܿɺ��ԡ���ͨ������˿������a����һ��ʱ���a��b���Դﵽ�µ�ƽ������ ��
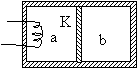 ��a����������ˣ�ѹǿ��С�� ��a����������ˣ�ѹǿ��С��
��b���¶ȱ��ֲ���
�ۼ��Ⱥ�a�ķ������˶���b�ķ������˶�������
��a���ӵ����ܵ���b���ӵ�����
29�������� ѡ��3-5��(��С�����С�⣬ÿС��6�֣���12�֡�ÿС��ֻ��һ��ѡ��������⡣)
(1)��A��B����������ɵ�ϵͳ�ܶ����غ㣬����˵����ȷ���� ��
��A��Bһ��������ϵͳ���������� ��ϵͳ����һ����A��B��������
��ϵͳ������A��B�����ܹ�һ��Ϊ�� ��ϵͳ������A��B�������ܳ���һ��Ϊ��
(2) һ�����Ӻ�һ�����ӽ�ϳ�뮺�, ͬʱ�ų������ӣ��˷�Ӧ������ 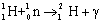 ������˵������ȷ���� �� ������˵������ȷ���� ��
�ٷ�Ӧ��뮺˵�����һ�����ڷ�Ӧǰ���Ӻ����ӵ�����֮��
�ڷ�Ӧǰ������������䣬�����������
�������ӵ�����Ϊ��mc2����mΪ��Ӧ�е���������cΪ��������е��ٶ�
���������������m�����ԡ����ʲ��𡱵�˵������ȷ
30��[��ѧ ���ʽṹ������]��13�֣���ԭ������С��20��A��B��C��D��E��F����Ԫ�أ����ǵ�ԭ������������������BԪ���ǵؿ��к�������Ԫ�ء���֪A��C�ļ۵�������ͬ��B��D�ļ۵�����Ҳ��ͬ����A��C��Ԫ��ԭ�Ӻ��������֮����B��D��Ԫ��ԭ�Ӻ���������֮�͵Ķ���֮һ��C��D��E����Ԫ�صĻ�̬ԭ�Ӿ�����ͬ���ܲ�������Eԭ�ӵ�p�ܼ��ϵ�������Dԭ�ӵ�p�ܼ��϶�һ�����ӣ�����Ԫ�صĻ�̬ԭ���У�Fԭ�ӵĵ��Ӳ�������Һ�A����ͬһ���塣�ش��������⣺
��1���õ���ʽ��ʾC��E�γɻ�����Ĺ��� ��
��2��д����̬Fԭ�ӵĺ�������Ų�ʽ ��
��3��д��Aԭ����Dԭ���γ�A2D���ӹ�����Dԭ�ӵĹ���ӻ����� ��
��4��A2B������ɵľ����ڣ����Ӽ�������Ϊ ��
31��[��ѧ �л���ѧ����]��13�֣��������ճ������г��õĺϳɸ߷��Ӳ��ϣ���������F��G������ij�������з�Ӧ�õ���
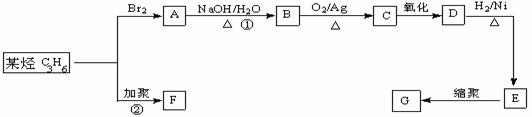
��1��д���߷��ӻ�����G�Ľṹ��ʽ��_____________________��
��2��д����Ӧ�ٵĻ�ѧ����ʽ��_________________________________________��
��3��д����Ӧ�ڻ�ѧ����ʽ��_____________________________________________��
��4��PBT�� 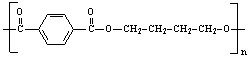 ����һ������Ҫ�Ĺ�������֮һ�� ����һ������Ҫ�Ĺ�������֮һ��
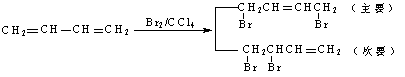
��֪���� 
�� 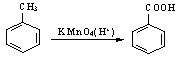
����Ʒ�����CH2=CHCH=CH2�� 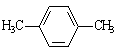 Ϊԭ�Ϻϳ�PBT�����÷�Ӧ����ͼ��ʾ����ע����Ӧ������ Ϊԭ�Ϻϳ�PBT�����÷�Ӧ����ͼ��ʾ����ע����Ӧ������
ʾ�������Ҵ��ϳɾ���ϩ�ķ�Ӧ����ͼ�ɱ�ʾΪ
CH3CH2OH  CH2��CH2 CH2��CH2   CH2��CH2 CH2��CH2 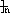
�ϳ�PBT�ķ�Ӧ����ͼΪ__________________________________________________
32�������� �ִ�����Ƽ�ר���(10��) Ӣ����λ��ѧ������̥��ϸ���о�����ġ�������������2007��ŵ��������ѧ��ҽѧ������ͼΪij����С����øü����Ƚ�ij���ص���ɫӫ�⵰������С�����̥��ϸ����ESϸ�����У��ٽ���������̥��ϸ����ֲ�����ߣ�����̥��ֲ����������С��Ĺ��̡����ͼ�����ش�
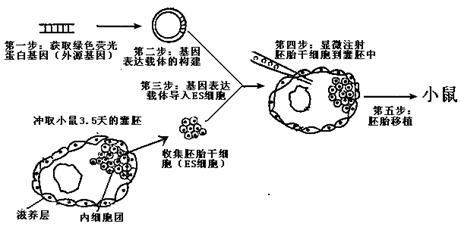
(1)��������������ɣ�����Ŀ�Ļ����⣬�������������ӡ���ֹ�Ӽ���ǻ���ȣ�������������_______________ʶ��ͽ�ϲ�λ��������Ŀ�Ļ���ת¼��mRNA��
(2)���ռ�����̥��ϸ����Դ�����ߵ�_______________��λ��ϸ����
(3)�ڵ��IJ�֮ǰ��Ҫ�����ɫӫ�⵰�����Ƿ������̥��ϸ��Ⱦɫ���DNA�ϣ���ⷽ���ɲ���______________������
(4)�ڵ��岽��̥��ֲʱ����Ҫ��ö��������ͬ�Ŵ����ʵ���̥��ͨ�����õļ�����_________��
(5)��̥��ֲ��Ҫ������������_______________��飬��ȷ����ֲ�Ƿ�ɹ���
(�����ˣ� ���� ������ ��ѧ ������ ���� ��ӭ�� )
|