| ��������: �Ž�����.com������������
Ӣ��������www.1-123.com�����������ḻʵ�õĽ�����ѧ���� |
| |
| |
| |
|
|
A��1��2��3��4�ı����Ͷ�һ�� B���ڴ˱����У�RRYYֻ����һ�� C���ڴ˱����У�RrYy�������Ĵ� D�������ͳ��ֻ��ʵĴ�С˳��Ϊ4>3>2>1 4.�ס��ҡ��������ֱ�Ϊ��ɫֲ���³´�л�������йر仯ʾ��ͼ�������������
A��ͼ���Ǻ��ܲ��ڲ�ͬ�ĺ�������´��������Һ������ B��ͼ�ұ�ʾҰ�������������ǿ�������ǿ�ȵĹ�ϵ��������ǿ��Ϊbʱ���������ǿ�ȴﵽ��� C��ͼ����ʾ����������Ũ�ȶ�ֲ����֯��CO2������Ӱ�죬Ϊ�������������߲˺�ˮ�����������ڵ�����Ӧ���ڵ�ͼ��B������Ӧ��Ũ�� D��ͼ����ʾ�㶹�����ȷ�ʱ��ˮ����ʱ��ı仯��ϵ����ѧ���о����֣��ڵڢ��������O2��������������CO2���ͷ������ʵڢ��ϸ������ǿ������ 5.Na -K ����4�ǻ������ģ���ɣ�����һ���ǻ�����ϸ���ʵ�һ����һ��ATP���λ�� ��������Na ���λ�㣬�����������K ���λ�㡣��һ��������ATP���ܣ���Na ��ϸ ������Ũ���ݶ��ų�����K ��ϸ������Ũ�����������롣�Դ˹��̵IJ���ȷ��˵���� �� �� A��Na ��K ����ϸ������������Ĺ��� B��Na -K ����һ����ͬʱ����ת���������ӵ����嵰�ף��ù�����ϸ��Ĥ��ѡ������ �� C��˵��ϸ��Ĥ����һ���������� D����һ���̿��ܻ����ϸ��Ĥ���������λ�� 6.���й����������������ȷ���� ������������϶����ǽ��������� ���ǽ���������϶������������� �ۼ���������϶��ǽ��������� �ܽ��������ﶼ�Ǽ��������� ���������������H2O��Ӧ������Ӧ���� ����H2O��Ӧ������������ﲻһ�������������� �߲������ᷴӦ��������һ������Ӧ A���٢ڢۢ� B���ݢޢ� C���ڢۢޢ� D���ۢ� 7.��NAΪ�����ӵ�����ֵ�����������в���ȷ���� A��12.4g�������к��е�P��P������0.6 NA B��2.9g2CaSO4��H2O ���еĽᾧˮ������Ϊ0.02 NA C��100 g��98%��Ũ H2SO4����������ԭ����Ϊ2 NA D��2mol SO 2��1mo lO 2 �����V2 O 5���ڵ��������ܱ������м��ȷ�Ӧ��,���������ʷ���������2 NA 8.�������ʵ�����F2��ClF��ϣ����ܱ������з�����Ӧ�� F2(g) ClF(g)�PClF3(g)����H<0�� ���������У���ȷ���� A�����º���ʱ����ClF ת��40% ʱ�������ڵ�ѹǿΪ��ʼʱ��0.8 �� B���� c(F2):c (ClF): c (ClF3) =1: 1: 1�� ��Ӧһ���ﵽƽ��״̬ C���ﵽƽ������������������������Ӧ���ʼ�С���淴Ӧ��������ƽ������ D��ƽ����ٽ����¶ȣ����ֺ��ݣ��ﵽ�µ�ƽ�⣬���������ƽ��Ħ���������ܼ�С 9.X��Y�������������о�ʢ��25ml2mol/l NaOH��Һ����X ��ͨ��560ml����״����CO2����Y�����м���1.1g�ɱ�������ȫ��Ӧ����������У�����˵����ȷ���ǣ� �� A����������c(Na )����� B���������ڶ���c(Na )=2c(CO32��) C���������ڸ�������Ũ�Ⱦ���c(Na ��>c(CO32��)>c(OH��)>c(HCO3��)> c(H ) D��X����Һ��PH����Y����Һ��PH 10.�ö��Ե缫���һ��Ũ�ȵ�CuSO4��Һʱ��ͨ��һ��ʱ��������õ���Һ�м��� 0.1mol Cu2��OH��2CO3��ǡ�ûָ������ǰ��Ũ�Ⱥ�pH �������Ƕ�����̼���ܽ⣩�����������ת�Ƶĵ��ӵ����ʵ���Ϊ��www.7caiedu.cn A��0.4mol B��0.5mol C��0.6mol D��0.8mol 11.��֪������� ���⽻������֪�����ᣨH3PO2��Ҳ�ɸ�D2O�����⽻�������������ƣ�NaH2PO2��ȴ�� ����ҲD2O�����⽻�����ɴ˿�֪����ķ��ӽṹΪ �� ��
12. �������ʵ�����F2��ClF��ϣ����ܱ������з�����Ӧ�� F2(g) ClF(g)�PClF3(g)�� ��H<0�����������У���ȷ���� A�����º���ʱ����ClF ת��40% ʱ�������ڵ�ѹǿΪ��ʼʱ��0.8 �� B���� c(F2):c (ClF): c (ClF3) =1: 1: 1�� ��Ӧһ���ﵽƽ��״̬ C���ﵽƽ������������������������Ӧ���ʼ�С���淴Ӧ��������ƽ������ D��ƽ����ٽ����¶ȣ����ֺ��ݣ��ﵽ�µ�ƽ�⣬���������ƽ��Ħ���������ܼ�С ����ѡ���������6С�⡣��ÿС��������ĸ�ѡ���У��е�ֻ��һ��ѡ����ȷ���е��ж��ѡ����ȷ��ȫ��ѡ�Եĵ�6�֣�ѡ�Ե���ȫ�ĵ�3�֣���ѡ���ĵ�0�֡���
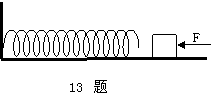 13.��ͼ��ʾ��һ����ڹ⻬��ˮƽ������һ����F�����ö��˶�������ǰ���̶�һ���㹻�������ʵ��ɣ�������뵯�ɽӴ����� 13.��ͼ��ʾ��һ����ڹ⻬��ˮƽ������һ����F�����ö��˶�������ǰ���̶�һ���㹻�������ʵ��ɣ�������뵯�ɽӴ�����
A����������������˶� B������ڿ�ʼ��һ��ʱ�������������˶� C�������ɵĵ������ں���Fʱ����龲ֹ D�������ɴ������ѹ����ʱ�����ļ��ٶȲ�Ϊ��
 14.��ͼ��ʾ��AΪ��ֹ�ڵ������ϵ����壬BΪ�Ƶ�������Բ������е����ǣ�CΪ�Ƶ�����Բ���˶������ǣ�PΪB��C�����ǹ���Ľ��㣮��֪A��B��C�Ƶ����˶���������ͬ������ڵ��ģ�����˵��������ȷ���� �� �� 14.��ͼ��ʾ��AΪ��ֹ�ڵ������ϵ����壬BΪ�Ƶ�������Բ������е����ǣ�CΪ�Ƶ�����Բ���˶������ǣ�PΪB��C�����ǹ���Ľ��㣮��֪A��B��C�Ƶ����˶���������ͬ������ڵ��ģ�����˵��������ȷ���� �� ��
A������A������C������ͬ��С�ļ��ٶ� B������C�������ٶȴ�������A���ٶ� C�����ܳ��֣��������ijһʱ������B��A�����Ϸ� D������B��P������м��ٶȴ�С������C�����м��ٶȴ�С��� 15.2008��1�·ݣ��ҹ��Ϸ��ֵ�������50�겻���Ĵ�ѩ�֣���ѹ�����·��������𣬶���ʹ����߱������������������߶�������ijѧУʵ�鰮��С�������������絼���������跢�ȳ����ľ��ַ���������ѹ������ѹ��ѹ����Ϊ��ѹ��ѹ���������·�ն˽�ѹ��ѹ����ģ�⸺��R0���棬������ĵ�·ԭ����ͼ��ʾ��RLΪ����ߵ��裬Ϊ��ģ������ߣ�ʵ��ʱ��һ��������˿����RL����������˿�����ѩ�У��ڱ�ѹ��ԭ��Ȧ���˼��Ͻ���������ֱ�ѩ�ڻ�������Ϊ���о���ó���Ч��������ģ��ʵ������������⣬�����������䣬������������ԣ�����Ϊ������������ǣ� ��
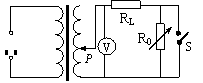 A������ѹ��ѹ��������ͷP�����ƶ�һЩ A������ѹ��ѹ��������ͷP�����ƶ�һЩ
B������ѹ��ѹ��������ͷP�����ƶ�һЩ��ͬʱ�ӳ�ͨ��ʱ�� C��ͨ�����㣬ѡ���ʵ������ѹ�����պ�S��ģ�⸺��R0��ʱ��· D��ͨ�����㣬ѡ���ʵ������ѹ������ģ�⸺��R0����ֵ����һЩ
 16.��ͼ��ʾ�����߿��ڴ��ھ��ȱ仯����ǿ�ų�������������ֵ֮�� 16.��ͼ��ʾ�����߿��ڴ��ھ��ȱ仯����ǿ�ų�������������ֵ֮�� A��0 B�� 17.һ�м�г�Შ������x��������������ijһʱ�̵IJ���ͼ����ͼ��ʾ�������ж���
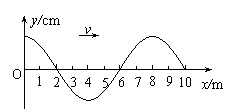 ��ȷ���� ��ȷ����
A�����в��IJ�����8m B����ʱ��x = 3m���ʵ�����y���������˶� C����ʱ��x = 6m���ʵ���ٶ�Ϊ0 D����ʱ��x = 7m���ʵ�ļ��ٶȷ�����y�Ḻ����
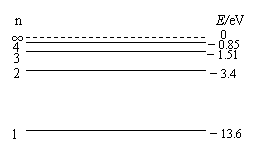 18.��ͼ��ʾ��������ԭ�Ӵ����ܼ�n��4�ļ���̬������������ϵ��ܼ�ԾǨʱ�����ڶ��ֿ��ܵ�ԾǨ������˵������ȷ���ǣ� �� 18.��ͼ��ʾ��������ԭ�Ӵ����ܼ�n��4�ļ���̬������������ϵ��ܼ�ԾǨʱ�����ڶ��ֿ��ܵ�ԾǨ������˵������ȷ���ǣ� ��
A�����ֻ�ܷų�4�ֲ�ͬƵ�ʵĹ��� B����n��4�ܼ�ԾǨ��n��1�ܼ��ų��Ĺ��Ӳ���� C����n��4�ܼ�ԾǨ��n��1�ܼ��ų��Ĺ���Ƶ����� D����n��4�ܼ�ԾǨ��n��3�ܼ��ų��Ĺ��Ӳ������ڴ�n��2�ܼ�ԾǨ��n��1�ܼ��ų��Ĺ��Ӳ��� �ڢ�� �ؿ����� �ڢ���ؿ����ֹ�9�⣬��157�֡�
 19.��18�֣���. ��1���ڡ��õ��ڲⶨ�������ٶȡ���ʵ���У��ٲ�ڳ�ʱ������ȷ������߳�l�Ͱ���ֱ��d����ڳ�Ϊ____________���ڲ�����ʱ��������_______λ��ʱ��ʼ��ʱ������1�Σ����������λ��N�Σ�Լ60��100�Σ���ʱ��Ϊt��������Ϊ________�� 19.��18�֣���. ��1���ڡ��õ��ڲⶨ�������ٶȡ���ʵ���У��ٲ�ڳ�ʱ������ȷ������߳�l�Ͱ���ֱ��d����ڳ�Ϊ____________���ڲ�����ʱ��������_______λ��ʱ��ʼ��ʱ������1�Σ����������λ��N�Σ�Լ60��100�Σ���ʱ��Ϊt��������Ϊ________��
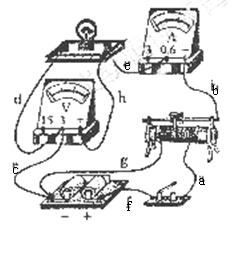
��.�ڡ����С���ݵķ����������ߡ�ʵ���У��õ���a��b��c��d��e��f��g��h����ͼ��ʾ��ʽ���ӵ�·����·������Ԫ��������ã�����ѹ���͵������ѵ��㣬�պϿ��غ� ������ѹ����ʾ��Ϊ2 V,�������ĵ�ʾ��Ϊ�㣬С���ݲ��������·�ĵ���Ϊ______�� ������ѹ����ʾ��Ϊ�㣬��������ʾ��Ϊ0.3 A,С�����������·�ĵ���Ϊ______�� �����������ڻ���������,С�������ȷ����仯������ѹ������������ʾ�����ܵ�Ϊ�㣬���·�ĵ���Ϊ_______��
�ٵ�ԴE��12V�����費�ƣ�
 �ڵ�����A��0~0.6A��0~3A������ɺ��ԣ� �ڵ�����A��0~0.6A��0~3A������ɺ��ԣ�
����ѹ��V��0~3V��0~15V������ܴ� �ܻ���������R����ֵ��Χ0~20������Ӧ������1A�� �ݿ���һ�����������ɡ� ʵ��ʱҪ����ڵ������˵ĵ�ѹ�ɴ�0��12V�����仯�� ���������߿��У�����ʵ���·ͼ.
�۰�ʵ���·ͼ��������ͼ3ʵ��ͼ�н������ӡ� ��ijλͬѧ���С���ݵķ�������������ͼ4��ʾ��ij�β���ʱ��������ָ��λ����ͼ5��ʾ������������Ϊ A����ʱС���ݵ�ʵ�ʹ���Ϊ W�� 20.(15��) ��ͼ��ʾ���⻬ˮƽ��AB����ֱ���ڵİ�Բ�ε�����B���νӣ�����뾶ΪR��һ������Ϊm�ľ�ֹ�����A��ѹ�����ɣ����뵯�ɲ�������M�ڵ����������»��һ���ҵ��ٶȣ���������B����뵼��˲�䣬�Թ����ѹ��Ϊ��������7����֮�������˶�ǡ����ɰ�Բ���˶�����C�㣬��
��2������B��C�˷��������Ĺ� ��3������뿪C������ˮƽ��ʱ�Ķ���
(1)��B����ߵ�ʱ���˶�ˮƽ�����������С�� (2)��Bת����͵�ʱ����A����B�Ը˵��������ֱ��Ƕ������Σ�
22.��20�֣���ͼ��ʾ��������Ϊm���������Ϊq�Ĵ������һ�����Ӵ�P1(һa��0)������ͬ������vo��xOyƽ���ڳ�x���Ϸ��ĸ����������(��0<�ȡܦ�)���������������Ӽ������ã�����֪a�㹻�� (1)����ͼ�е��ʵ�λ�ú������һ��ֱ��xOyƽ�桢�Ÿ�Ӧǿ��ΪB����ǿ�ų���ʹ��ش�������ͨ���ôų�����ƽ����x�᷽���˶�����ͼ�ж����������ӵ���С�ų�����߽�����κ�λ�ã� (2)����ͼ�е�ijЩ�����ټӴ�ֱ��xOyƽ�桢�Ÿ�Ӧǿ��ΪB����ǿ�ų���ʹ��Pl�㷢������ش�������ͨ���ų�����ͨ��P2(a��0)�㣮
�ڶ���������ͼʾvo��������Ĵ��������˶��Ĺ켣�� ��д�����Ӵų�������xOyƽ�����ɽ���߽�Ĺ켣���̣�
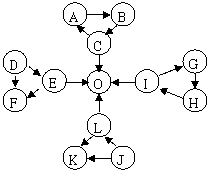 23.��15�֣�ijУ����С����̽����������ת��ʱ�����ֲ������ʿ��Դ�������ͼ��ʾ�����ǹ�ϵ����֪�� 23.��15�֣�ijУ����С����̽����������ת��ʱ�����ֲ������ʿ��Դ�������ͼ��ʾ�����ǹ�ϵ����֪��
�� ͼ��ÿ��С�����ε��������������ٺ��� һ����ͬԪ�ء� �ڣġ���Ϊ�������ʣ���Ϊ���嵥�ʣ���������Ϊ��������� �ۣ���ʹƷ����Һ��ɫ��Ҳ��ʹ�����ʯ��ˮ����ǣ���Ϊ����ɫ�������÷�Ӧ���ɣϣ���̷�ӦҲ�����ɣϣ��ˡ��̺�����ȫ��ͬ��Ԫ�ء� �ܣ�Ϊ������������ɣϣ��Ǻ̷ͣ�Ӧ����������ȣ��Ⱦ��н�ǿ�������ԡ� ������F�ĵ���ʽΪ��������������E������������ѧ�������� ������д���̡��ʵĻ�ѧ����ʽ���������������� ���� �����������£����һ��Ũ�ȣ���Һ��pH==10���������ӷ���ʽ��ʾ��ԭ�� ���������������������������������������������������������� ������д���źͣ÷�Ӧ�����ӷ���ʽ������������������������ ��
24.��15�֣�ѡ���Դ���ԭ(SCR)�����д����������½�NOx ת��ΪN2��H2O������Ŀǰ�������᳧����β���������ձ���õ�һ�ַ����� ijУ�ס���������ѧ����С������֤NO�ܱ�������ԭ��������ת���ʡ� ��һ����������ȡ�����Ǹ���ͭ���� �Ǹ���ͭ��Adkin�������Ǽ��õ�NO����ԭ�Ĵ�������ͭ���ĸ���������ɷֲ��̶����磺CuO��Cr2O3�ȣ�ͳ��Ϊ�Ǹ���ͭ������ͬѧȡһ��������ͭ��Һ�������������ᱵ���ȶ������� �ظ������Һ�백ˮ���õ�����ɫ������ ��������[���ⶨΪ����ʽ����ͭ泥�CuNH4(OH)CrO4 )]������ϴ�ӣ�80����12h�� ��������� ��1�������õ��IJ��������У� ��ѡ����ţ���ͬ���������õ��������У� �� A�������� B��ʯ���� C�������� D���ձ� E������ǯ F���ƾ��� G�������� H��©�� I��������������������ȥ�� ��2��CuNH4(OH)CrO4��295��ֽ����ɸ��ϵ��������������������ˮ���÷�Ӧ�Ļ�ѧ����ʽ: �� �������������ü����Ƶô������������̽���ʵ�顣
�Իش��������⣺ ��3������ȡ������Aװ�ã�������Ӧ�Ļ�ѧ����ʽΪ�� �� ����Bװ����ȡ���������Һ©������ƿ��ʢ�ŵ�ҩƷ�ֱ��ǣ� �� \* MERGEFORMAT ��4����ͼCװ����ȡNOʱ���ÿɳ鶯��ͭ˿���ŵ��ǣ� �� ��5��װ�âߵ����ÿ������� �� ��6��������װ�âݵ�NO��2688mL��������Ϊ��״������ͬ������������������ռ�����״����2016mLN2����NO��ת����Ϊ�� �� �⣺��1��D��G��H �� C��E��F��G��I����ѡ��ѡ�������֣��� ��2��2Cu(OH)NH4CrO4 ��3��2NH4Cl Ca(OH)2 ��5������δ��Ӧ��NO ��6��90% 25.��15�֣�������ʴ��ɺܴ�ľ�����ʧ������������Ȼ���ѣ����и�����ʴ��Ϊ���أ�Ѱ���ֹ������ʴ�ķ��������ش� ��1�������ı��淢�������ڴ����dz��õķ������������з�Ӧ����Ҫ��Ӧ֮һ�� ����ƽ����ʽ���� Na2FeO2 �� NaNO2 �� = �� NaFeO2 �� NH3�� �� NaOH
��ͼʾ��֪���ܶ�Ϊ 1.05g��mL��1 ������������Ӧʱ�������Ļ�ԭ������ ���ܶȴ���1.35 g��mL��1������������Ӧʱ���仹ԭ������Ҫ�� NO2������HNO3 ������Ӧ�Ĺ����ǣ� �� �� mg ���뺬 n g HNO3��������Һǡ����ȫ��Ӧ��������Ļ�ԭ����ֻ�� NO, �� m ��ȡֵ������ (����ĸ��� ) A�� �۹�ҵ��һ�㲻����Ũ������������洦��������ܵ�ԭ���ǣ� �� ��3������ (M) �ĸ�ʴ����Ϊ������Ӧ�� M��ne����Mn �������������洦���ķ����⣬���з���Ҳ���������õ��� ������ĸ��ţ� A�������в���������Ƚ������ı����ڲ��ṹ���Ƴɲ���� B��������Ʒ����ƴ� C��������к�̼�����Ƴ����� D����ˮ����բ����ֱ����Դ�ĸ������� 26.��25�֣��ش����Т�����
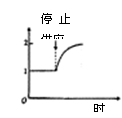
д�����б�������������ʻ��������̣� B D G I �� ��2�����ڽ�������������õ�ҶƬ�������Ȼֹͣ����CO2������ͼ6�л��Ҷ������NADPH�����ڶ�ʱ���ڵı仯���ߡ�
��3�� ͼ7��ʾ��������X���¶ȡ�����ǿ�ȡ�CO2Ũ�ȣ�����ɫֲ��������ǿ�ȵ�Ӱ�졣ͼ8��ʾ�ڲ�ͬ���¶ȣ�15�桢25�棩�����¹���ǿ�������������ʹ�ϵ�����ͼ������
1��ͼ7�д����¶���CO2Ũ�ȵ�Ӱ�����������DZ�� �� ���¶���Ҫͨ��Ӱ�������õ� ����Ӱ��������ǿ�ȵġ� 2��ͼ8�У�������ǿ��Ϊ10ǧ�տ�˹ʱ��Ӱ��������Ч�ʵĻ������������� �� 3��������ǿ�ȴ���0ʱ���ڹ���ǿ��Ϊ ǧ�տ�˹ʱ�������¶������µĺϳ��л������������ͬ�ġ� ������ǿ��Ϊ8���¶�Ϊ25��ʱ������ɫ2Сʱ���������ǵ����� �ˡ� ��. �������������ԡ�������ڵ���Ҫ;��ʾ��ͼ�ش����⣺ ________�������ڹ�������������֯�� �γ�Y���ȵ�ԭ����____________��
TRH��TSH�ķ�������________������ ��������________���ڡ� 27.��15�֣��Ķ����в��ϣ��ش��й����⣺ ��ѧ�ҷ��֣����������ijЩ���У����Ը������Ⱦɫ�������XY�����Ը������Ⱦɫ�������XX�����������ǵ������20�����ҷ���ʱ�����۱���ԼΪ1��1����������Щ�����30�����ҷ���ʱ����������ԭ�����к�����Ⱦɫ�壬ȫ�����������ԡ� ��1����ͬ�¶������·������ܵ��Ա�����в��죬��˵����__________________________________�� ��2�����⣺�ϸߵ��¶��Ǹı��˷����ŵ���XX������Ⱦɫ���ʹ֮�ı���״������ֻ�ı����Ա�ı������أ��������ʵ����̽����һ���⡣��ֻ˵���������˼·���ɣ� ���ϡ��þߣ�ͬһ˫�ײ��������������ܾ��ѡ���ͬ�����ϡ������������Լ��ȡ� ʵ�鲽�裺 ��ȡͬһ˫�ײ��������������ܾ��ѣ�ƽ���ֳ����ݣ������� ʵ����ף�____________________________________________________________, �������ң�____________________________________________________________�� ����ÿ���������ѡȡ����ֻ���ܱ�ţ���1��20��Ҫ�������㹻���ֱ��������ѡȡ�з���������ϸ�����д������Ƴ�__________�� ���������¹۲� _________________________________________������ͳ�ơ� ��Ԥ��ʵ����������ʵ������� a ʵ��Ԥ�ڣ���������ʵ���װƬ���۲쵽����ϸ������Ⱦɫ����ɾ���XX��XY��1��1 �������___________________________________________________________________�� bʵ��Ԥ�ڣ�________________________________________________________________�� ���������__________________________________________________________________�� ��3�����¶�ֻ�ı����ܵı����ͣ���30�������·����ɵ��������������ֳϸ���Ĺ����У�ϸ���к���XȾɫ�����Ϊ________���������к�XX�����������������·����ɵĴ��ܽ��䣬�����������º���Ա���_________�֡�
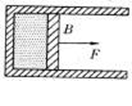
ѡ������ �ڢ��ѡ�����ֹ�5�⣬��35�֡����У���28��29��Ϊ�����⣬��30��31��Ϊ��ѧ�⣬���������������⡢������ѧ���и���ѡһ����������28��29�ⶼ������28��Ʒ֣�����30��31�ⶼ������30��Ʒ֣���32��Ϊ�����⣬�DZش��⡣�뽫�𰸶���д�ڴ��ѡ�������ָ��λ���ϡ� 28.����������ѡ��3��3�����������С�⣬ÿС��6�֣���12�֡�ÿС��ֻ��һ��ѡ��������⣩ ��1���̶���ˮƽ�������ɻ���B�����һ���������壬�������֮�������ÿ��Ժ��ԡ��������ױڵĵ������ܺܺã��������¶ȱ��ֲ��䣬��������F������B������������������ͼ��ʾ���������������Ĺ����У�������������������н��ۣ�������ȷ����( �� )
 A����������������������ܲ��� B����������������������ܼ�С A����������������������ܲ��� B����������������������ܼ�С
C�����������������������ܲ��� D�������������ȣ�����ѹǿ���� ��2��һ���ڱڹ⻬����粻�����ȴ��ݵ����̶��ڵ����ϣ����ڻ����·�����ſ�������
A������ƽ�����ܲ��� B����λʱ���ڸױڵ�λ������ܵ������������ײ�Ĵ������� C��ÿ�����ӶԸױڵij��������С D���������������ƣ�����F�Ի������Ĺ����ڸ����������ܵĸı��� 29.����������ѡ��3��5�����������С�⣬ÿС��6�֣���12�֡�ÿС��ֻ��һ��ѡ��������⣩ ��1��һ��
A.X��ԭ�Ӻ��к���86������ B.X��ԭ�Ӻ��к���141������ C.��Ϊ�ѱ��ͷ������������������������ѱ��������������� D. ��2������Ϊ4kg��װɰС����5m/s���ٶ��ع⻬ˮƽ���������˶�������Ϊ1ǧ�˵������0.2m�ߴ��������£�ǡ���복��ɰ����ٶ�Ϊ�� �� A. 5m/s B. 4.4m/s C. 4m/s D. 2m/s 30.����ѧ�������ʽṹ�����ʡ� ��1����Ԫ�����ڱ��У�ͬһ����Ԫ�ػ�ѧ�������ƣ�ĿǰҲ������ЩԪ�صĻ�ѧ���ʺ�����Ԫ�����ڱ������Ϸ������·�����һ����Ԫ���������ƣ����Ϊ�Խ��߹��� ��2����Щ������B(OH)3(����)��Al(OH)3����ԭ����ȱ���ӵģ������ǵ�����ԭ������������������8�����ӡ�Ϊ��ʹ������ԭ�Ӵﵽ8�����ȶ��ṹ������ԭ�ӿ��Խ������Ծ��й¶Ե��Ӷ�ԭ�ӵ�һ�Ե����γɷǷ��Ĺ��ۼ���������λ������λ�������á�������ʾ����(�������Ӷ�)A��B�����ܵ��Ӷԣ�������Ϊ���B(OH)3�����ᣩ��ˮ��Ҳ��һ�������ԣ������DZ��������H �����ǿ���ȡˮ�е�OH��ʹˮ�����H �Ӷ�ʹ��Һ�������ԡ� ����������Ϣ����ش����⣺ ��1����ڿ�����ȼ�ճ����� __�⣬Ҳ�������� _______(�û�ѧʽ��д)�� ��2�����������������Ӧ��ˮ����Ļ�ѧʽ�� ������________(�����ԡ����Ի�����)���������֤ʵ�����ʵ����ӷ���ʽ�� _______________________________________________�� ��3������֪��ӦBe2C 4H2O=2Be(OH)2 CH4������Al4C3Ͷ�����ǿ����Һ��Ӧ�����ӷ���ʽ�� �� ��4���������� �ᣬ����뷽��ʽΪ �� ��5����ѧ��֤ʵ���Ȼ������ڹ��ۻ��������ʽΪAl2Cl6����ṹʽΪ���������е�һ�֣�����Ϊ��ȷ�Ľṹ��______________��
31.����ѧ�����л���ѧ������ �������ͼ����
��֪��һ��̼ԭ�������������ǻ�ʱ����������ת����
��1��E�к��еĹ������� �� ��2����Ӧ�۵Ļ�ѧ�� �� ��3����֪B����Է�������Ϊ162������ȫȼ�յIJ�����n(CO2)��n (H2O)=2��1����B�ķ���ʽΪ �� ��4��F�Ǹ߷��ӹ���������е���Ҫԭ�ϡ�F���������ص㣺���ܸ�FeCl3��Һ������ɫ��Ӧ�����ܷ����Ӿ۷�Ӧ���۱����ϵ�һ�ȴ���ֻ�����֡�F��һ�������·����Ӿ۷�Ӧ�Ļ�ѧ����ʽΪ �� ��5��������G��F��ͬ���칹�壬���ڷ����廯����ܷ���������Ӧ��G�ж��ֽṹ��д������һ�ֵĽṹ��ʽ �� 32.��������ִ�����Ƽ�ר�⡿ ����ֲ��ϸ����������ũ������Ʒ�ֿ��Կ˷�ԶԵ�ӽ����͵��ϰ��������ͼ�ش�
��1����ͼ��ʾӦ����ֲ��ϸ�����̵ģߣߣߣߣߣߣߣߣߺͣߣߣߣߣߣߣߣ����� ��2��ϸ���ڶ�ֲ��ϸ������֧�ֺͱ������ã���ͼʾϸ��������Ҫͨ���٢ڹ���ȥ��ϸ���ڣ�Ӧ�ðѣߣߣߣߣߣ��ܽ��ڣߣߣߣߣ�ѡ���ţ�A����ˮ��B��һ��Ũ�ȵ�������Һ���Ʊ�ϸ���ڷֽ�Һ�� ��3�����̢ܲ����� ��־�ںϳɹ� ����������й�ϵ��ϸ���ṹ�ǣߣߣߣߣߣߣߡ�ϸ���ڵļӺ���Ҫϸ���Ѻϳɵ���ά�����͵�ϸ��Ĥ�⣬ϸ��������ά�صķ�ʽ�ǣߣߣߣߣߡ� ��4�����̢��ǰ��ӽ�ϸ������������ֲ�꣬����Ҫ���ӽ�ϸ�������ɣߣߣߣߣ���֯��Ȼ���յ����ٷֻ��γ�ֲ�꣬�ٷֻ���ԭ���ǣߣߣߣߣߣߣߣߣߣߣߣߡ� �ο��� ���Ծ���Ϊ�ڢ����ѡ���⣩�͵ڢ���� �ڢ����18С�⣬ÿ��6�֣���108�֡� һ��ѡ���⣺ѡ�Եĸ�6�֣�ѡ���Ļ�δѡ�ø�0�֡� 1.B 2.B 3.D 4.D 5.B 6.D 7.B 8.A 9.C 10.C 11.B 12.A
����ѡ���⣺ȫ��ѡ�Եĸ�6�֣�ѡ�Ե���ȫ�ĸ�3�֣���ѡ���û�δѡ�ĸ�0�֡�
�ڢ���ؿ����ֹ�9�⣬��157�֡� 19.(18��)
��. d���� ��2�֣� h���� ��2�֣� g���ߣ�2�֣� �ٵ�·ͼ��ͼ��(��) ��2�֣�
����ͼ(��) ��2�֣� ��0.40��1�֣� �� 2.4��1�֣�
20.��15�֣� ��1��EP=3mgR ��2��Wf=0.5mgR ��3��Ek=2.5mgR 21.��19�֣� �⣺(1)��B����ߵ�ʱ�ٶ�Ϊv0����
��ʱ��A���ٶ�Ϊ ���ʱ�˶���A��������ΪFA����
A��Ը˵�������Ϊ ˮƽ��Ը˵���������A��Ը˵�������ƽ�⣬�پ�ţ����������֪���˶�ˮƽ�����������СΪF0=1. 5 mg. ��1�֣� (2)����B����͵�ʱ���ٶ�Ϊ
��� ��A���� ��ø˶�A��������� ��B���� ��ø˶�B��������� ��ţ�ٵ������ɿ�֪��A��Ը˵���������СΪ0.3mg,�������ϣ�B�Ը˵���������СΪ3. 6mg���������£���2�֣�
22.��20�֣� �⣺(1)��������Ӵ�A���뿪�ų�����A������Ϊ(x��y)��������ת�İ뾶ΪR����ת��Բ����C�㣬��תԲ�Ľ�Ϊ������x��һa Rsin����y= R��Rcos����(4��) ���(x a)2 (yһR)2��R2��(3��) �ɼ������Ӵų��ı߽�Ĺ켣��һ����(һa��R)ΪԲ�ģ��뾶ΪR��mVo��Bq��Բ����Բλ��x���Ϸ�����P1�����У���3�֣� (2)���ݶԳ��Կɵó���P2�����ӵĴų���С����Ҳ��Բ��(1��) ͬ��������䷽��Ϊ(x-a)2 (yһR)2��R2 (2��) Բ��Ϊ(a��R)���뾶ΪR��mVo��Bq����Բλ��x���Ϸ�����P2�����У�(2��) �������ֶ����ж����ų�����ֱ��xOyƽ�����(1��)
�⣺����������ʽ��(2��) ���Ӽ����Ǽ��Թ��ۼ�(2��) ������CO2 Mg ������AlO2�� 2H2O==Al(OH)3 OH�� (4��) ������2Na2O2 4H ==4Na O2 2H2O (4��)
24.��15�֣� �⣺��1��D��G��H (2��) �� C��E��F��G��I����ѡ��ѡ�������֣���(2��) ��2��2Cu(OH)NH4CrO4 ��3��2NH4Cl Ca(OH)2 Ũ��ˮ����ʯ��(��ʯ�һ�������������) (2��) ��4����Ӧ������ʱ��ͣ���������㡢����ʹ�á���ԼҩƷ��(1��) ��5������δ��Ӧ��NO (1��) ��6��90%(2��) 25.��15�֣� �⣺��1�� ��2����NH3 ��NH4 ��2�֣���������ǣ������Ũ��Խ���仹ԭ�����е�Ԫ�ػ��ϼ�Խ�ߡ���3�֣� �����������𰸾����֡��������Ũ��Խ�������������ж��������ĺ���Խ�ߣ����ߣ�ֻ������Ũ�Ƚϵ�ʱ�������вŻ���ֵ������ȵȣ� ��B��C��D ����һ����������һ�֣�ȫ��2�֣���ֻҪ����A��E�㲻���֣� ��3�֣� �������ӷ����Ҳ��ȶ��������ֽ⣬�ʲ��ײ�����������Ի�����Ⱦ���� ��3�֣�
26.��25�֣� ����I������(1) H (1��) e (1��) ATP (1��)
 ��̼������ (1��) ������̼�̶� (1��) ��̼������ (1��) ������̼�̶� (1��)
��2��
(3��)
��3��1��d a (2��) ����Ӧ (1��) 2���¶�(1��) 3��0<����3 (2��) 93.6��10-3 (1��)
II����l���ټ�״�ټ����ͷż���(1��) ��������(1��)�� ��2������(1��) �ٽ��³´�л�������������ʵ������ֽ⣬�Ӷ����Ӳ�����(2��) ����3������(1��) ����(1��)����4����������(1��) Эͬ����(1��)�� ��5�����ں���Һ���� (1��)
27.��15�֣� �⣺(1)������״�ı��ֲ����ܻ�����ƶ����ܻ������ص�Ӱ�졣��2�֣� ��2����ʵ����ף� ��30�������½��������ɳ��� ��1�֣� �������ң���20�������½��������ɳ��ܣ�1�֣� ��װƬ��1�֣� ����Ⱦɫ����ɣ�Ⱦɫ����ɣ�����һ����Ⱦɫ�����ͷ�������2�֣� ��a ����������ϸߵ��¶�ֻ�ı����Ա�ı����͡���2�֣� b ʵ��Ԥ�ڣ�����ʵ���װƬ��30�������������ij��ܣ����۲쵽����ϸ������Ⱦɫ����ɶ���XY������ʵ���װƬ��20�������������ij��ܣ����۲쵽����ϸ������Ⱦɫ�������XX��XY��1��1 ��3�֣� ����������ϸߵ��¶�ʹ�����ŵ���XX����Ⱦɫ����ɱ��XY���Ӷ��ı����Ա�ı����͡���2�֣� ��3��2 ��1�֣� 1��1�֣�
�ڢ��ѡ�����ֹ�5�⣬��35�֡����У���28��29��Ϊ�����⣬��30��31��Ϊ��ѧ�⣬���������������⡢������ѧ���и���ѡһ����������28��29�ⶼ������28��Ʒ֣�����30��31�ⶼ������30��Ʒ֣���32��Ϊ�����⣬�DZش��⡣�뽫�𰸶���д�ڴ��ѡ�������ָ��λ���ϡ� 28.��12�֣� ��1��A ��2��B 29.��12�֣� ��1��A ��2��C 30.��13�֣� �⣺��1��Li2O��1�֣� Li3N ��1�֣� ��2��Be(OH)2��1�֣���������1�֣���Be(OH)2 2H ==Be2 2H2O ��1�֣� Be(OH)2 2OH-==BeO22- 2H2O��1�֣� ��3��Al4C3 4OH- 4H2O ==3CH4�� 4AlO2- ��3���� ��4���� ��1���� B(OH)3 H2O ��5��sp3 ��1���� ����6��1����
31.��13���� ��������1�� �Ȼ� (2��) ��2�� ��3��C10H10O2 (2��)
��4��
(3��)
��5��
(3��)
32.��10�֣� �⣺(1)ֲ����ϸ���ں�(1��) ֲ����֯���� (1��) ��2����ά��ø����ø (1��) B (1��) ��3���µ�ϸ����(1��) ��4���߶����� (1��) ����(1��) ��5������ (1��) ����ѡ�����(2��) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |